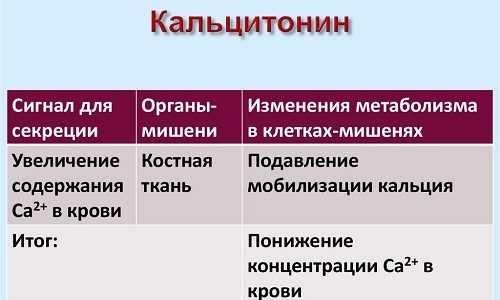
Как называется марганцовка
Раствор перманганата калия
Это ныне практически запрещенное, когда-то очень популярное, средство одно время почти исчезло из применения в обычной медицине. Но сейчас мы наблюдаем его «ренессанс», вернее, ренессанс осложнений после его применения. Так ли хорошо лечиться «запретным»?
Печальные последствия марганцовочной терапии
«Доктор, у меня это…» — почти как в анекдоте краснеет передо мной 19-летняя девушка. Успокаиваю, осматриваю. Что же, действительно ничего хорошего. Кожа лобка представляет собой конгломерат из рубцовой ткани, еще свежих ожогов, сукровицы и гноя.
Решившись на эпиляцию интимной зоны, девушка не знала, что фолликулиты (маленькие прыщики у корней удаленных волос) — обычное, довольно частое осложнение этой процедуры. Перепугалась… кто-то посоветовал марганцовку, а потом «что-то пошло не так»…
Девушку мы полечили, ожоги зажили, а вот сможет ли она у косметологов хоть как-то убрать грубые келоидные рубцы — вопрос. Понятное дело, что интимные прически ей теперь уже до конца жизни не делать…
Кто-то «лечил» экзему, кто-то «выводил» тату или бородавки, кому-то подсказали такое средство от запаха ног… всех их можно опознать по уродующим рубцам в месте применения чудо-лекарства. В последнее время таких пациентов становится больше и больше...
Читайте также:
Бриллиантовая зеленка
Где они берут средство, попавшее в Постановление Правительства РФ от 30.06.1998 № 681 «Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» (с изменениями и дополнениями), я не знаю — у кого-то запасы с давних времен, где-то торговцы плюют на запреты, надеясь на прибыль…

Опять отобрали у народа дешевое чудо-средство?
Перманганат калия (Kalii permanganas) — KMnO4 — красно-фиолетовые ромбические кристаллы или мелкий кристаллический порошок темно-фиолетового, почти черного цвета с металлическим блеском. Хорошо растворим в холодной воде (1:16), легко — в кипящей воде, образуя окрашенные в яркий красно-фиолетовый цвет растворы. Поверхностное антисептическое, прижигающее и дезодорирующее действие марганцовокислого калия обусловлено окислением им органических веществ.
Ореол «запретного плода», наверное, привлекает пользователей — раз запрещают, значит, это что-то суперэффективное, иначе бы не запрещали. Действительно, марганцовка очень эффективна — она убивает всю заразу, которая ей попадается, при этом еще и уничтожает запахи… Все бы хорошо, но есть одно но: рубцы после ожогов формируются практически всегда, и часто это уродующие, келоидные рубцы.
Как же так, спросите вы, ведь в советское время широко пользовались марганцовкой, даже пили ее с целью вызвать рвоту, и ничего… автор запугивает?
Ну, во-первых, ожоги пищевода и желудка в то время были не такой уж редкостью, во-вторых, в те времена ее и разводить умели.
Получить безопасный раствор почти нереально
Перед тем как писать эту статью, я специально полез в несколько поисковиков с вопросом: «как правильно разводить марганцовку?». Сотни статей с советами. Я смог прочесть около десятка — ни одна статья не приводила хотя бы минимально безопасного способа растворения этого медикамента.
Чего только не советуют:
...возьмите несколько кристаллов…
…светло-розовый цвет…
…используйте прозрачную посуду…
…перед применением взболтайте так, чтобы жидкость закружилась и нерастворившееся частички были видны...
…процедите через марлю...

Ни один из этих советов не дает безопасного раствора, потому что кристаллы перманганата калия, способные вызвать ожог, слишком малы, чтобы увидеть их невооруженным глазом, и иногда проходят даже через несколько слоев марли. Возмутительно, что в этом далеко не безопасном растворе рекомендуют купать даже младенцев.
В 1990-е годы был небольшой период тотального лекарственного дефицита. Тогда меня, еще молодого доктора, и научили разводить марганцовку. Сначала готовится первый, так называемый маточный раствор. Ему дают отстояться. Затем из верхних его слоев берут немного жидкости и уже из нее готовят раствор нужной концентрации. Все это происходит в темноте и при соблюдении температурного режима (объясняли, что в слишком холодном растворе — плохо растворяется, а если разводить в слишком горячем, то потом при остывании может опять кристаллизоваться).
В общем — мороки… И даже при таком, казалось бы, безопасном способе осложнения были не так редки.
Вскоре я перестал пользоваться марганцовкой в практике лечения людей (в ветеринарии и в уходе за растениями она по-прежнему актуальна), тем более что средств, не менее хорошо выполняющих ее функции, сейчас хоть отбавляй, они (если подобраны вам доктором и в соответствии с вашими особенностями заболевания и стадией воспалительного процесса, а не соседом по лестничной площадке или в интернет-источниках) более эффективны и уж куда более безопасны.
Конечно, марганцовку запретили не из-за этого, а по другим причинам, но это как раз тот случай, когда дерматологи поддерживают запрет.
Крепкого здоровья!
Леонид Щеботанский
Фото istockphoto.com
Товары по теме: борная к-та, ихтиол, перекись водорода, Йодинол, йода спирт р-р, фурацилин, Фурагин, хлоргексидина биглюконат
Марганец — Википедия
| Марганец | |
|---|---|
| ← Хром | Железо → | |
| Твёрдый, хрупкий металл серебристо-белого цвета | |
| Электролитический марганец | |
| Название, символ, номер | Марганец / Manganum (Mn), 25 |
| Атомная масса (молярная масса) |
54,938045 (5)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d5 4s2 |
| Радиус атома | 127 пм |
| Ковалентный радиус | 117 пм |
| Радиус иона | (+7e) 46 (+2e) 80 пм |
| Электроотрицательность | 1,55 (шкала Полинга) |
| Электродный потенциал | −1,180 В |
| Степени окисления | 7, 6, 5, 4, 3, 2, 1, 0 |
| Энергия ионизации (первый электрон) | 716,8 (7,43) кДж/моль (эВ) |
| Плотность (при н. у.) | 7,21 г/см³ |
| Температура плавления | 1 517 K |
| Температура кипения | 2 235 K |
| Уд. теплота плавления | 13,4 кДж/моль |
| Уд. теплота испарения | 221 кДж/моль |
| Молярная теплоёмкость | 26,3[2] Дж/(K·моль) |
| Молярный объём | 7,35 см³/моль |
| Структура решётки | кубическая |
| Параметры решётки | 8,890 Å |
| Температура Дебая | 400 K |
| Теплопроводность | (300 K) 6,87[3] Вт/(м·К) |
| Номер CAS | 7439-96-5 |
| 25 | Марганец |
| 3d54s2 | |
Ма́рганец — элемент 7-й группы (по устаревшей классификации — побочной подгруппы седьмой группы) четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 25. Обозначается символом Mn (лат. Manganum, ма́нганум, в составе формул по-русски читается как марганец, например, KMnO4 — калий марганец о четыре). Простое вещество марганец — металл серебристо-белого цвета. Наряду с железом и его сплавами относится к чёрным металлам. Известны пять аллотропных модификаций марганца — четыре с кубической и одна с тетрагональной кристаллической решёткой[2].
Один из основных минералов марганца — пиролюзит — был известен в древности как чёрная магнезия и использовался при варке стекла для его осветления. Его считали разновидностью магнитного железняка, а тот факт, что он не притягивается магнитом, Плиний Старший объяснил женским полом чёрной магнезии, к которому магнит «равнодушен». В 1774 году шведский химик К. Шееле показал, что в руде содержится неизвестный металл. Он послал образцы руды своему другу химику Ю. Гану, который, нагревая в печке пиролюзит с углем, получил металлический марганец. В начале XIX века для него было принято название «манганум» (от нем. Manganerz — марганцевая руда).
Марганец — 14-й элемент по распространённости на Земле, а после железа — второй тяжёлый металл, содержащийся в земной коре (0,03 % от общего числа атомов земной коры). Массовая доля марганца увеличивается от кислых (600 г/т) к основным породам (2,2 кг/т). Сопутствует железу во многих его рудах, однако встречаются и самостоятельные месторождения марганца. В чиатурском месторождении (район Кутаиси) сосредоточено до 40 % марганцевых руд. Марганец, рассеянный в горных породах, вымывается водой и уносится в Мировой океан. При этом его содержание в морской воде незначительно (10−7—10−6 %), а в глубоких местах океана его концентрация возрастает до 0,3 % вследствие окисления растворённым в воде кислородом с образованием нерастворимого в воде оксида марганца, который в гидратированной форме (MnO2·xH2O) и опускается в нижние слои океана, формируя так называемые железомарганцевые конкреции на дне, в которых количество марганца может достигать 45 % (также в них имеются примеси меди, никеля, кобальта). Такие конкреции могут стать в будущем источником марганца для промышленности.
В России является остродефицитным сырьём, известны месторождения: «Усинское» в Кемеровской области, «Полуночное» в Свердловской, «Порожинское» в Красноярском крае, «Южно-Хинганское» в Еврейской автономной области, «Рогачёво-Тайнинская» площадь и «Северо-Тайнинское» поле на Новой Земле.
Минералы марганца[править | править код]
- Алюминотермическим методом, восстанавливая оксид Mn2O3, образующийся при прокаливании пиролюзита:
- 4MnO2⟶2Mn2O3+O2{\displaystyle {\ce {4 MnO2 -> 2 Mn2O3 + O2}}}
- Mn2O3+2Al⟶2Mn+Al2O3{\displaystyle {\ce {Mn2O3 + 2 Al -> 2 Mn + Al2O3}}}
- Восстановлением железосодержащих оксидных руд марганца коксом. Этим способом в металлургии обычно получают ферромарганец (~80 % Mn).
- Чистый металлический марганец получают электролизом.
Некоторые свойства приведены в таблице. Другие свойства марганца:
- Работа выхода электрона: 4,1 эВ
- Коэффициент теплового расширения: 0,000022 K−1 (при 0 °C)
- Электропроводность: 0,00695⋅106 Ом−1·см−1
- Теплопроводность: 0,0782 Вт/(см·K)
- Энтальпия атомизации: 280,3 кДж/моль при 25 °C
- Энтальпия плавления: 14,64 кДж/моль
- Энтальпия испарения: 219,7 кДж/моль
- Твёрдость:
- по шкале Бринелля: Мн/м²
- по шкале Мооса: 4[4]
- Давление паров: 121 Па при 1244 °C
- Молярный объём: 7,35 см³/моль
| Окисленная форма | Восстановленная форма | Среда | E0, В |
|---|---|---|---|
| Mn2+ | Mn | H+ | −1,186 |
| Mn3+ | Mn2+ | H+ | +1,51 |
| MnO2 | Mn3+ | H+ | +0,95 |
| MnO2 | Mn2+ | H+ | +1,23 |
| MnO2 | Mn(OH)2 | OH− | −0,05 |
| MnO42− | MnO2 | H+ | +2,26 |
| MnO42− | MnO2 | OH− | +0,62 |
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |
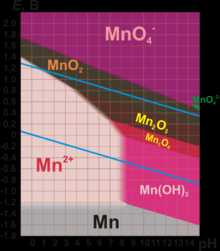
Характерные степени окисления марганца: 0, +2, +3, +4, +6, +7 (степени окисления +1, +5 малохарактерны).
При окислении на воздухе пассивируется. Порошкообразный марганец сгорает в кислороде:
- Mn+O2⟶MnO2{\displaystyle {\ce {Mn + O2 -> MnO2}}}
Марганец при нагревании разлагает воду, вытесняя водород:
- Mn+2h3O→∘tMn(OH)2+h3↑{\displaystyle {\ce {Mn{}+2h3O->[^{\circ }t]Mn(OH)2{}+h3\uparrow }}}
При этом слой образующегося гидроксида марганца замедляет реакцию.
Марганец поглощает водород, с повышением температуры его растворимость в марганце увеличивается. При температуре выше 1200 °C взаимодействует с азотом, образуя различные по составу нитриды.
Углерод реагирует с расплавленным марганцем, образуя карбиды Mn3C и другие. Образует также силициды, бориды, фосфиды.
С соляной и серной кислотами реагирует по уравнению
- Mn+2H+⟶Mn2++h3↑{\displaystyle {\ce {Mn{}+2H^{+}->Mn^{2}+{}+h3\uparrow }}}
С концентрированной серной кислотой реакция идёт по уравнению
- Mn+2h3SO4⟶MnSO4+SO2↑+2h3O{\displaystyle {\ce {Mn{}+2h3SO4->MnSO4{}+SO2\uparrow +2h3O}}}
С разбавленной азотной кислотой реакция идёт по уравнению
- 3Mn+8HNO3⟶3Mn(NO3)2+2NO↑+4h3O{\displaystyle {\ce {3Mn{}+8HNO3->3Mn(NO3)2{}+2NO\uparrow +4h3O}}}
В щелочном растворе марганец устойчив.
Марганец образует следующие оксиды: MnO, Mn2O3, MnO2, MnO3 (не выделен в свободном состоянии) и марганцевый ангидрид Mn2O7.
Mn2O7 в обычных условиях — жидкое маслянистое вещество тёмно-зелёного цвета, очень неустойчивое; в смеси с концентрированной серной кислотой воспламеняет органические вещества. При 90 °C Mn2O7 разлагается со взрывом. Наиболее устойчивы оксиды Mn2O3 и MnO2, а также комбинированный оксид Mn3O4 (2MnO·MnO2, или соль Mn2MnO4).
При сплавлении оксида марганца (IV) (пиролюзит) со щелочами в присутствии кислорода образуются манганаты:
- 2MnO2+4KOH+O2⟶2K2MnO4+2h3O{\displaystyle {\ce {2 MnO2{}+ 4 KOH{}+ O2 -> 2 K2MnO4{}+ 2 h3O}}}
Раствор манганата имеет тёмно-зелёный цвет. При подкислении протекает реакция
- 3K2MnO4+3h3SO4⟶3K2SO4+2HMnO4+MnO(OH)2↓+h3O{\displaystyle {\ce {3 K2MnO4{}+ 3 h3SO4 -> 3 K2SO4{}+ 2 HMnO4{}+ MnO(OH)2 v + h3O}}}
Раствор окрашивается в малиновый цвет из-за появления аниона MnO4−, и из него выпадает коричневый осадок оксида-гидроксида марганца (IV).
Марганцевая кислота очень сильная, но неустойчивая, её невозможно сконцентрировать более, чем до 20 %. Сама кислота и её соли (перманганаты) — сильные окислители. Например, перманганат калия в зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца (II), в нейтральной — до соединений марганца (IV), в сильно щелочной — до соединений марганца (VI).
При прокаливании перманганаты разлагаются с выделением кислорода (один из лабораторных способов получения чистого кислорода). Реакция идёт по уравнению (на примере перманганата калия)
- 2KMnO4→∘tK2MnO4+MnO2+O2{\displaystyle {\ce {2KMnO4->[^{\circ }t]K2MnO4{}+MnO2{}+O2}}}
Под действием сильных окислителей ион Mn2+ переходит в ион MnO4−:
- 2MnSO4+5PbO2+6HNO3⟶2HMnO4+2PbSO4+3Pb(NO3)2+2h3O{\displaystyle {\ce {2 MnSO4{}+ 5 PbO2{}+ 6 HNO3 -> 2 HMnO4{}+ 2 PbSO4{}+ 3 Pb(NO3)2{}+ 2 h3O}}}
Эта реакция используется для качественного определения Mn2+ (см. в разделе «Определение методами химического анализа»).
При подщелачивании растворов солей Mn (II) из них выпадает осадок гидроксида марганца (II), быстро буреющий на воздухе в результате окисления. Подробное описание реакции см. в разделе «Определение методами химического анализа». В нейтральных или кислых водных растворах ион Mn2+ образует окрашенный в бледно-розовый цвет аквакомплекс [Mn(H2O)6]2+.
Соли MnCl3, Mn2(SO4)3 неустойчивы. Гидроксиды Mn(OH)2 и Mn(OH)3 имеют основный характер, MnO(OH)2 — амфотерный. Хлорид марганца (IV) MnCl4 очень неустойчив, разлагается при нагревании, чем пользуются для получения хлора:
- MnO2+4HCl⟶MnCl2+Cl2↑+2h3O{\displaystyle {\ce {MnO2{}+4HCl->MnCl2{}+Cl2\uparrow +2h3O}}}
Нулевая степень окисления у марганца проявляется в соединениях с σ-донорными и π-акцепторными лигандами. Так, для марганца и известен карбонил состава Mn2(CO)10.
Известны и другие соединения марганца с σ-донорными и π-акцепторными лигандами (PF3, NO, N2, P(C5H5)3).
Марганец является моноизотопным элементом — в природе существует только один устойчивый изотоп 55Mn. Все другие изотопы марганца нестабильны и радиоактивны, они получены искусственно. Известны 25 радиоактивных изотопов марганца, имеющие массовое число А в диапазоне от 44 до 70. Наиболее стабильными из них являются 53Mn (период полураспада T1/2 = 3,7 млн лет), 54Mn (T1/2 = 312,3 суток) и 52Mn (T1/2 = 5,591 суток). Преобладающим каналом распада лёгких изотопов марганца (А < 55) является электронный захват (и иногда конкурирующий с ним позитронный распад) в соответствующие изотопы хрома. У тяжёлых изотопов (А > 55) основным каналом распада является β−-распад в соответствующие изотопы железа. Известны также 7 изомеров (метастабильных возбуждённых состояний) с периодами полураспада более 100 нс.
Применение в металлургии[править | править код]
Марганец в виде ферромарганца применяется для раскисления стали при её плавке, то есть для удаления из неё кислорода. Кроме того, он связывает серу, что также улучшает свойства сталей. Введение до 12—13 % Mn в сталь (так называемая сталь Гадфильда), иногда в сочетании с другими легирующими металлами, сильно упрочняет сталь, делает её твёрдой и сопротивляющейся износу и ударам (т. н. «наклёп»). Такая сталь используется для изготовления шаровых мельниц, землеройных и камнедробильных машин, броневых элементов и т. д. В «зеркальный чугун» вводится до 20 % Mn.
В 1920—1940-х годах применение марганца позволяло выплавлять броневую сталь. В начале 1950-х годов в журнале «Сталь» возникла дискуссия по вопросу о возможности снижения содержания марганца в чугуне, и тем самым отказа от поддержки определённого содержания марганца в процессе мартеновской плавки, в которой вместе с В. И. Явойским и В. И. Баптизманским принял участие Е. И. Зарвин, который на основе производственных экспериментов показал нецелесообразность существовавшей технологии. Позже он показал возможность ведения мартеновского процесса на маломарганцовистом чугуне. С пуском ЗСМК началась разработка передела низкомарганцовистых чугунов в конвертерах.[5]
Сплав 83 % Cu, 13 % Mn и 4 % Ni (манганин) обладает высоким электросопротивлением, мало изменяющимся с изменением температуры. Поэтому его применяют для изготовления реостатов и пр.
Марганец вводят в бронзы и латуни.
Применение в химии[править | править код]
Значительное количество диоксида марганца потребляется при производстве марганцево-цинковых гальванических элементов, MnO2 используется в таких элементах в качестве окислителя-деполяризатора.
Соединения марганца также широко используются как в тонком органическом синтезе (MnO2 и KMnO4 в качестве окислителей), так и промышленном органическом синтезе (компоненты катализаторов окисления углеводородов, например, в производстве терефталевой кислоты окислением p-ксилола, окисление парафинов в высшие жирные кислоты).
Арсенид марганца обладает гигантским магнитокалорическим эффектом, усиливающимся под давлением.
Теллурид марганца — перспективный термоэлектрический материал (термо-ЭДС 500 мкВ/К).
Определение методами химического анализа[править | править код]
Марганец принадлежит к пятой аналитической группе катионов.
Специфические реакции, используемые в аналитической химии для обнаружения катионов Mn2+, следующие:
1. Едкие щёлочи с солями марганца (II) дают белый осадок гидроксида марганца (II):
- MnSO4+2KOH→Mn(OH)2↓+K2SO4{\displaystyle {\mathsf {MnSO_{4}+2KOH\rightarrow Mn(OH)_{2}\downarrow +K_{2}SO_{4}}}}
- Mn2++2OH−→Mn(OH)2↓{\displaystyle {\mathsf {Mn^{2+}+2OH^{-}\rightarrow Mn(OH)_{2}\downarrow }}}
Осадок на воздухе меняет цвет на бурый из-за окисления кислородом воздуха.
Выполнение реакции. К двум каплям раствора соли марганца добавляют две капли раствора щёлочи. Наблюдают изменение цвета осадка.
2. Пероксид водорода в присутствии щёлочи окисляет соли марганца (II) до тёмно-бурого соединения марганца (IV):
- MnSO4+h3O2+2NaOH→MnO(OH)2↓+Na2SO4+h3O{\displaystyle {\mathsf {MnSO_{4}+H_{2}O_{2}+2NaOH\rightarrow MnO(OH)_{2}\downarrow +Na_{2}SO_{4}+H_{2}O}}}
- Mn2++h3O2+2OH−→MnO(OH)2↓+h3O{\displaystyle {\mathsf {Mn^{2+}+H_{2}O_{2}+2OH^{-}\rightarrow MnO(OH)_{2}\downarrow +H_{2}O}}}
Выполнение реакции. К двум каплям раствора соли марганца добавляют четыре капли раствора щёлочи и две капли раствора H2O2.
3. Диоксид свинца PbO2 в присутствии концентрированной азотной кислоты при нагревании окисляет Mn2+ до MnO4− с образованием марганцевой кислоты малинового цвета:
- 2MnSO4+5PbO2+6HNO3→2HMnO4+2PbSO4↓+3Pb(NO3)2+2h3O{\displaystyle {\mathsf {2MnSO_{4}+5PbO_{2}+6HNO_{3}\rightarrow 2HMnO_{4}+2PbSO_{4}\downarrow +3Pb(NO_{3})_{2}+2H_{2}O}}}
- 2Mn2+
| Перманганат калия | |
|---|---|
({{{картинка3D}}}) | |
 ( ({{{изображение}}}) | |
| Общие | |
| Систематическое наименование | Перманганат калия |
| Традиционные названия | Марганцовокислый калий, марганцовка |
| Хим. формула | KMnO4 |
| Физические свойства | |
| Состояние | твердое (хрупкие кристаллы) |
| Молярная масса | 158,034 г/моль |
| Плотность | 2,703 г/см³ |
| Термические свойства | |
| Температура | |
| • разложения | 240 °C |
| Мол. теплоёмк. | 119,2 Дж/(моль·К) |
| Энтальпия | |
| • образования | -813,4 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 6,38 (20 °C) |
| Классификация | |
| Рег. номер CAS | 7722-64-7 |
| PubChem | 516875 |
| Рег. номер EINECS | 231-760-3 |
| SMILES | [O-] [Mn](=O)(=O)=O.[K+] |
| InChI | 1S/K.Mn.4O/q+1;;;;;-1VZJVWSHVAAUDKD-UHFFFAOYSA-N |
| RTECS | SD6475000 |
| Номер ООН | 1490 |
| ChemSpider | 22810 |
| Безопасность | |
| Токсичность | низкая |
| NFPA 704 | |
Почему запретили марганцовку и как ее теперь можно приобрести :: SYL.ru
Еще несколько лет назад в каждом доме был пузырек с фиолетовым кристаллами, в народе называемыми марганцовкой. Этот раствор использовался для разных целей. И многие помнят розовую, неприятную на вкус воду, которую приходилось пить при отравлениях или обрабатывать ей раны. Но в последние годы многие люди столкнулись с проблемой: невозможно приобрети этот препарат. И они в недоумении: почему запретили марганцовку? Ведь этот дешевый антисептик часто незаменим в быту и медицине.
Лечебные свойства марганцовки
Научное название этого препарата - перманганат калия. Он является самым популярным антисептиком для наружного и внутреннего применения. Свежий раствор марганцовки обладает окисляющими свойствами и способен убить большинство микробов. Как же применяется марганцовка?

- слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
- более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
- в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
- марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
- хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
- ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.

До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
При разведении препарата нужно внимательно следить, чтобы его кристаллы не попали на кожу и слизистые и полностью растворились в воде. Ведь они могут вызвать сильный ожог и раздражение кожи. Поэтому при приготовлении препарата рекомендуют сначала приготовить более концентрированный раствор, а потом уже его добавлять в воду.
 Особенно это важно при внутреннем применении марганцовки и при использовании ее для ванночек ребенку. Кроме того, перманганат калия является легковоспламеняющимся веществом, и может произойти взрыв при трении его кристаллов о железо или при нарушении условий хранения.
Особенно это важно при внутреннем применении марганцовки и при использовании ее для ванночек ребенку. Кроме того, перманганат калия является легковоспламеняющимся веществом, и может произойти взрыв при трении его кристаллов о железо или при нарушении условий хранения.Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
1. Соли калия очень нестабильны и при определенных условиях могут воспламеняться, вплоть до взрыва. Это может произойти даже при комнатной температуре и при несоблюдении условий хранения препарата. Этим свойством часто пользуются террористы при изготовлении взрывных устройств. Это одна из причин, почему запретили продажу марганцовки в больших количествах.
2. Кроме того, перманганат калия относится к средствам, которые называются "перекурсоры". Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Но как ни странно, официально реализация перманганата калия в аптеках не запрещена, а просто ограничена.
 Те, кто с возмущеньем интересуются, почему запретили продавать марганцовку, получают ответ, что купить ее все-таки можно. Продается препарат по рецепту врача или в небольшом количестве, по 1-2 пакетика в одни руки. Оказывается, на аптеки наложили строгие ограничения и ввели новые правила относительно хранения и продажи препарата. Во многих городах провизоров обязуют вести строгий учет прихода и расхода марганцовки. А сами аптеки должны быть оборудованы специально для безопасного хранения этого взрывоопасного препарата. Поэтому большинство хозяев аптечного бизнеса отказываются продавать такое "неудобное", к тому же недорогое лекарство. Потому приобрести марганцовку можно, но в немногих государственных учреждениях.
Те, кто с возмущеньем интересуются, почему запретили продавать марганцовку, получают ответ, что купить ее все-таки можно. Продается препарат по рецепту врача или в небольшом количестве, по 1-2 пакетика в одни руки. Оказывается, на аптеки наложили строгие ограничения и ввели новые правила относительно хранения и продажи препарата. Во многих городах провизоров обязуют вести строгий учет прихода и расхода марганцовки. А сами аптеки должны быть оборудованы специально для безопасного хранения этого взрывоопасного препарата. Поэтому большинство хозяев аптечного бизнеса отказываются продавать такое "неудобное", к тому же недорогое лекарство. Потому приобрести марганцовку можно, но в немногих государственных учреждениях.Как относятся люди к такому запрету
У некоторых в доме еще остались старые запасы такого нужного препарата. Но те, кто столкнулся с необходимостью купить новую упаковку этого антисептика, выясняют, что марганцовка запрещена. Почему? Люди в недоумении.
 Ведь существуют еще более опасные препараты и вещества, используемые для приготовления наркотиков. И в то же время они находятся в свободной продаже. Это например, ацетон или средство для прочистки труб "Крот". Для изготовления наркотических средств используется также дистиллированная вода, сахар, кофе и многие другие вещества. Но в ограниченной продаже оказалась только марганцовка. Почему запрещена, причины этого не могут внятно разъяснить ни в одной аптеке. Поэтому люди часто возмущаются. А то, что это пока еще не стало массовым процессом, можно объяснить запасами перманганата калия во многих домах.
Ведь существуют еще более опасные препараты и вещества, используемые для приготовления наркотиков. И в то же время они находятся в свободной продаже. Это например, ацетон или средство для прочистки труб "Крот". Для изготовления наркотических средств используется также дистиллированная вода, сахар, кофе и многие другие вещества. Но в ограниченной продаже оказалась только марганцовка. Почему запрещена, причины этого не могут внятно разъяснить ни в одной аптеке. Поэтому люди часто возмущаются. А то, что это пока еще не стало массовым процессом, можно объяснить запасами перманганата калия во многих домах.Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Марганцовка как называется — Здоровье феникса
Еще несколько лет назад в каждом доме был пузырек с фиолетовым кристаллами, в народе называемыми марганцовкой. Этот раствор использовался для разных целей. И многие помнят розовую, неприятную на вкус воду, которую приходилось пить при отравлениях или обрабатывать ей раны. Но в последние годы многие люди столкнулись с проблемой: невозможно приобрети этот препарат. И они в недоумении: почему запретили марганцовку? Ведь этот дешевый антисептик часто незаменим в быту и медицине.
Содержание статьи:
Лечебные свойства марганцовки
Научное название этого препарата — перманганат калия. Он является самым популярным антисептиком для наружного и внутреннего применения. Свежий раствор марганцовки обладает окисляющими свойствами и способен убить большинство микробов. Как же применяется марганцовка?
— слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
— более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
— в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
— марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
— хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
— ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
При разведении препарата нужно внимательно следить, чтобы его кристаллы не попали на кожу и слизистые и полностью растворились в воде. Ведь они могут вызвать сильный ожог и раздражение кожи. Поэтому при приготовлении препарата рекомендуют сначала приготовить более концентрированный раствор, а потом уже его добавлять в воду. Особенно это важно при внутреннем применении марганцовки и при использовании ее для ванночек ребенку. Кроме того, перманганат калия является легковоспламеняющимся веществом, и может произойти взрыв при трении его кристаллов о железо или при нарушении условий хранения.
Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
1. Соли калия очень нестабильны и при определенных условиях могут воспламеняться, вплоть до взрыва. Это может произойти даже при комнатной температуре и при несоблюдении условий хранения препарата. Этим свойством часто пользуются террористы при изготовлении взрывных устройств. Это одна из причин, почему запретили продажу марганцовки в больших количествах.
2. Кроме того, перманганат калия относится к средствам, которые называются «перекурсоры». Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Но как ни странно, официально реализация перманганата калия в аптеках не запрещена, а просто ограничена. Те, кто с возмущеньем интересуются, почему запретили продавать марганцовку, получают ответ, что купить ее все-таки можно. Продается препарат по рецепту врача или в небольшом количестве, по 1-2 пакетика в одни руки. Оказывается, на аптеки наложили строгие ограничения и ввели новые правила относительно хранения и продажи препарата. Во многих городах провизоров обязуют вести строгий учет прихода и расхода марганцовки. А сами аптеки должны быть оборудованы специально для безопасного хранения этого взрывоопасного препарата. Поэтому большинство хозяев аптечного бизнеса отказываются продавать такое «неудобное», к тому же недорогое лекарство. Потому приобрести марганцовку можно, но в немногих государственных учреждениях.
Как относятся люди к такому запрету
У некоторых в доме еще остались старые запасы такого нужного препарата. Но те, кто столкнулся с необходимостью купить новую упаковку этого антисептика, выясняют, что марганцовка запрещена. Почему? Люди в недоумении. Ведь существуют еще более опасные препараты и вещества, используемые для приготовления наркотиков. И в то же время они находятся в свободной продаже. Это например, ацетон или средство для прочистки труб «Крот». Для изготовления наркотических средств используется также дистиллированная вода, сахар, кофе и многие другие вещества. Но в ограниченной продаже оказалась только марганцовка. Почему запрещена, причины этого не могут внятно разъяснить ни в одной аптеке. Поэтому люди часто возмущаются. А то, что это пока еще не стало массовым процессом, можно объяснить запасами перманганата калия во многих домах.
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Source: www.syl.ru
Читайте также
Марганцовка - это... Что такое Марганцовка?
Калия перманганат (лат. Kalii permanganas) — марганцовокислый калий, калиевая соль марганцевой кислоты KMnO4.
- Распространённое название в быту — марганцовка
Физические свойства
Внешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления σ 1,59 (при 20°C).
Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/моль·K (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/моль·K (т) (при 298 К) |
Химические свойства
Сильный окислитель. Стандартные окислительно-восстановительные потенциалы приведены в таблице.
| Окисленная форма | Восстановленная форма | Среда | E0, В |
|---|---|---|---|
| MnO4- | MnO42- | OH- | +0,56 |
| MnO4- | H2MnO4 | H+ | +1,22 |
| MnO4- | MnO2 | H+ | +1,69 |
| MnO4- | MnO2 | OH- | +0,60 |
| MnO4- | Mn2+ | H+ | +1,51 |
В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия:
в кислой среде: 2KMnO4 + 5K2SO3 + 3H2SO4 → 6K2SO4 + 2MnSO4 + 3H2O
в нейтральной среде: 2KMnO4 + 3K2SO3 + H2O → 3K2SO4 + 2MnO2 + 2KOH
в щелочной среде: 2KMnO4 + K2SO3 + 2KOH → K2SO4 + 2K2MnO4 + H2O, KMnO4 + K2SO3 + KOH → K2SO4 + K3MnO4 + H2O (на холоду)
Однако надо отметить, что в последняя реакция (в щелочной среде) идёт по указаной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
2KMnO4 + 2H2SO4 → 2KHSO4 + Mn2O7 + H2O,при этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4. По реакции с фторидом йода(V) можно получить аналогичный оксофторид:
KMnO4 + IF5 → KF + IOF3 + MnO3F
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
2KMnO4 →(t) K2MnO4 + MnO2+ O2↑
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
5KMnO4 →(t) K2MnO4 +K3MnO4 + 3MnO2+ 3O2↑
Реагирует с солями двухвалентного марганца, например:
2KMnO4 + 3MnSO4 + 2H2O → 5MnO2 + K2SO4 + 2H2SO4
Эта реакция коммутации в принципе обратна дисмутации (диспропорционирование) K2MnO4 на MnO2 и KMnO4.
- Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
Применение
Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
Медицинское применение
Разбавленные растворы (около 0,1%) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при некоторых отравлениях используют разбавленный раствор.
Фармакологическое действие
Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения - альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах - раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв. Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая гематотоксическое действие (приводит к развитию метгемоглобинемии). Используется так же в гомеопатии.
Показания
Смазывание язвенных и ожоговых поверхностей - инфицированные раны, язвы и ожоги кожи. Полоскание полости рта и ротоглотки - при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в т.ч. при ангинах). Для промывания и спринцеваний при гинекологических и урологических заболеваниях - кольпиты и уретриты. Для промываний - желудка при отравлениях, вызванных приемом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи - при попадании на нее анилина; глаз - при поражении их ядовитыми насекомыми.
Противопоказания
Гиперчувствительность.
Побочные действия
Аллергические реакции, при использовании концентрированных растворов - ожоги и раздражение. Передозировка. Симптомы: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки - отечная, темно-коричневого, фиолетового цвета, возможен отек гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей - около 3 г, для взрослых - 0.3-0.5 г/кг. Лечение: метиленовый синий (50 мл 1% раствора), аскорбиновая кислота (в/в - 30 мл 5% раствора), цианокобаламин - до 1 мг, пиридоксин (в/м - 3 мл 5% раствора).
Способ применения и дозы
Наружно, в водных растворах для промывания ран (0.1-0.5%), для полоскания рта и горла (0.01-0.1%), для смазывания язвенных и ожоговых поверхностей (2-5%), для спринцевания (0.02-0.1%) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Взаимодействие
Химически несовместим с некоторыми органическими веществами (уголь, сахар, танин) и легкоокисляющимися веществами может произойти взрыв.
Другие сферы применения
- Щелочной раствор перманганата калия хорошо отмывает лабораторную посуду от жиров и других органических веществ.
- Растворы (концентрации примерно 3 г/л) широко применяются при тонировании фотографий.
- В пиротехнике применяют в качестве сильного окислителя.
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
2MnO2 +3 Cl2 + 8KOH → 2KMnO4 + 6KCl + 4H2O
2K2MnO4 + Cl2 → 2KMnO4 + 2KCl
3K2MnO4+2H2O → 2KMnO4+ MnO2 + 4KOH
2K2MnO4 + 2H2O → 2KMnO4 +H2↑ + 2KOH
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Литература
- Вульфсон Н.С. — Препаративная органическая химия с.656,657
- Казанский Б.А. (ред.) — Синтезы органических препаратов (Сборник 3) с.145
- Реми Г. — Курс неорганической химии (Том 1) с.817
См. также
Wikimedia Foundation. 2010.
Марганцовка как по другому называется | Советы врачей
Почему запретили марганцовку и как ее теперь можно приобрести
Лечебные свойства марганцовки
- слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
- более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
- в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
- марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
- хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
- ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Как применяют марганцовку в быту
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
2. Кроме того, перманганат калия относится к средствам, которые называются перекурсоры . Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Как относятся люди к такому запрету
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Похожие статьи
Ведь это и есть основное оружие страшных бородатых теорроров.
Раньше можно было, а сейчас нельзя. До маразма дошли!
http://www.syl.ru/article/189246/undefined
Почему запретили марганцовку и как ее теперь можно приобрести
Лечебные свойства марганцовки
- слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
- более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
- в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
- марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
- хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
- ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Как применяют марганцовку в быту
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
2. Кроме того, перманганат калия относится к средствам, которые называются перекурсоры . Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Как относятся люди к такому запрету
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Похожие статьи
Ведь это и есть основное оружие страшных бородатых теорроров.
Раньше можно было, а сейчас нельзя. До маразма дошли!
http://www.syl.ru/article/189246/undefined
Как правильно называется марганцовка в аптеке
Почему запретили марганцовку и как ее теперь можно приобрести
Лечебные свойства марганцовки
- слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
- более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
- в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
- марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
- хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
- ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Как применяют марганцовку в быту
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
2. Кроме того, перманганат калия относится к средствам, которые называются перекурсоры . Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Как относятся люди к такому запрету
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Добавить комментарий
Почему запрещена марганцовка к продаже: причины запрета. С чего все началось?
Краткое содержание статьи:
Зачем нужна марганцовка?
С химической точки зрения марганцовка представляет собой перманганат калия :
На протяжении длительного времени перманганат калия был дешевым безрецептурным средством . достаточно было сходить в аптеку и купить ровно столько, сколько нужно.
Как правило, марганцовку хранили где-то в кладовке, на дальней полке. Хозяйки не особо ее любили из-за способности окрашивать все остальное, да и направлений применения было не так уж много. Что уж говорить о риске отравления .
Где купить марганцовку в аптеке?
На сегодняшний день в большинстве аптек вам скажут, что марганцовка запрещена к продаже и нигде на прилавках вы ее не найдете. На самом деле это не совсем так, она просто внесена в список рецептурных препаратов .
Поэтому для покупки марганцовки в аптеке:
- Обзаведитесь рецептом от врача.
- Проконсультируйтесь у него, где именно в вашем городе можно купить марганцовку.
- Найдите в сети список аптек с номерами телефонов.
- Перед выходом прозвоните и поинтересуйтесь, если ли в наличии марганцовка.
Схема не самая сложная, но требует слишком много усилий для такой простой покупки. Поэтому проще проверить свои запасы или поспрашивать у родни и знакомых. В крайнем случае, всегда можно заменить перманганат калия какой-то альтернативой.
Чем можно заменить марганцовку?
Как правило, марганцовку используют как самый простой антисептик. С его помощью обрабатывают загрязненные раны, места ожогов. В этом плане его можно заменить:
Перед тем как купать малыша, воду можно обработать при помощи отвара ромашки. шалфей и череда тоже подойдут для этих нужд. Все тот же антисептический эффект, но при этом на 100% природный.
Для полоскания горла лучше использовать фурацилин. желтые таблетки можно купить в любой аптеке, и опять без рецепта. У агрономов все чуть сложнее, вместо привычных кристаллов можно использовать настойку борной кислоты или календулы.
Для обработки почвы понадобятся уже более специфические средства, подойдет тот же Фитоспорин .
Почему не продают марганцовку?
В связи с этим вопросом есть три теории, почему власти могли наложить запрет на продажу перманганата калия:
1-как.ru - портал ответов на интернет-вопросы
Почему запретили марганцовку
Причины дефицита
Однако на самом деле это не так. Дело в том, что выпуск марганцовки просто сократили в значительной степени, а продаваться в аптеках она стала исключительно по рецепту. Именно поэтому купить ее на данный момент очень сложно. Большинство населения таким решением не довольно. С давних времен кристаллы перманганата калия разбавляли в воде и использовали для лекарственных целей.
Некоторые аптеки отказались от реализации марганцовки по собственному желанию. Объясняется это решение очень просто. В соответствии с некоторыми изменениями, в значительной степени ужесточились требования хранения этого препарата.
Особые свойства марганцовки
Стоит отметить, что взрывные химические реакции могут возникнуть при естественных условиях, например, если не соблюдать условия хранения препарата. Самонагревание гранул может произойти даже при комнатной температуре.
Вторым поводом для ограничения выпуска считается занесение марганцовки в список «прекурсосов». Такие вещества используются для изготовления наркотических веществ в домашних условиях. Самый известный наркотик такого типа - «Винт».
Источники: http://www.syl.ru/article/189246/new_pochemu-zapretili-margantsovku-i-kak-ee-teper-mojno-priobresti, http://1-kak.ru/51-pochemu-zapreshchena-margancovka-k-prodazhe.html, http://www.kakprosto.ru/kak-834546-pochemu-zapretili-margancovku
Комментариев пока нет!
Избранные статьи
Правильно обрезать грушу видео
Обрезка дерева молодой далее.
Как правильно рассчитать рабочее время в графике
ВОПРОС: Как правильно рассчитать переработку в далее.
Как правильно ставить диски сцепления мазе
Сборка и регулировка сцепления Сборку далее.
Как правильно оформить брошюру
7 советов по правильному оформлению буклетов Чтобы далее.
Правильно сажать грушу весной видео
Груша -посадка и уход. Сорта груши Груша посадка и уход, далее.
Как правильно рассчитать бжу
БЖУ для похудения Любой диетолог просчитывает диету далее.
Как правильно делать разворот на перекрестке
Как развернуться на перекрестке. Для многих начинающих автомобилистов разворот на далее.
Популярные статьи
Как правильно написать автобиографию военкомат
Как написать автобиографию в военкомат – образец написания? Новости по тематике Автобиография в военкомат (образец)– это тема, которая ставит в тупик большое число призывников.
Как правильно поставить нумерацию страниц в ворде
Сложно себе представить какую-либо книгу без нумерации страниц. Это сильно бы затрудняло использование книг, так как даже оглавление не.
http://pravilnyj-otvet.ru/kak-pravilno-nazyvaetsja/kak-pravilno-nazyvaetsja-margancovka-v-apteke.html
Комментариев пока нет!
Куда исчезла марганцовка и где ее можно приобрести
Возможно, у кого-то еще сохранился стеклянный пузырек с кристаллами темного цвета, еще недавно считавшийся незаменимым средством при отравлении или обеззараживании. Водный раствор антисептика, бледно-розового цвета, широко применялся в бытовых условиях и в медицинских учреждениях.
 Фото: https://mtdata.ru/u16/photoAC59/20588114161-0/original.jpg
Фото: https://mtdata.ru/u16/photoAC59/20588114161-0/original.jpgОднако, доступная по цене и безотказная в использовании, марганцовка неожиданно исчезла с прилавков аптек. Попробуем разобраться почему, привычное всем с детства, средство перешло в разряд запрещенных к свободной продаже препаратов.
Лекарственное назначение марганцовки
Перманганат калия — научное обозначение средства, обладающего окисляющими свойствами и уничтожающего большое количество опасных микробов. Раствор служит как для наружного применения, так и для приема внутрь.
Как и где наиболее эффективно используется препарат:
- слабый раствор помогает справится с неприятной ситуацией при отравлениях, кишечных расстройствах и инфекциях;
- насыщенный раствор, до 0,5%, используется при обработке открытых ран, пролежней и язв;
- распространено применение раствора марганцовки во время купания младенцев, что способствует быстрому заживлению пупочной ранки и не имеет противопоказаний;
- борется с вредными бактериями при стоматите и гингивите. Приготовленным раствором полощут рот, также хорошо помогает при полосканиях больного горла;
- подсушивает различные высыпания на коже, например, при ветряной оспе;
- ванночки для ног с марганцовкой заживляют трещины и мозоли, дополнительно избавляя от излишней потливости.
Бытовое применение перманганата калия
Марганцовка в быту служила, в первую очередь, обеззараживающим средством для воды. Ее обязательно брали с собой в походы, а также обрабатывали колодцы. Особенно удобно использование препарата при плохом качестве воды или невозможности ее прокипятить.
Нашел свою нишу пераманганат калия и в садоводстве — для избавления от вредителей почву и приготовленные семена обрабатывают разбавленным, до едва заметного розового цвета, раствором. Действие стимулирует быстрый и здоровый рост до 100% посадок.
Часто раствор используют для устранения резких, въевшихся запахов.
Основные минусы перманганата калия
Одна из главных опасностей заключена в попадании не растворившегося полностью кристалла на слизистую человека. В результате может образоваться рана, вызванная достаточно глубоким и болезненным ожогом. При приготовлении раствора необходимо разводить марганцовку в отдельной посуде и потом просто вливать его в воду, добиваясь нужной концентрации.
Этот совет особенно важен, если раствор готовится для употребления внутрь или для наполнения детских ванночек. И, конечно, стоит неукоснительно соблюдать правила хранения кристаллов перманганата калия. При минимальном трении кристаллов о железо может возникнуть воспламенение или даже взрыв.
Почему исчезла из продажи марганцовка?
В РФ официальный запрет на продажу и использование перманганата калия был введен в 2007 году. Причиной стали опасные свойства антисептика, несущие угрозу здоровью человека.
- Нестабильность солей калия относит средство в разряд взрывоопасных и легковоспламеняющихся веществ. Данное свойство марганцовки используется для незаконного изготовления самодельных взрывных устройств. В аптеках всегда была запрещена продажа препарата в больших количествах. Нет гарантии защиты от случайного возгорания, которое возможно при нарушении правил хранения независимо от температуры воздуха.
- Не менее серьезную опасность несет в себе отношение перманганата калия к «перекурсорам» — составляющим наркотических средств. В некоторых странах марганцовку приравняли к наркотикам и за хранение препарата налагается крупный штраф.
Можно ли купить антисептик в аптеке
Вопреки слухам приобрести средство в аптеках все-таки можно, но в строго ограниченном количестве. Также выдается перманганат калия по рецепту врача, но не более 1-2 пакетиков в руки. Аптеки и склады с медикаментами обязаны учитывать каждую единицу препарата, с этим связаны многочисленные отказы владельцев бизнеса от продажи не прибыльного средства, вызывающего столько хлопот.
Найти марганцовку можно только в редких государственных аптеках, специально обустроенных с учетом возможности хранения опасных препаратов с угрозой взрыва.
Отношение людей к запрету
Во многих домах в прошлом имелись стандартные аптечки, в которых перманганат калия был обязательным компонентом. Благодаря мизерному расходу и неограниченному сроку хранения, старые запасы благополучно перекочевали в наши дни. Но что же делать, если кто-то решил купить антисептик «посвежее» и наткнулся на запрет.
Людям совершенно непонятны причины для принятия такого кардинального решения, ведь большая часть населения выросла в условиях, не определяющих соответствие препарата настолько неоправданно высокому уровню опасности.
Совершено справедливо замечание о свободной продаже средств, с наибольшей долей вероятности используемых в качестве полноценных наркотических веществ. Каждый желающий может свободно купить, к примеру, сильнодействующее средство против засоров труб «Крот» или, допустим, ацетон.
Следуя этой логике, необходимо запретить продажу дистиллированной воды, кофе, сахара, которые также используются в изготовлении наркотиков. Запасы марганцовки во многих домах пока еще не придали массовости возмущениям покупателей.
Причины отсутствия, простого и действенного, антисептика в продаже толком не смогли объяснить ни в одной аптеке. Если же отправной точкой запрета стали взрывоопасные качества препарата и их незаконное использование, то люди также понимают, что подобные ограничения, в данном случае, бессильны.
 Фото: https://spirtnoe.expert/wp-content/uploads/2018/06/Ochistka-samogona-i-bragi-margantsovkoj.jpg
Фото: https://spirtnoe.expert/wp-content/uploads/2018/06/Ochistka-samogona-i-bragi-margantsovkoj.jpgНеобходимое количество марганцовки, для таких целей, можно купить в разных аптечных пунктах или прибегнуть хитростью к помощи посторонних людей. Единственными пострадавшим стали покупатели, не нашедшие в продаже нужного и действенного антисептика. Многие качества привычной марганцовки не имеют аналогов даже среди самых современных обеззараживающих и антибактериальных средств.
The following two tabs change content below.Вся информация на сайте создана специально для того, что бы вы были в курсе последних самых актуальных новостей. А так же что бы вам было легче заниматься индивидуальным строительством или же простым ремонтом своей квартиры.
ЦЕЛЕБНЫЕ СВОЙСТВА МАРГАНЦОВКИ — ПОЛЕЗНЫЕ СОВЕТЫ - Советы Народной Мудрости
ЛЕЧЕНИЕ МАРГАНЦОВКОЙ — полезные советы
В годы Великой Отечественной войны, как патроны у солдата, она находилась в сумках санитаров, фельдшеров и широко использовалась при лечении ран в госпиталях.
Первое, к чему прибегают при заболеваниях горла, расстройствах кишечника, отравлениях — это марганцовка (перманганат калия, марганцовокислый калий).
В годы Великой Отечественной войны, как патроны у солдата, она находилась в сумках санитаров, фельдшеров и широко использовалась при лечении ран в госпиталях.
В основе действия перманганата калия — его способность окислять органические вещества, выделяя при этом кислород. Этим обусловлено антимикробное и антисептическое действие марганцовки.
Водный раствор перманганата калия обладает противовоспалительными свойствами. В различных концентрациях этот раствор применяют для промывания ран, полоскания рта и горла, для смазывания язвенных и ожоговых поверхностей, спринцеваний. Диапазон применения перманганата калия достаточно широк. Даже при наличии многих новых синтетических средств он и сейчас незаменим «в» гинекологической, урологической, дерматологической практике.
В таблице противоядий при отравлениях перманганат калия является одним из важнейших средств оказания первой помощи.
Однако при всех достоинствах марганцовокислого калия обращаться с ним надо осторожно. В больших концентрациях он прижигает и вызывает отек слизистых оболочек рта, глотки, пищевода, желудка, кишок, рвоту и понос. Поэтому применять раствор следует с осторожностью.
Еще наши бабушки знали полезные в быту свойства марганцовки: ей промывали раны, лечили отравление, обеззараживали, купали младенцев и даже использовали в борьбе с вредителями в огороде. Такое широкое применение марганцовки объясняет главное ее свойство – это противогрибковый, противомикробный препарат. За счет активных процессов окисления марганцовка убивает вредные микробы – возбудителей различных инфекций как на поверхности кожи, так и внутри организма.
Целебные свойства марганцовки (перманганата калия)
Марганцовка — эффективное дезинфицирующее средство. Раствор перманганата калия (марганцовки) обладает антисептическими свойствами, способен нейтрализовать токсическое действие на организм таких отравляющих соединений, как аконитин, морфин, другие алкалоиды, фосфор (при приеме их внутрь).
Перманганат калия — один из видов перманганатов (от лат. manganum — «марганец») — марганцовокислых солей. Это химическое вещество широко используют как для домашних нужд, так и для медицины. Перманганат калия — кристаллы темно-фиолетового цвета, хорошо растворимые в воде (в зависимости от концентрации цвет может быть от светло-розового до красно-фиолетового), метиловом спирте, уксусной кислоте и ацетоне. В быту марганцовокислый калий, растворенный в воде, называют марганцовкой.
Лечение марганцовкой в медицине
Нейтрализация синильной кислоты (ядовитого вещества) марганцовкой происходит лишь в щелочной среде. Калия перманганат — сильный окислитель. Водный раствор марганцовки оказывает сильное дезинфицирующее и подсушивающее действие, его широко используют в дерматологической и хирургической практике.
При появлении первых признаков гастрита и гастроэнтероколита в первую очередь надо промыть желудок, используя для этого слабый (слегка розовый) раствор марганцовки. Для промывания желудка у взрослых и даже детей зондом пользоваться необязательно, достаточно просто дать выпить больному приготовленный раствор в количестве 0,5 — 2 л, после чего рефлекторно вызвать рвоту.
При отравлениях, когда нужно как можно быстрее вызвать рвоту, пострадавшему дают выпить розовый раствор марганцовки, который является также лекарственным, дезинфицирующим желудочно-кишечный тракт средством.
Раствор зачастую готовят «на глаз», но основные рекомендации — это 10 кристаллов на 1 литр воды, дальнейшую крепость раствора можно корректировать по его цвету. Очень важно, чтобы перед применением все кристаллы растворились в воде, иначе в процессе соприкосновения с кожей или внутренними органами нерастворенные кристаллы могут вызвать ожог.
Наиболее популярен раствор марганцовки при отравлении. При первых признаках, в том числе при диарее больному предлагают раствор марганцовки, который стимулирует очищение кишечника.
Марганцовка для применения внутрь при отравлении готовится в соотношении 2 кристалла на чашку воды, такой раствор выпивается. Благодаря своим антисептическим свойствам подобное лекарство останавливает очаг инфекции в желудке.
Марганцовка – применение в урологии, гинекологии
За счет своих антисептических, противомикробных способностей раствор марганцовки применяют при лечении грибковых, бактериальных заболевания в урологии и гинекологии. Марганцовка имеет применение при молочнице, когда слабый раствор назначают для ежедневных спринцеваний. При урологических проблемах у мужчин, связанных с наружными воспалительными процессами, назначают промывания раствором марганцовки.
При применении в урологии и гинекологии важно соблюдать правила приготовления раствора, следить за тем, чтобы кристаллы марганцовки полностью растворились. В противном случае при попадании на слизистую кристаллы могут вызвать еще большее раздражение.
Марганцовка — противопоказания
Не рекомендуется применять раствор марганцовки при индивидуальной непереносимости. Это сразу можно понять по наличию побочных эффектов – отек, изменение цвета слизистых, резкая боль при применении внутрь, судороги и др. При наличии подобных или других неприятных симптомов прием марганцовки следует прекратить.
Марганцовка за счет своих окислительных свойств абсолютно несовместима с применением угля, сахара и другими веществами, которые легко окисляются. Важно хранить кристаллы перманганата калия вдали от легкоокисляющихся веществ, иначе их соприкосновение может привести к взрыву и даже пожару.
Лечение марганцовкой (перманганатом калия) в народной медицине
Лечение марганцовкой в народной медицине для устранения болей, вызванных мозолями. Для этого в раствор марганцовки розового цвета добавляют поваренную соль и, налив раствор в тазик, опускают в него ноги на 20 мин, после процедуры ноги не нужно вытирать. Через некоторое время боль в области мозолей пройдет. Ни в коем случае для лечения марганцовкой нельзя пользоваться сильно концентрированным раствором (фиолетового цвета), так как это может повлечь за собой вред здоровью, получение ожогов кожи и слизистых, отравление.
Хороший лечебный эффект при опрелостях, в том числе и у грудных детей, оказывают гигиенические ванны с марганцовкой: вода должна быть розового цвета и теплой.
При повышенной потливости нижних конечностей, неприятных запахах, гнойных мозолях поможет теплая ножная ванна с солью и марганцовкой, после процедур ноги следует хорошо вытереть и посыпать тальком.
Лечение перманганатом калия активно используется для промывания открытых ран, в том числе и гноящихся. При дерматитах, характеризующихся появлением пузырей, кожу следует обмыть розовым раствором перманганата калия.
Если при постановке банок их слишком долго держать, на коже могут образоваться багровые пятна и даже пузырьки, наполненные сукровичной жидкостью. В подобных случаях пораженные места полезно смазать 5 — 10%-ным раствором марганцовокислого калия.
Лечение перманганатом калия на практике: лучшие рецепты
В запущенных случаях геморроя можно приготовить целебный раствор.
Требуется:
1 ч. л. пищевой соды,
1 ст. л. любого растительного масла,
марганцовка,
3 л воды.
Приготовление
В горячую воду всыпать столько марганцовки, чтобы получить розовый цвет, добавить соду, масло, раствор влить в ванну.
Применение. Принимать ванну в течение 20 мин на ночь. Процедуру проводить ежедневно в течение недели.
В народной медицине есть рецепт для лечения марганцовкой от дизентерии.
В состав этого средства входят несколько кристаллов марганцовки на 0,5 л воды. Советуют увеличивать концентрацию раствора в зависимости от возраста (грудничкам — бледно-розовый, а взрослым людям — малиновый раствор).
Рекомендуется принимать такой раствор внутрь, совмещая это с процедурой постановки клизмы.
Надо иметь в виду, что перманганат калия при взаимодействии с различными органическими веществами становится взрывоопасным. Поэтому его кристаллы надо хранить в чистой стеклянной посуде с притертыми пробками, а раствор — в склянках из темного стекла, так как под действием солнечных лучей и дневного света он легко разлагается.
При пользовании раствором часто остаются трудно смываемые пятна на коже и белье. Чтобы устранить их, кожу можно обмыть раствором сернистого аммония в концентрации 1:5, а затем горячей водой. С белья пятна выводят раствором щавелевой кислоты (1:9), 2-процентным раствором соляной кислоты, уксусом или лимонным соком..
Источник
Значение слова МАРГАНЦОВКА. Что такое МАРГАНЦОВКА?
-
МАРГАНЦО́ВКА, -и, ж. Разг. Марганцовокислый калий, а также его раствор. Полоскать горло марганцовкой.
Источник (печатная версия): Словарь русского языка: В 4-х т. / РАН, Ин-т лингвистич. исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.; Полиграфресурсы, 1999; (электронная версия): Фундаментальная электронная библиотека
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать Карту слов. Я отлично умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я обязательно научусь отличать широко распространённые слова от узкоспециальных.
Насколько понятно значение слова молотобоец (существительное):
Кристально
понятно
Понятно
в общих чертах
Могу только
догадываться
Понятия не имею,
что это
Другое
Пропустить