Миелоидный лейкоз что это такое
Острый миелоидный лейкоз — Википедия
Острый миелоидный лейкоз (также ОМЛ, острый нелимфобластный лейкоз, острый миелогенный лейкоз) — это злокачественная опухоль миелоидного ростка крови, при которой быстро размножаются изменённые белые кровяные клетки. Накапливаясь в костном мозге, они подавляют рост нормальных клеток крови, что приводит к снижению количества эритроцитов, тромбоцитов, и нормальных лейкоцитов. Болезнь проявляется быстрой утомляемостью, одышкой, частыми мелкими повреждениями кожи, повышенной кровоточивостью, частыми инфекционными поражениями. До сих пор явная причина заболевания неизвестна, однако некоторые факторы риска его возникновения выявлены. ОМЛ является острым заболеванием, развивается быстро и без лечения приводит к смерти больного за несколько месяцев, иногда — недель.
Это самый распространённый вид острого лейкоза у взрослых, заболеваемость им с возрастом увеличивается. Хотя острый миелоидный лейкоз заболевание относительно редкое — на его долю приходится лишь 1,2 % смертельных случаев злокачественных опухолей в США[3], — ожидается его учащение вместе с постарением населения.
Встречаются несколько разновидностей ОМЛ, лечение и прогноз для них оказывается разным. Уровень выживаемости на протяжении пяти лет колеблется между 15 и 70 %, а частота ремиссии — от 78 до 33 % в зависимости от подвида заболевания. В начале ОМЛ лечат химиопрепаратами для того, чтобы добиться ремиссии; затем может проводиться поддерживающее химиолечение, или проводится пересадка кроветворных стволовых клеток. Последние исследования на генетическом уровне позволили разработать тесты, с помощью которых можно довольно точно определить вероятность выживания больного и эффективность того или иного лекарства для индивидуального случая ОМЛ.[источник не указан 825 дней]
Самые часто используемые схемы классификации ОМЛ — это давняя франко-американо-британская (ФАБ) система и более современная система Всемирной организации здравоохранения (ВОЗ).
Классификация острого миелоидного лейкоза по системе Всемирной системы здравоохранения[править | править код]
Система классификации острого миелоидного лейкоза ВОЗ разработана с учётом системы ФАБ и имеет целью более эффективное клиническое применение и учитывает наиболее прогностически значимые признаки заболевания. Каждый из видов (категорий) ОМЛ по классификации ВОЗ включает в себя несколько подвидов (подкатегорий) описательного характера, представляющих интерес для гематологов и онкологов; однако, бо́льшая часть клинически важной информации в классификации ВОЗ взаимосвязана через распределение по перечисленным ниже подвидам.
Подвиды острого миелоидного лейкоза по классификации ВОЗ:[4]
| Название подвида | Описание | МКБ-О |
|---|---|---|
| ОМЛ с характерными генетическими изменениями | Включает: | Несколько |
| ОМЛ с изменениями, связанными с миелодисплазией | Этот подвид включает больных с предшествующим миелодиспластическим синдромом (МДС) или миелопролиферативной болезнью (МПБ) или с характерными для него цитогенетическими изменениями. Этот подвид ОМЛ чаще встречается у пожилых людей и отличается неблагоприятным прогнозом. Включает в себя ОМЛ со следующими изменениями:
| M9895/3 |
| ОМЛ и МДС, связанные с предыдущим лечением | Этот подвид ОМЛ включает больных, получавших химиотерапию и/или лучевое лечение, после которых возник ОМЛ или МДС. При этих лейкозах могут быть характерные изменения в хромосомах, прогноз при них часто бывает хуже. | M9920/3 |
| Миелоидная саркома | Этот подвид включает больных с миелоидной саркомой | |
| Миелопролиферативные заболевания, связанные с Синдромом Дауна | Этот подвид включает больных как с кратковременными (преходящими) миелопролиферативными состояниями на фоне синдрома Дауна, так и с ОМЛ на фоне синдрома Дауна | |
| Бластная плазмацитоидная дендритноклеточная опухоль | Этот подвид включает больных с бластными дендритноклеточными опухолями | |
| ОМЛ, не подпадающие под признаки перечисленных подвидов | Включает подвиды ОМЛ, не входящие в перечисленные выше, в том числе: | M9861/3 |
Бывают такие подвиды острого лейкоза, при которых изменённые лейкоциты невозможно определить как лимфоциты или гранулоциты, или когда присутствуют злокачественно изменённые клетки обоих ростков. Такие лейкозы иногда называют бифенотипными острыми лейкозами.
Франко-американско-британская классификация[править | править код]
Франко-американско-британская классификационная (ФАБ) система разделяет ОМЛ на 9 подвидов, от М0 по M8, основываясь на типах клеток — предшественниц лейкоцитов, и на степени зрелости изменённых клеток. Определение злокачественных клеток проводят на основании внешних признаков при световой микроскопии и/или цитогенетически, выявляя лежащие в основе отклонений изменения в хромосомах. У разных подвидов ОМЛ разные прогноз и ответ на лечение. Несмотря на преимущества классификации ВОЗ, система ФАБ до сих пор широко применяется. По ФАБ существует девять подтипов ОМЛ.
Необычные фенотипы острого миелоидного лейкоза[править | править код]
Морфологические подтипы ОМЛ включают многие исключительно редкие подтипы не включённые в классификацию ФАБ. Все они, за исключением острого миелоидного дендритноклеточного лейкоза включены в классификацию ВОЗ. В списке ниже перечислены эти подтипы.
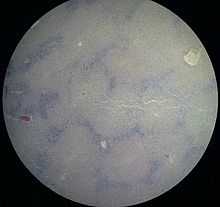 Инфильтрированная лейкоцитами печень при миелолейкозе
Инфильтрированная лейкоцитами печень при миелолейкозе Бо́льшая часть симптомов ОМЛ вызывается замещением нормальных клеток крови лейкозными клетками. Недостаточное образование лейкоцитов обусловливает высокую восприимчивость больного к инфекциям — несмотря на то, что лейкемические клетки происходят от предшественников лейкоцитов, способность противостоять инфектам у них отсутствует. [5] Снижение количества красных кровяных телец (анемия) может вызывать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой повреждаемости кожи и повышенной кровоточивости.
Ранние признаки ОМЛ часто неопределённы и неспецифичны, и могут походить на признаки гриппа или других распространённых болезней. Вот некоторые общие симптомы ОМЛ: лихорадка, усталость, потеря веса или снижение аппетита, одышка, анемия, повышенная повреждаемость кожи и слизистых оболочек и кровоточивость, петехии (плоские, размером с булавочную головку пятнышки внутри кожи на месте кровоизлияний), гематомы, боль в костях и суставах, и стойкие или частые инфекции.[5]
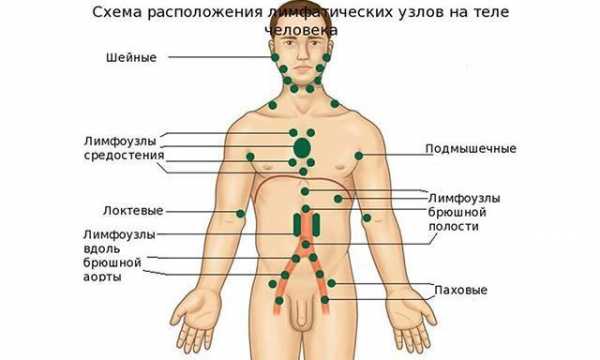
При ОМЛ может быть увеличение селезёнки но обычно оно незначительно и бессимптомно. Увеличение лимфоузлов при ОМЛ случается нечасто, в отличие от острого лимфобластного лейкоза. В 10 % случаев развиваются изменения кожи в виде кожного лейкоза. Изредка при ОМЛ возникает Синдром Свита, он же паранеопластический синдром — воспаление кожи вокруг поражённых хлоромой участков.[5]
У некоторых больных ОМЛ появляется припухлость дёсен из-за инфильтрации тканей лейкозными клетками. Изредка первым признаком лейкоза оказывается хлорома — плотная лейкемическая масса за пределами костного мозга. Иногда заболевание протекает бессимптомно, и лейкоз выявляется общим анализом крови в ходе профилактического осмотра.[6]
Был выявлен ряд факторов, способствующих возникновению ОМЛ — иные расстройства системы кроветворения, воздействие вредных веществ, ионизирующее излучение, и генетическое влияние.
Пре-лейкоз[править | править код]
"Пре-лейкозные нарушения кроветворения, такие, как миелодиспластический синдром или миелопролиферативный синдром могут привести к ОМЛ; вероятность заболевания зависит от формы миелодиспластического или миелопролиферативного синдрома.[7]
Воздействие химических веществ[править | править код]
Противоопухолевое химиотерапевтическое воздействие, особенно алкилирующими веществами, может увеличивать вероятность возникновения ОМЛ в последующем. Наивысшая вероятность заболевания приходится на 3—5 лет после химиотерапии.[8] Другие химиотерапевтические препараты особенно эпиподофилотоксины и антрациклины, также связываются с постхимиотерапевтическими лейкозами. лейкозы такого вида часто объясняют специфическими изменениями в хромосомах лейкозных клеток.[9]
Воздействие бензола и других ароматических органических растворителей, связанное с профессиональной деятельностью, в качестве возможной причины ОМЛ остаётся спорным. Бензол и многие его производные проявляют канцерогенные свойства in vitro. Данные некоторых наблюдений подтверждают возможность влияния профессиональных контактов с этими веществами на вероятность развития ОМЛ, однако другие исследования подтверждают, что если и существует такая опасность, то она является лишь добавочным фактором.[10][11]
Ионизирующее излучение[править | править код]
Воздействие ионизирующего излучения повышает вероятность заболеваня ОМЛ. У переживших атомную бомбардировку Хиросимы и Нагасаки заболеваемость ОМЛ повышена,[12] так же как у рентгенологов, получивших высокие дозы рентгеновского излучения в то время, когда меры радиологической защиты были недостаточными.[13]
Генетические факторы[править | править код]
Вероятно, существует наследственно повышенная вероятность заболевания ОМЛ. Есть большое количество сообщений о множестве семейных случаев ОМЛ, когда заболеваемость превышала среднестатистическую.[14][15][16][17] Вероятность возникновения ОМЛ у ближайших родственников больного втрое выше.[18]
Ряд врождённых состояний может повышать вероятность ОМЛ. Чаще всего это синдром Дауна, при котором вероятность ОМЛ повышена в 10 — 18 раз.[19]
Изменения соотношения клеточных элементов в общем анализе крови — первое, что наводит на мысль о возможности ОМЛ. Наиболее частым оказывается лейкоцитоз- повышение общего количества лейкоцитов, иногда с появлением бластных (незрелых) форм, но бывает так, что ОМЛ проявляется изолированным снижением тромбоцитов, эритроцитов, а количество лейкоцитов может оказаться даже сниженным (лейкопения).[20] Предварительный диагноз ОМЛ может быть определён в случае выявления в мазках периферической крови бластных форм лейкоцитов, но для окончательного диагноза должны быть выявлены соответствующие изменения в анализе аспирационного биоптата костного мозга.
Костный мозг и кровь исследуют световым микроскопированием и поточной цитометрией для установления диагноза и дифференцирования ОМЛ от других лейкозов, например, от острого лимфобластного лейкоза, а также для уточнения подтипа ОМЛ. Образец крови или костного мозга обычно проверяют на присутствие хромосомных транслокаций обычными цитогененитческими способами, или способом флуоресцентной гибридизации in situ. Генетические исследования проводят и для выявления характерных мутаций, которые могут влиять на исход заболевания — например, в FLT3, в нуклеоплазмине, или в KIT.[21]
Цитохимические красители для мазков крови и костного мозга оказываются очень полезными для дифференциальной диагностики ОМЛ и ОЛЛ, а также для выделения подтипов ОМЛ. Сочетание миелопероксидазы или красителя Суданский чёрный и неспцифического эстеразного красителя обеспечивает получение нужной информации в большинстве случаев. Реакции миелопероксидазы или Суданского чёрного оказываются самыми полезными для установления диагноза ОМЛ и его дифференцирования от ОЛЛ. Неспецифический краситель эстеразы используется для моноцитаронй составляющей острых миелолейкозов и для дифференцирования от незрелой формы монобластного лейкоза от ОЛЛ.[4]
Диагноз и классификация ОМЛ может оказаться непростой задачей, этим должен должен заниматься квалифицированный гематопатолог или гематолог. В явных случаях наличие некоторых характерный морфологических признаков, таких, как тельца Ауэра, или специфическия для АМЛ результаты поточной цитометрии дают возможность надёжно отделять ОМЛ от других лейкозов; однако при отсутствии такх явных признаков диагностика существенно осложняется.[22]
В соответствии с широко используемыми критериями классификации ВОЗ диагноз ОМЛ устанавливаетсяв том случае, если доказано если в крови и/или костном мозге более 20 % клеток представлены миелобластами.[23] ОМЛ следует тщательно дифференцировать от так называемых прелейкозных состояний, в частности, от миелодиспластического синдрома или миелопролиферативного синдрома, которые лечатся по-разному.
Поскольку острый промиелоцитарный лейкоз (ОПЛ), требуя уникального способа лечения очень хорошо ему поддаётся, очень важно быстро подтвердить или отвергнуть этот подвид лейкоза. Для этого часто используют флюоресцентную гибридизацию in situ, выполненную на крови или костном мозге, поскольку ею легко выявляется хромосомная транслокация (t[15;17]) специфичная для ОПЛ.[24]
Злокачественными клетками при ОМЛ выступают миелобласты. В нормальном гемопоэзе миелобласты являются незрелыми предшественниками лейкоцитов миелоидного ряда;нормальные миелобласты постепенно созревают, превращаясь в нормальные лейкоциты. Однако при ОМЛ в каком — то из миелобластов накапливаются генетические изменения, которые «замораживают» клетку в незрелом состоянии, останавливая процесс клеточной дифференциации. [25] Сама по себе такая мутация не вызывает лейкоз, но когда «остановка дифференциации» сочетается с другими мутациями, которые приводят к утрате генетического контроля над ростом клеток, результатом оказывается неуправляемое размножение незрелого клеточного клона, определяющего клиническую сущность ОМЛ.[26]
Большое разнообразие и генетическая неоднородность ОМЛ происходит от того, что лейкозная трансформация может возникнуть на множестве этапов дифференциации клетки.[27] Современные схемы классификации ОМЛ признают факт зависимости свойств и поведения лейкозных клеток, а также течения лейкоза от того, на каком этапе остановилась дифференциация.
Специфические цитогенетическиеотклонения обнаруживаются у многих больных ОМЛ. Виды изменений хромосом часто прогностически значимы.[28] Хромосомные транслокации кодируют синтез гибридных белков, чаще всего, факторов транскрипции — вспомогательных белков — помощников РНК-полимераз, изменённые свойства которых могут привести к останову дифференциации.[29] Например, при остром промиелоцитарном лейкозе транслокация t(15; 17) вызывает синтез гибридного протеина PML-RARα, который связывается с рецептором ретиноевой кислоты в промоторах некоторых специфических для миелоидных клеток генов и останавливает в этих клетках дифференциацию.[30]
Схема транслокации хромосом.Клинические проявления и симптомы ОМЛ возникают потому что, умножаясь, клетки лейкозного клона мешают деятельности нормальных клеток и стремятся вытеснить их из костного мозга.[31] Это приводит к нейтропении, анемии, и тромбоцитопении. Чаще всего симптомы ОМЛ определяются недостаточностью нормальных клеток крови. В редких случаях у больных развиваются хлоромы — плотные опухоли из лейкозных клеток за прелами костного мозга, которые могут вызывать различные симптомы в зависимости от локализации хлоромы.[5]
Лечение ОМЛ состоит в основном из химиотерапии, и делится на два этапа: индукция и постремиссионное лечение(или консолидация). Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до не обнаруживаемого уровня; цель консолидирующей терапии заключается в ликвидации остаточных, не обнаруживаемых современными методами остатками болезни и излечение.[32]
Индукция[править | править код]
Для всех подтипов ОМЛ за исключением M3 по классификации ФАБ, обычно используют индукционную химиотерапию цитарабином и антрациклиновым антибиотиком (например, даунорубицином или идарубицином).[33] Этот способ индукционной химиотерапии известен под названием «7+3». Название происходит от того, что в этом режиме предусматриваются 7 дней непрерывного инфузионного вливания цитарабина, при этом в первые три дня одновременно болюсно вводится антрациклиновый антибиотик. При таком способе лечения ремиссия наступает почти у 70 % больных ОМЛ.[34] Могут применяться и другие способы индукционного лечения, включая режимы FLAG, DAT, ADE и подобные, или монотерапию высокими дозами цитарабина, или лечение препаратами, находящимися на стадии исследования.[35][36] Вследствие токсического воздействия лечения, в том числе подавления миелоидного ростка и повышения вероятности инфекционных осложнений очень старым больным индукционная химиотерапия не предлагается, и назначается менее интенсивное паллиативное лечение химиопрепаратами. Подвид ОМЛ M3, также известный под названием острый промиелоцитарный лейкоз, почти во всех случаях лечится препаратом ПТРК (полностью транс- ретиноевая кислота) в дополнение к индукционной терапии.[37][38][39] При лечении острого промиелоцитарного лейкоза нужно учитывать возможность развития синдрома диссеминированного внутрисосудистого свёртывания вследствие поступления содержимого гранул промиелоцитов в периферическую кровь. Лечение острого промиелоцитарного лейкоза исключительно эффективно, это достоверно доказано множеством документированных случаев лечения.
3 августа 2017 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США(FDA) одобрило к применению VYXEOS (Jazz Pharmaceuticals, Inc) для лечения взрослых с недавно диагностированными двумя подвидами ОМЛ (t- AML и AML-MRC). VYXEOS представляет собой липосомальную комбинацию цитарабина и даунорубицина и показало себя намного эффективнее при лечении этих двух подтипов , чем применение стандартной 7+3 комбинации. Лекарство продемонстрировало среднюю общую выживаемость 9,6 месяцев по сравнению с 5,9 месяцами при комбинации 7+3 [40]
В 2018 году FDA одобрила применение гласдегиба (glasdegib) в комбинации с низкодозным цитарабином для лечения пациентов в возрасте старше 75 лет, которым невозможно провести интенсивную химиотерапию. Одобрение препарат получил с условием размещения в инструкции предупреждения о высоком риске токсичности для плода.[41]
Целью индукционного этапа лечения является достижение полной ремиссии. Полная ремиссия не означает, что заболевание полностью вылечено. Скорее, состояние полной ремиссии говорит о невозможности обнаружить спящую болезнь существующими способами диагностики.[33] Полная ремиссия достигается у 50-70 % взрослых больных с впервые выявленным ОМЛ, разница зависит от прогностических факторов, о которых сказано выше.[42] Длительность ремиссии зависит от прогностических качеств исходного лейкоза. В основном, все случаи ремиссии без дополнительного, консолидирующего лечения закачиваются рецидивом.[43]
Консолидационное лечение[править | править код]
Даже после достижения полной ремиссии вероятно, немногие лейкозные клетки всё же выживают. Их так мало, что обнаружить их пока невозможно. В случае не проведения послеремиссионного, или консолидационного лечения почти у всех больных в конце — концов возникает рецидив.[44] Поэтому для того, чтобы избавиться от неопределимых больных клеток и предотвратить рецидив — то есть, достичь полного излечения, нужна дополнительная терапия. Вид лечения после достижения ремиссии определяется индивидуально в зависимости от прогностических факторов и общего состояния здоровья больного. При прогностически благоприятных подвидах лейкозов (например, при inv(16), t(8;21) и t(15;17) обычно назначают 3-5 дополнительных курса интенсивной химиотерапии, известной как консолидационное лечение. Больным с высоким риском рецидива (например, при наличии цитогенетических изменений, сопутствующего миелодиспластического синдрома, или при ОМЛ, связанном с предшествующим лечением обычно рекомендуется транплантация аллогенных стволовых клеток гемопоэтического ряда, если позволяет общее состояние и есть подходящий донор.[45][46] При ОМЛ со средней вероятностью рецидива (при нормальных цитогенетических показателях или с такими цитогенетическими изменениями, которые не попадают в группы риска)вопрос консолидационного лечения не столь ясен и определяется рядом специфических показателей — возрастом больного, общим состоянием его здоровья, системой ценностей, и наконец, наличием донора подходящих стволовых клеток.[46]
Тем больным, которым пересадка стволовых клеток после консолидационного лечения не показана, проводят иммунотерапию комбинацией гистамина гидрохлорида (цеплена) и пролейкина. Такое лечение позволяет снизить вероятность рецидива на 14 %, удлиняя ремиссию на 50 %.[47]
Таким образом, стандартной терапией ОМЛ признаны высокоинтенсивная химиотерапия (ВХТ) и трансплантация костного мозга.[48]
Однако результаты лечения, несмотря на относительно высокие ответы у молодых, остаются неудовлетворительными у лиц старше 65 лет (30-50%) связанные с ранней летальностью (10%) и непродолжительностью ремиссии. Больше половины с ОМЛ – это больные старшего возраста и/или со значимой сопутствующей патологией, которые, как правило, не могут получать высокотоксичные схемы химиотерапии, поэтому для их терапии применяют низкие дозы цитарабина цитарабина и поддерживающее лечение: антибиотики и гемотрансфузии.
С 2010 года в США для лечения ОМЛ рекомендовано применять гипометилирующие агенты (5-азацитидин, децитабин) у пациентов, которые не подходят для трансплантации костногомозговых клеток/интенсивной химиотерапии.[49] В процессе метилирования ДНК гипометилирующие агенты ковалентно связываются с ДНК-метилтрансферазой, что приводит к реактивации генов, после чего восстанавливается дифференцировка гемопоэтических клеток-предшественников и нормальное кроветворение. 5-азацитидин обладает двойным механизмом действия. Он встраивается не только в молекулу ДНК, но и в молекулу РНК. Тем самым 5-азацитидин понижает количество РНК в клетках, что приводит к цитостатическому эффекту вне зависимости от клеточной фазы.
На основании результатов исследования 3 фазы AZA-001 - международное, мультицентровое, контролируемое исследование в параллельных группах, в котором пациенты МДС высокого риска/ОМЛ (ВОЗ критерии) сравнивались со стандартно используемой терапией (сопроводительная терапия, интенсивная химиотерапия, низкие дозы цитарабина), азацитидин был зарегистрирован, в том числе и в РФ, для лечения этих групп больных. Было показано, что азацитидин в 2,5 раза увеличивает общую выживаемость пациентов с ОМЛ (критерии ВОЗ).[50]
Рецидив ОМЛ[править | править код]
При рецидиве ОМЛ единственным испытанным способом лечения, который может оказаться действенным, оказывается пересадка стволовых клеток при условии, если она ещё не применялась.[51][52][53]
При рецидиве ОМЛ больным, которым не планируется пересадка стволовых гемопоэтических клеток, или в случае рецидива после пересадки стволовых клеток можно предложить лечение в рамках клинического испытания, поскольку выбор среди обычных способов лечения весьма ограничен. В настоящее время проходит клинические испытания цитостатическое вещество клофарабин, также испытываются различные способы прицельной терапии с использованием ингибиторов фарнезилтрансферазы, децитабина и ингибиторов белка множественной лекарственной устойчивости, ингибиторы гистондеацетилазы цитарабина, блокаторы ангиогенеза, аналоги дезоксиаденозина. Иногда ограниченное количество методов терапии рецидивов ОМЛ вынуждает обращаться к паллиативному лечению.
После клинических испытаний триоксида мышьяка Управление по контролю за качеством пищевых продуктов и лекарственных препаратовСША одобрило его применение в качестве паллиативного средства лечения рецидивирующего острого промиелоцитарного лейкоза (ОПЛ). Также как и ПТРК триоксид мышьяка неэффективен при других подвидах ОМЛ.[54]
В 2000 году в США для лечения рецидивов ОМЛ у больных старше 60-ти лет, которых нельзя лечить высокими дозами химиопрепаратов, было разрешено применять гемтузумаб озогамицин (Милотарг), препарат, в котором, как предполагалось, цитотоксическое вещество — противоопухолевый антибиотик калихимицин — связан с моноклональным антителом, обеспечивающим доставку антибиотика точно в лейкозную клетку.[55]
20 июля 2018 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США(FDA) зарегистрировала первый ингибитор гена IDh2 ивосидениб (ivosidenib), предназначенный для лечения пациентов с рецидивом ОМЛ и обладающих мутацией онкогена IDh2. Терапия с применением ivosidenib позволяет пациентам достичь полной ремиссии ОМЛ, а так же снизить потребность в трансфузиях эритроцитов и тромбоцитов. В исследовании препарата ивосидениб участвовали 125 взрослых пациентов. КИ показали полный положительный ответ на лечение у 30,4% испытуемых (также ответ с частичным гематологическим восстановлением 8,8% пациентов, у которых количество лейкозных клеток находилось на умеренно низком уровне). Препарат стал первым лекарственным средством для лечения острого миелоидного лейкоза, одобренный в США. Регистрационное свидетельство на препарат было выдано компании Agios Pharmaceuticals.[56][57]
Хромосомная транслокация, (9;11), сочетающаяся с ОМЛОстрый миелоидный лейкоз — излечимое заболевание. Вероятность выздоровления каждого пациента разная, поскольку определяется множеством прогностических факторов.[58]
Цитогенетика[править |
Хронический миелоидный лейкоз — Википедия
Хронический миелоидный лейкоз (ХМЛ, хронический миелолейкоз) — форма лейкоза, которая характеризуется ускоренной и нерегулируемой пролиферацией преимущественно миелоидных клеток в костном мозге с их накоплением в крови. ХМЛ — гемопоэтическое клональное заболевание, основным проявлением которого является пролиферация зрелых гранулоцитов (нейтрофилов, эозинофилов и базофилов) и их предшественников. Это миелопролиферативное заболевание ассоциировано с характерной хромосомной транслокацией (филадельфийской хромосомой). В настоящее время основным способом лечения хронического миелолейкоза является таргетная (целевая) терапия ингибиторами тирозинкиназ, такими как иматиниб, нилотиниб, дазатиниб и другие, значительно улучшившая показатели выживаемости.
На примере ХМЛ впервые была показана связь злокачественного заболевания с конкретной генетической аномалией. В случае ХМЛ такой характерной аномалией является хромосомная транслокация, которая проявляется присутствием в кариотипе так называемой филадельфийской хромосомы. Эта мутантная хромосома получила своё название по месту работы её первооткрывателей, Питера Ноуелла (Пенсильванский университет) и Дэвида Хангерфорда (Онкологический центр Фокса Чейза), которые впервые описали её в 1960 году в Филадельфии (штат Пенсильвания, США)[2].
При этой транслокации, участки 9-й и 22-й хромосом меняются местами. В результате, фрагмент гена BCR из хромосомы 22 и ген ABL из хромосомы 9 образуют единую рамку считывания. Продуктами этого аномального слитого гена могут быть белки с молекулярной массой 210 (p210) или, реже, 185 кДа (p185). Так как в норме белок ABL содержит тирозинкиназный домен, продукт мутантного гена также является тирозинкиназой[3][4].
Белок BCR-ABL взаимодействует с одной из субъединиц клеточного рецептора к интерлейкину 3. Транскрипция гена BCR-ABL происходит непрерывно и не нуждается в активации другими белками. BCR-ABL активирует сигнальный каскад, контролирующий клеточный цикл, ускоряя деление клеток. Более того, белок BCR-ABL подавляет репарацию ДНК, вызывая неустойчивость генома и делая клетку более восприимчивой к дальнейшим генетическим аномалиям. Активность BCR-ABL — патофизиологическая причина хронического миелолейкоза. По мере изучения природы белка BCR-ABL и его тирозинкиназной активности, была разработана таргетная (целевая) терапия, позволяющая специфически ингибировать эту активность. Ингибиторы тирозинкиназ могут способствовать полной ремиссии ХМЛ, что ещё раз подтверждает ведущую роль BCR-ABL в развитии заболевания[4].
Заболевание часто протекает бессимптомно, выявляясь при рутинном клиническом анализе крови. В этом случае ХМЛ следует дифференцировать от лейкемоидной реакции, при которой мазок крови может иметь схожую картину. ХМЛ может проявляться недомоганием, субфебрильной лихорадкой, подагрой, повышенной восприимчивостью к инфекциям, анемией, тромбоцитопенией с кровоточивостью (хотя также может наблюдаться повышенное содержание тромбоцитов). Также отмечается спленомегалия.[3][5]
В течение ХМЛ выделяют три фазы на основании клинических характеристик и лабораторных данных. В отсутствие лечения ХМЛ обычно начинается с хронической фазы, в течение нескольких лет прогрессирует в фазу акселерации и, в конечном счёте, завершается бластным кризом. Бластный криз — терминальная фаза ХМЛ, клинически подобная острому лейкозу. Вовремя начатое медикаментозное лечение, как правило, может остановить прогрессирование болезни по этому пути. Одним из факторов прогрессии от хронической фазы к бластному кризу является приобретение новых хромосомных аномалий (в дополнение к филадельфийской хромосоме)[3]. Некоторые пациенты к моменту постановки диагноза могут находиться уже в фазе акселерации или бластного криза[5].
Хроническая фаза[править | править код]
Около 85 % пациентов с ХМЛ к моменту постановки диагноза находятся в хронической фазе. В течение этой фазы клинические проявления обычно отсутствуют или имеются «лёгкие» симптомы, такие как недомогание или чувство переполнения живота. Продолжительность хронической фазы различна и зависит от того, насколько рано было диагностировано заболевание, а также от проведённого лечения. В конечном счёте, при отсутствии эффективного лечения, заболевание переходит в фазу акселерации[5].
Фаза акселерации[править | править код]
Диагностические критерии перехода в фазу акселерации могут различаться: наиболее широко используются критерии, установленные исследователями онкологического центра Андерсона при Техасском университете[6], Сокалом с соавторами[7], а также Всемирной организацией здравоохранения[8][9]. Критерии ВОЗ, вероятно, наиболее широко распространены, и отличают фазу акселлерации по следующим признакам:
- 10—19 % миелобластов в крови или костном мозге;
- > 20 % базофилов в крови или костном мозге;
- < 100 000 тромбоцитов в микролитре крови, вне связи с терапией;
- > 1 000 000 тромбоцитов в микролитре крови, вне зависимости от терапии;
- цитогенетическая эволюция с развитием новых аномалий в дополнение к филадельфийской хромосоме;
- прогрессирование спленомегалии или увеличение числа лейкоцитов, вне зависимости от терапии.
Фаза акселерации предполагается при наличии любого из указанных критериев. Фаза акселерации указывает на прогрессию заболевания и приближение бластного криза[8]
Бластный криз[править | править код]
Бластный криз — финальная стадия развития ХМЛ, протекающая, подобно острому лейкозу, с быстрой прогрессией и непродолжительной выживаемостью[5]. Бластный криз диагностируется на основе одного из следующих признаков у пациента с ХМЛ[10]:
- >20 % миелобластов или лимфобластов в крови или костном мозге;
- крупные группы бластов в костном мозге при биопсии;
- развитие хлоромы (солидного фокуса лейкемии вне костного мозга).
Предположение о ХМЛ часто делается на основании общего анализа крови, демонстрирующего повышение количества гранулоцитов всех типов, включая зрелые миелоидные клетки. Количество базофилов и эозинофилов повышено практически всегда, что позволяет дифференцировать ХМЛ и лейкемоидную реакцию. При диагностике ХМЛ часто проводится биопсия костного мозга, однако одной лишь морфологической оценки костного мозга недостаточно для постановки диагноза ХМЛ[4][5].
В конечном счёте, ХМЛ диагностируется посредством выявления филадельфийской хромосомы в образцах костного мозга. Эта характерная хромосомная аномалия может быть выявлена в результате цитогенетического анализа, при помощи флюоресцентной гибридизации in situ или детекции гена BCR-ABL методом ПЦР[5].
Существуют разногласия в отношении так называемого Ph-негативного ХМЛ, или случаев предполагаемого ХМЛ, при котором филадельфийская хромосома не обнаруживается. У многих таких пациентов в действительности имеют место комплексные хромосомные аномалии, маскирующие транслокацию t(9;22), либо эта транслокация обнаруживается только при флюоресцентной гибридизации или ПЦР с обратной транскрипцией, но не при рутинном кариотипировании[11]. Для небольшой подгруппы пациентов с отсутствием молекулярных свидетельств присутствия гена BCR-ABL может быть поставлен диагноз недифференцированное миелодиспластическое/миелопролиферативное расстройство, так как оно, как правило, отличается от ХМЛ по клиническому течению[8].
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ Nowell P.C. Discovery of the Philadelphia chromosome: a personal perspective (англ.) // Journal of Clinical Investigation (англ.)русск. : journal. — 2007. — Vol. 117, no. 8. — P. 2033—2035. — doi:10.1172/JCI31771. — PMID 17671636.
- ↑ 1 2 3 Faderl S., Talpaz M., Estrov Z., Kantarjian H.M. Chronic myelogenous leukemia: biology and therapy (англ.) // Annals of Internal Medicine (англ.)русск.. — 1999. — Vol. 131, no. 3. — P. 207—219. — PMID 10428738.
- ↑ 1 2 3 Hehlmann R., Hochhaus A., Baccarani M; European LeukemiaNet. Chronic myeloid leukaemia (англ.) // The Lancet. — Elsevier, 2007. — Vol. 370, no. 9584. — P. 342—350. — doi:10.1016/S0140-6736(07)61165-9. — PMID 17662883.
- ↑ 1 2 3 4 5 6 Tefferi A. Classification, diagnosis and management of myeloproliferative disorders in the JAK2V617F era (англ.) // Hematology Am Soc Hematol Educ Program : journal. — 2006. — Vol. 2006. — P. 240—245. — doi:10.1182/asheducation-2006.1.240. — PMID 17124067.
- ↑ Kantarjian H., Dixon D., Keating M., Talpaz M., Walters R., McCredie K., Freireich E. Characteristics of accelerated disease in chronic myelogenous leukemia (англ.) // Cancer (англ.)русск. : journal. — Wiley-Blackwell (англ.)русск., 1988. — Vol. 61, no. 7. — P. 1441—1446. — doi:10.1002/1097-0142(19880401)61:7<1441::AID-CNCR2820610727>3.0.CO;2-C. — PMID 3162181.
- ↑ Sokal J., Baccarani M., Russo D., Tura S. Staging and prognosis in chronic myelogenous leukemia (англ.) // Semin Hematol : journal. — 1988. — Vol. 25, no. 1. — P. 49—61. — PMID 3279515.
- ↑ 1 2 3 Tefferi A., Thiele J., Orazi A., Kvasnicka H.M., Barbui T., Hanson C.A., Barosi G., Verstovsek S., Birgegard G., Mesa R., Reilly J.T., Gisslinger H., Vannucchi A.M., Cervantes F., Finazzi G., Hoffman R., Gilliland D.G., Bloomfield C.D., Vardiman J.W. Proposals and rationale for revision of the World Health Organization diagnostic criteria for polycythemia vera, essential thrombocythemia, and primary myelofibrosis: recommendations from an ad hoc international expert pane (англ.) // Blood (англ.)русск. : journal. — American Society of Hematology (англ.)русск., 2007. — Vol. 110, no. 4. — P. 1092—1097. — doi:10.1182/blood-2007-04-083501. — PMID 17488875.
- ↑ Vardiman J., Harris N., Brunning R. The World Health Organization (WHO) classification of the myeloid neoplasms (англ.) // Blood (англ.)русск. : journal. — American Society of Hematology (англ.)русск., 2002. — Vol. 100, no. 7. — P. 2292—2302. — doi:10.1182/blood-2002-04-1199. — PMID 12239137. Архивировано 6 ноября 2006 года.
- ↑ Karbasian Esfahani M., Morris E.L., Dutcher J.P., Wiernik P.H. Blastic phase of chronic myelogenous leukemia (неопр.) // Current Treatment Options in Oncology. — 2006. — Т. 7, № 3. — С. 189—199. — doi:10.1007/s11864-006-0012-y. — PMID 16615875.
- ↑ Savage DG; Szydlo RM; Goldman J.M. Clinical features at diagnosis in 430 patients with chronic myeloid leukaemia seen at a referral centre over a 16-year period (англ.) // British Journal of Haematology (англ.)русск. : journal. — 1997. — Vol. 96, no. 1. — P. 111—116. — doi:10.1046/j.1365-2141.1997.d01-1982.x. — PMID 9012696.
Особенности протекания и лечения миелоидного лейкоза
Злокачественные клетки могут поразить любую систему, орган, ткань организма, в том числе, кровь. При развитии опухолевых процессов миелоидного ростка крови, сопровождаемого интенсивным размножением изменённых белых кровяных клеток, диагностируется болезнь, называемая миелоидным лейкозом (миелолейкозом).

Что такое миелолейкоз
Заболевание представляет собой один из подтипов лейкемии (рака крови). Развитие миелолейкоза сопровождается злокачественным перерождением незрелых лимфоцитов (бластов) в красном костном мозге. В результате распространения по организму мутировавших лимфоцитов поражается сердечно-сосудистая, лимфатическая, мочевыделительная, другие системы.
Классификация (виды)
Профильные медицинские специалисты выделяют миелоидный лейкоз (код по МКБ-10 – C92), протекающий в атипичной форме, миелоидную саркому, хронический, острый (промиелоцитарный, миеломоноцитарный, с 11q23-аномалией, с многолинейной дисплазией), другой миелоидный лейкоз, не уточнённые патологические формы.
Острая и хроническая стадии прогрессирующего миелолейкоза (в отличие от множества других недугов) не трансформируются друг в друга.
Острый миелоидный лейкоз
Острый миелолейкоз характеризуется стремительным развитием, активным (избыточным) ростом бластных незрелых кровяных клеток.
Выделяют следующие стадии остро протекающего миелолейкоза:
- Начальную. Во многих случаях протекает бессимптомно, обнаруживаясь при проведении биохимии крови. Симптоматика проявляется обострением хронических заболеваний.
- Развёрнутую. Характеризуется выраженной симптоматикой, периодами ремиссий и обострений. При эффективно организованном лечении наблюдается полная ремиссия. Запущенные формы миелолейкоза переходят в более тяжёлые стадии.
- Терминальную. Сопровождается дестабилизацией процесса кроветворения.
Хронический миелоидный лейкоз
Хронический миелолейкоз (при описании используется аббревиатура ХМЛ) сопровождается интенсивным ростом лейкоцитарных клеток, замещением здоровых тканей костного мозга соединительной тканью. Миелолейкоз обнаруживается преимущественно в пожилом возрасте. При обследованиях диагностируют одну из стадий:
- Доброкачественную. Сопровождается повышением концентрации лейкоцитов без ухудшения самочувствия.
- Акселеративную. Обнаруживаются признаки заболевания, число лейкоцитов продолжает расти.
- Бластный криз. Проявляется резким ухудшением состояния здоровья, инфекционными осложнениями, низкой чувствительностью к лечению.

Если в ходе анализа клинической картины невозможно точно определить характер прогрессирующей патологии, ставится диагноз «не уточнённый миелолейкоз» или «другой миелоидный лейкоз».
Причины развития заболевания
Миелоидный лейкоз – одна из болезней, характеризующихся не до конца изученными механизмами развития. Медицинские специалисты, изучая потенциальные причины, спровоцировавшие хронический или острый миелоидный лейкоз, используют термин «фактор риска».
Повышение вероятности развития миелолейкоза обуславливается:
- Наследственными (генетическими) особенностями.
- Осложненным течением синдромов Блума, Дауна.
- Отрицательными последствиями влияния ионизирующего излучения.
- Прохождением курсов лучевой терапии.
- Длительным применением некоторых типов лекарственных препаратов.
- Перенесёнными аутоиммунными, раковыми, инфекционными болезнями.
- Тяжёлыми формами туберкулеза, ВИЧ, тромбоцитопении.
- Контактами с ароматическими органическими растворителями.
- Загрязнённостью экологии.
Среди факторов, провоцирующих миелоидный лейкоз у детей, выделяют генетические болезни (мутации), а также особенности течения периода беременности. Онкологическое заболевание крови у малыша может развиваться вследствие пагубного влияния радиационного, других видов излучения на женщин в период беременности, отравления, табакокурения, других вредных привычек, тяжёлых болезней матери.
Симптомы
Преобладающие симптомы, проявляющиеся при миелолейкозе, определяются стадией (степенью тяжести) заболевания.
Проявления на начальной стадии
Доброкачественный миелоидный лейкоз на начальной стадии не сопровождается выраженной симптоматикой и нередко обнаруживается случайно, в ходе сопутствующего диагностирования.
Симптомы акселеративной стадии
Акселеративная стадия проявляется:
- Потерей аппетита.
- Похудением.
- Повышенной температурой.
- Упадком сил.
- Одышкой.
- Учащёнными кровотечениями.
- Побледнением кожи.
- Гематомами.
- Обострениями воспалительных заболеваний носоглотки.
- Нагноениями повреждений кожных покровов (царапин, ран).
- Болезненными ощущениями в ногах, позвоночнике.
- Вынужденной ограниченностью двигательной активности, изменениями походки.
- Увеличением небных миндалин.
- Припухлостью десен.
- Повышением числа лейкоцитов, концентрации мочевой кислоты в крови.

Симптомы терминальной стадии
Для терминальной стадии миелолейкоза характерно стремительное развитие симптоматики, ухудшение самочувствия, развитие необратимых патологических процессов.
Симптоматика миелолейкоза дополняется:
- Многочисленными кровоизлияниями.
- Интенсификацией потоотделения.
- Стремительной потерей веса.
- Ноющими костными, суставными болями различной интенсивности.
- Повышением температуры до 38-39 градусов.
- Ознобом.
- Увеличением селезёнки, печени.
- Частыми обострениями инфекционных недугов.
- Анемией, снижением концентрации тромбоцитов, появлением миелоцитов, миелобластов в крови.
- Формированием некротических зон на слизистых оболочках.
- Увеличением лимфоузлов.
- Сбоями в функционировании зрительной системы.
- Головными болями.
Терминальная стадия миелолейкоза сопровождается бластным кризом, повышенным риском смертельного исхода.
Особенности течения хронического миелолейкоза
Хроническая стадия имеет наибольшую продолжительность (в среднем – около 3-4 лет) среди всех стадий недуга. Клиническая картина миелолейкоза преимущественно размыта и не вызывает опасений у пациента. С течением времени заболевания симптомы усугубляются, совпадая с проявлениями острой формы.
Ключевая особенность хронического миелоидного лейкоза заключается в более низкой скорости развития симптоматики и осложнений по сравнению со стремительно прогрессирующей острой формой.
Как проводится диагностика
Первичная диагностика миелолейкоза включает осмотр, анализ анамнеза, оценку размеров печени, селезёнки, лимфоузлов при помощи пальпации. Для того чтобы максимально тщательно изучить клиническую картину и назначить эффективную терапию, в профильных медучреждениях проводят:
- Развёрнутые исследования крови (миелоидный лейкоз у взрослых и детей сопровождается повышением концентрации лейкоцитов, появлением бластов в крови, показатели эритроцитов, тромбоцитов снижаются).
- Биопсию костного мозга. В ходе манипуляции через кожные покровы в костный мозг вводится полая игла, производится забор биоматериала с последующим микроскопическим исследованием.
- Спинномозговую пункцию.
- Ультразвуковое сканирование.
- Рентгенографическое обследование грудной клетки.
- Генетические исследования крови, костного мозга, лимфатических узлов.
- ПЦР-тест.
- Иммунологические обследования.
- Сцинтиграфию костей скелета.
- Томографию (компьютерную, магнитно-резонансную).
При необходимости перечень диагностических мероприятий расширяется.
Лечение
Терапия миелолейкоза, назначаемая после подтверждения диагноза, проводится в стационаре медицинского учреждения. Методы лечения могут быть разными. Принимаются во внимание результаты предыдущих этапов лечения (если оно проводилось).
Лечение хронического миелоидного лейкоза включает:
- Индукционную, медикаментозную терапию.
- Трансплантацию стволовых клеток.
- Противорецидивные мероприятия.
Индукционная терапия
Проводимые процедуры способствуют уничтожению (прекращению роста) онкологических клеток. Цитотоксические, цитостатические средства вводятся в спинномозговую жидкость, очаги, где сконцентрирована основная масса онкоклеток. Для усиления эффекта применяют полихимиотерапию (введение группы химиопрепаратов).
Положительные результаты индукционной терапии миелолейкоза наблюдаются после прохождения нескольких лечебных курсов.
Дополнительные методы медикаментозной терапии
Специфическое лечение мышьяковым триоксидом, ATRA (транс-ретиноевой кислотой) используют при выявлении острого промиелоцитарного лейкоза. С целью остановки роста и деления лейкемических клеток применяют моноклональные антитела.
Пересадка стволовых клеток
Трансплантация отвечающих за кроветворение стволовых клеток – действенный метод терапии миелолейкоза, способствующий восстановлению нормального функционирования костного мозга, иммунной системы. Пересадку проводят:
- Аутологичным способом. Клеточный забор осуществляется у пациента в ремиссионный период. Замороженные, обработанные клетки вводятся после химиотерапии.
- Аллогенным способом. Клетки пересаживаются от доноров-родственников.
ВАЖНО! Вопрос проведения лучевой терапии миелолейкоза рассматривается только при подтверждении распространения раковых клеток на спинной, головной мозг.
Противорецидивные мероприятия
Цель противорецидивных мероприятий – закрепление результатов химиотерапии, устранение остаточной симптоматики миелолейкоза, снижение вероятности повторных обострений (рецидивов).
В рамках противорецидивного курса применяют препараты, способствующие улучшению кровообращения. Проводятся поддерживающие химиотерапевтические курсы со сниженной дозировкой действующих веществ. Продолжительность противорецидивного лечения миелолейкоза определяется индивидуально: от нескольких месяцев до 1-2 лет.

Для оценки результативности применяемых лечебных схем, контроля динамики проводятся периодические обследования, направленные на выявление раковых клеток, определение степени поражения тканей миелолейкозом.
Осложнения от терапии
Осложнения от химиотерапии
Пациентам с диагнозом «острый миелоидный лейкоз» в рамках лечебных курсов вводятся препараты, наносящие ущерб здоровым тканям и органам, поэтому риск осложнений находится на неизбежно высоком уровне.
К перечню часто обнаруживаемых побочных эффектов медикаментозной терапии миелолейкоза относят:
- Уничтожение здоровых клеток вместе с онкоклетками.
- Ослабление иммунитета.
- Общее недомогание.
- Ухудшение состояния волос, кожных покровов, облысение.
- Потерю аппетита.
- Нарушение функционирования пищеварительной системы.
- Анемию.
- Повышенный риск кровотечений.
- Сердечно-сосудистые обострения.
- Воспалительные болезни полости рта.
- Искажения вкусовых ощущений.
- Дестабилизацию функционирования репродуктивной системы (менструальные нарушения у женщин, прекращение выработки спермы у мужчин).
Преимущественное большинство осложнений лечения миелолейкоза самоустраняется после завершения химиотерапии (или в перерывах между курсами). Некоторые подвиды сильнодействующих медикаментов могут спровоцировать бесплодие и другие необратимые последствия.
Осложнения после трансплантации костного мозга
После проведения процедуры трансплантации повышается риск:
- Развития кровотечений.
- Распространения инфекции по организму.
- Отторжения трансплантата (может произойти в любой момент времени, даже через несколько лет после пересадки).
Во избежание осложнений миелолейкоза необходимо осуществлять постоянный мониторинг состояния пациентов.
Особенности питания
Несмотря на ухудшение аппетита, наблюдающееся при хроническом и остром миелоидном лейкозе, необходимо придерживаться предписанного специалистом режима питания.
Для восстановления сил, удовлетворения потребностей организма, угнетенного миелобластным (миелоидным) лейкозом, предотвращения неблагоприятных последствий интенсивной терапии белокровия, необходима сбалансированная диета.
При миелолейкозе и других формах лейкемии рекомендуется дополнять рацион питания:
- Продуктами, богатыми витамином C, микроэлементами.
- Зеленью, овощами, ягодами.
- Рисовой, гречневой, пшеничной кашей.
- Морской рыбой.
- Молочными продуктами (нежирным пастеризованным молоком, творогом).
- Мясом кролика, субпродуктами (почками, языком, печенью).
- Прополисом, медом.
- Травяным, зелёным чаем (оказывает антиоксидантное действие).
- Оливковым маслом.

Для недопущения перегрузок пищеварительного тракта и других систем при миелолейкозе из меню исключают:
- Алкоголь.
- Продукты, содержащие трансжиры.
- Фастфуд.
- Копчёные, жареные, изобилующие солью блюда.
- Кофе.
- Сдобу, кондитерские изделия.
- Продукты, способствующие разжижению крови (лимон, калину, клюкву, какао, чеснок, орегано, имбирь, паприку, карри).
При миелолейкозе необходимо контролировать объём потребления белковой пищи (не более 2 г. в сутки на 1 кг. массы тела), поддерживать водный баланс (от 2-2,5 л. жидкости в сутки).
Прогноз продолжительности жизни
Миелолейкоз – болезнь, сопровождаемая повышенным риском летального исхода. Продолжительность жизни при остром или хроническом миелоидном лейкозе определяется:
- Стадией, на которой был обнаружен миелолейкоз и начато лечение.
- Возрастными особенностями, состоянием здоровья.
- Уровнем лейкоцитов.
- Чувствительностью к химической терапии.
- Интенсивностью поражения головного мозга.
- Продолжительностью периода ремиссии.
При своевременном проведении лечения, отсутствии симптомов осложнений ОМЛ прогноз жизни при остром миелоидном лейкозе благоприятен: вероятность пятилетней выживаемости составляет порядка 70%. В случае наличия осложнений показатель снижается до 15%. В детском возрасте вероятность выживаемости достигает 90%. Если терапия миелолейкоза не проводится, показатель даже 1-летней выживаемости находится на низкой отметке.
Хроническая стадия миелолейкоза, при которой проводятся систематические лечебные мероприятия, характеризуется благоприятным прогнозом. У большинства пациентов продолжительность жизни после своевременной идентификации миелолейкоза превышает 20 лет.
Пожалуйста, оставьте свой отзыв о статье, используя форму в нижней части страницы.
симптомы, лечение, анализ крови, стадии и прогноз жизни
Миелолейкоз – заболевание, имеющее прямое отношение к онкологии, заключается в поражении клеток крови. Миелоидный лейкоз действует на стволовые клетки костного мозга. Код по МКБ-10 у болезни C92. Патология распространяется стремительно, поэтому уже через некоторое время поражённые элементы прекращают выполнять функции. Способен продолжительное время протекать, не показывая симптомов. По статистике выявляется чаще у людей от 30 лет.
Причины
Как все онкологические заболевания, атипичный лейкоз не изучен. Сейчас исследователи, медики предполагают о возможных причинах возникновения патологии:
- распространённой теорией считается воздействие химических препаратов на человека;
- бактериальные заболевания;
- длительное воздействие веществ аренов;
- побочные действия от лечения опухолей;
- результат иного онкологического заболевания.
Учёные активно раскрывают возможные пути появления болезни, чтобы впоследствии изучить и искоренить нарушение.
Факторы риска
Ряд обстоятельств способен ощутимо повлиять на возникновение онкологии, а именно:
- воздействие радиации;
- пол;
- возраст.
Две трети факторов невозможно изменить, но постараться избежать первого – вполне осуществимо.
Виды
Работники медицины различают две видовые группы миелолейкоза.
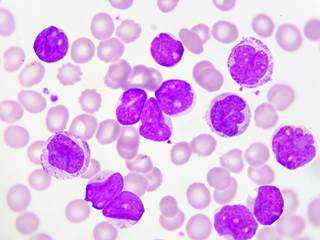
Клетки крови при миелолейкозе
Острый
При обостренной форме онкологии происходит заражение клеток, не поддающееся контролю. В короткий срок здоровая клетка заменяется поражённой. Своевременное лечение поможет продлить жизнь человека. Его отсутствие ограничивает существование человека сроком до 2 месяцев.
Первый симптом острого миелолейкоза может не вызвать тревожности, но полагается обратиться к врачу за вердиктом. Онкологические симптомы миелолейкоза проявляются одновременно либо нарастают постепенно.
Острый миелобластный синдром и симптомы:
- боли в костях и суставах;
- носовые кровоизлияния;
- повышенное выделение пота во время сна;
- сбои в кровотечении, что является причиной бледности кожи;
- частые заражения;
- воспаление дёсен;
- появление гематом по площади тела;
- проблемы с дыханием даже при низком уровне физической активности.
Проявление двух и более симптомов свидетельствует о серьёзных сбоях в организме, рекомендуется посетить поликлинику. Назначение своевременного лечения поможет сохранить жизнь.

Острый миелолейкоз обнаруживает классификацию, включающую массу факторов и причин, обособленных в группы:
- примитивные изменения в генах;
- изменения на почве нарушения развития тканей, органов;
- следствие иных заболеваний;
- синдром Дауна;
- миелоидная саркома;
- лечение, диагностика, симптомы и признаки могут различаться.
Хронический лимфоцитарный лейкоз
В этом случае учёными установлена связь, определяющая причину возникновения болезни и нарушения в генетической составляющей человека. Лимфолейкоз действует только на стволовые клетки, способные неограниченно делиться. Мутации происходят в новых клетках, так как за счёт незакончившегося формирования в них легче проникнуть. Здоровая кровяная клетка постепенно преобразовываются в лейкоцит. После скапливаются в костном мозге и уже оттуда циркулируют по телу, медленно заражая органы человека. Хронический миелолейкоз (ХМЛ) способен перейти в острый лимфобластный лейкоз.
Этапы хронического миелолейкоза:
Первый этап. Болезнь нарастает постепенно. Характеризуется увеличением селезёнки, вторичными признаками миелолейкоза: увеличивается уровень зернистых лейкоцитов, а также безъядерных элементов в периферической крови. Симптомы первого этапа хронического миелолейкоза можно сопоставить с симптомами при остром миелолейкозе: появляется одышка, тяжесть в желудке, потливость. Серьёзные ощущения, свидетельствующие об усилении онкологии:
- боль под рёбрами, перетекающая в боль спины;
- истощение организма.
На фоне этого может развиться инфаркт селезёнки, а после появятся проблемы с печенью.

Второй этап хронической онкологии характеризуется ускоренным развитием живой злокачественной опухоли. Начальная стадия болезни не показывается либо выражается в крайне малой степени. Для такого состояния характерны:
- повышение температуры тела;
- анемия;
- быстрая утомляемость;
- также продолжает увеличиваться количество белых кровяных клеток;
- помимо лейкоцитов увеличиваются и другие кровяные клетки.
Прогностические результаты и оперативное прохождение нужных процедур приводят к тому, что в крови обнаруживаются компоненты, которых не должно быть при нормальном развитии организма. Повышается степень несозревших лейкоцитов. Это влияет на периодический зуд кожного покрова.
Третья (заключительная) стадия характеризуется патофункциональными изменениями, при которых происходит кислородное голодание каждой части человеческой ткани, а также нарушение внутреннего обмена веществ. Больше кислородным голоданием страдают клетки мозга. Наиболее серьезные проявления терминальной стадии:
- суставные боли;
- усталость;
- повышение температуры до 40 градусов;
- резко снижается масса больного;
- инфаркт селезенки;
- позитивный pH.
Среди дополнительных симптомов отмечают проблемы с нервными окончаниями, изменения внутренней составляющей крови. Продолжительность жизни при данной стадии болезни зависит от используемых препаратов и терапии.
Диагностика
Современные методы преуспевают в вычислении онкологических заболеваний. Распространенные, стандартные процессы, которые позволяют выявить у человека злокачественный элемент клетки крови:

- Проводится ОАК. Благодаря этой процедуре устанавливается степень общего количества клеток. Что это дает? У пациентов, страдающих миелолейкозом, увеличивается количество незрелых клеток, а также зафиксировано снижение количества эритроцитов и тромбоцитов.
- Биохимический анализ крови позволяет выявить перебои в функционировании печени и селезенки. Такие неполадки спровоцированы проникновением в органы лейкозных клеток.
- Забор тканей и клеток, а также проникновение инородных тел в костный мозг. Эти две процедуры проводятся в одно время. Прототипы мозга берутся из бедренной кости.
- Метод исследования генетики и развития человека посредством исследования хромосом. В структуре генов человека при болезни онкологией содержатся лейкозные клетки, именно они позволяют обнаружить острый миелоидный лейкоз.
- Смешение разных орбиталей атома молекулы. Таким методом изучают хромосомы, при болезни онкологией находится аномальная.
- Миелограмма показывает статистику костного мозга в виде таблицы.
- Гемограмма позволяет обследовать пациента и точно установить диагноз. Для нее характерно быстрое распределение компонентов, развернутый метод установление локализации.
Применяются и стандартные методы диагностики: МРТ, УЗИ и т.д. Они не могут обещать больному выявления точного диагноза или стадии.
Лечение
Так как есть отличия между симптомами хронического и острого заболевания, следовательно, и лечение предусмотрено разное.
Лечение хронического миелолейкоза
Фазы разделяют степени поражения организма человека, поэтому лечение предусматривается в зависимости от этапа болезни. При хроническом или неактивном этапе рекомендуется соблюдать общие нормы лечения, вести здоровый образ жизни, питание должно быть насыщено витаминами. Отдых на этом этапе сопоставляется труду, количество витаминов также прописывается.

Если уровень лейкоцитов продолжает увеличиваться, замечаются осложнения, больным прописывают цитостатические медикаменты. После прохождения курса лечения лекарственным препаратом поддерживается терапия, которая направлена на восстановление правильного функционирования селезёнки. Радиотерапия используется, когда селезёнка не приняла первоначальный облик. После чего курс лечения прерывается сроком на 31 день, затем повторяется, проводя восстанавливающую терапию.
Фаза кислородного голодания чаще всего практикует один, реже два химических препарата. Чаще ими являются специализированные препараты, в которых заложены некоторые группы витаминов, способствующие поддержанию здоровья и жизни в человеке. Принцип применения такой же, как и в неактивной фазе: сначала проводится эффективная терапия, а затем поддерживающее применение. Курсы внутривенного введения химических препаратов проводятся от трех раз в год. Если методика не срабатывает, проводится процедура разделения крови на плазму и иные составляющие. При симптомах ХМЛ применяются переливания донорской крови, в состав которой входят непосредственно клетки, плазма, а также примеси эритроцитов и тромбоцитов. Радиотерапию вводят при значительных величинах злокачественной опухоли.
Гарантию на выздоровление 70% страдающих миелолейкозом получили при пересадке костного мозга. Данная процедура проводится на начальном этапе недомоганий. И может быть следствием удаления селезенки. Этот орган может быть «убран» двумя путями: незапланированный заключается в разрыве селезенки, а основной зависит от ряда факторов. Костный мозг для пересадки должен быть идентичен мозгу больного.
Лечение острого миелолейкоза
Химиотерапию принято считать фундаментом лечения при миелолейкозе. Процесс разделяется на две части: до ремиссии и после неё. Следует помнить о мерах безопасности. После химиотерапии может наступить рецидив либо инвалидность.
Какие клинические рекомендации прослеживаются? На индукционной ступени лечения проводится комплекс мероприятий, направленных на устранение причин и симптомов заболевания, удаление ненужных лейкозных клеток. Консолидационные мероприятия устраняют возможности рецидива, поддерживают нормальное состояние человека. Классификация влияет на принцип лечения ОМЛ, возраст, пол, индивидуальную переносимость и возможности.
Распространение получила методика внутривенного введения цитостатического препарата. Процесс продолжается в течение недели. Первые три дня сочетаются с иным медикаментом группы антибиотиков.
Когда присутствует риск развития телесных заболеваний либо инфекционных, применяется менее интенсивная процедура, суть которой состоит в создании комплекса мероприятий для больного. Сюда входит хирургическое вмешательство, психотерапевтическая помощь больному и т. д.
Индукционные мероприятия дают положительные результат более чем у 50% больных. Отсутствие второй степени консолидации приводит к рецидиву, поэтому считается необходимым мероприятием. При возможности возвращения рака после стандартно-прописанных 3-5 процедур поддерживающей химиотерапии проводится пересадка костного мозга. Кроветворение способствует восстановлению организма. Для анализа требуется периферическая кровь. В Израиле показатели выздоровления от лимфолейкоза высоки за счет того, что неблагоприятные условия для человека ликвидируются сразу, опухолевый процесс спадает. Метод обнаружения бласт в периферической крови также используется и там.
Бластный криз – злокачественный процесс, считается заключающим. На данной стадии синдромы невозможно излечить, лишь поддерживать процессы жизнедеятельности, так как этиология и патогенез фазы до конца не изучены. Негативный опыт говорит о том, что лейкоциты превышают нужный объём.
Прогноз острого миелолейкоза
Онкологи дают разную оценку выживаемости при ОМЛ, так как обуславливается некоторым количеством факторов, например, возраст, пол и другие. Стабильная оценка классификаций ОМЛ показала, что средняя выживаемость разнится от 15 до 65%. Прогноз возвращения болезни от 30 до 80%.
Наличие телесных, инфекционных расстройств становится причиной худшего прогноза для людей пожилого возраста. Наличие параллельных недугов делает недоступной химиотерапию, так необходимую для лечения миелолейкоза. При гематологических заболеваниях картина выглядит гораздо неутешительнее, чем при возникновении злокачественной опухоли как результата сопутствующей болезни. Острый миелобластный лейкоз редко наблюдается у детей, чаще у взрослых.
Прогноз хронического миелолейкоза
Определяющей причиной положительного результата является момент начала лечения. От продолжительности и вероятности вылечить рак зависят последующие факторы: величина расширения печени, селезёнки, количество безъядерных элементов крови, белых кровяных клеток, незрелых клеток костного мозга.
Возможность летального исхода растёт вместе с количеством признаков, определяющих развитие онкологии. Частой причиной смерти становятся сопутствующие инфекции или подкожные кровоизлияния частей тела. Средняя продолжительность жизни – два года. Оперативное определение и лечение болезни способно умножить этот срок в десяток раз.
Острый миелоидный лейкоз - причины, симптомы, диагностика и лечение, прогноз
Острый миелоидный лейкоз – злокачественное заболевание системы крови, сопровождающееся неконтролируемым размножением измененных лейкоцитов, снижением количества эритроцитов, тромбоцитов и нормальных лейкоцитов. Проявляется повышенной склонностью к развитию инфекций, лихорадкой, быстрой утомляемостью, потерей веса, анемией, кровоточивостью, образованием петехий и гематом, болями в костях и суставах. Иногда выявляются изменения кожи и припухлость десен. Диагноз устанавливается на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, трансплантация костного мозга.
Общие сведения
Острый миелоидный лейкоз (ОМЛ) – злокачественное поражение миелоидного ростка крови. Неконтролируемая пролиферация лейкозных клеток в костном мозге влечет за собой подавление остальных ростков крови. В результате количество нормальных клеток в периферической крови уменьшается, возникают анемия и тромбоцитопения. Острый миелоидный лейкоз является самым распространенным острым лейкозом у взрослых. Вероятность развития болезни резко увеличивается после 50 лет. Средний возраст пациентов составляет 63 года. Мужчины и женщины молодого и среднего возраста страдают одинаково часто. В старшей возрастной группе наблюдается преобладание лиц мужского пола. Прогноз зависит от вида острого миелоидного лейкоза, пятилетняя выживаемость колеблется от 15 до 70%. Лечение осуществляют специалисты в области онкологии и гематологии.
Острый миелоидный лейкоз
Причины острого миелоидного лейкоза
Непосредственной причиной развития ОМЛ являются различные хромосомные нарушения. В числе факторов риска, способствующих развитию таких нарушений, указывают неблагоприятную наследственность, ионизирующее излучение, контакт с некоторыми токсическими веществами, прием ряда лекарственных препаратов, курение и болезни крови. Вероятность возникновения острого миелоидного лейкоза увеличивается при синдроме Блума (низкий рост, высокий голос, характерные черты лица и разнообразные кожные проявления, в том числе гипо- или гиперпигментация, кожная сыпь, ихтиоз, гипертрихоз) и анемии Фанкони (низкий рост, дефекты пигментации, неврологические расстройства, аномалии скелета, сердца, почек и половых органов).
Острый миелоидный лейкоз достаточно часто развивается у больных с синдромом Дауна. Прослеживается также наследственная предрасположенность при отсутствии генетических заболеваний. При ОМЛ у близких родственников вероятность возникновения болезни повышается в 5 раз по сравнению со средними показателями по популяции. Самый высокий уровень корреляции выявляется у однояйцевых близнецов. Если острый миелоидный лейкоз диагностируется у одного близнеца, риск у второго составляет 25%. Одним из важнейших факторов, провоцирующих ОМЛ, являются заболевания крови. Хронический миелоидный лейкоз в 80% случаев трансформируется в острую форму болезни. Кроме того, ОМЛ нередко становится исходом миелодиспластического синдрома.
Ионизирующее излучение вызывает острые миелоидные лейкозы при превышении дозы 1 Гр. Заболеваемость увеличивается пропорционально дозе облучения. На практике имеет значение пребывание в зонах атомных взрывов и аварий на атомных электростанциях, работа с источниками излучения без соответствующих защитных средств и радиотерапия, применяемая при лечении некоторых онкологических заболеваний. Причиной развития острого миелоидного лейкоза при контакте с токсическими веществами является аплазия костного мозга в результате мутаций и поражения стволовых клеток. Доказано негативное влияние толуола и бензола. Обычно ОМЛ и другие острые лейкозы диагностируются спустя 1-5 лет после контакта с мутагеном.
В числе лекарственных средств, способных провоцировать острые миелоидные лейкозы, специалисты называют некоторые препараты для химиотерапии, в том числе ингибиторы ДНК-топоизомеразы II (тенипозид, этопозид, доксорубицин и другие антрациклины) и алкилирующие средства (тиофосфамид, эмбихин, циклофосфамид, хлорамбуцил, кармустин, бусульфан). ОМЛ также может возникать после приема хлорамфеникола, фенилбутазона и препаратов мышьяка. Доля лекарственных острых миелоидных лейкозов составляет 10-20% от общего количества случаев заболевания. Курение не только повышает вероятность развития ОМЛ, но и ухудшает прогноз. Средняя пятилетняя выживаемость и продолжительность полных ремиссий у курильщиков ниже, чем у некурящих.
Классификация острого миелоидного лейкоза
Классификация острого миелоидного лейкоза по версии ВОЗ очень сложна и включает в себя несколько десятков разновидностей заболевания, разделенных на следующие группы:
- ОМЛ с типичными генетическими изменениями.
- ОМЛ с изменениями, обусловленными дисплазией.
- Вторичные острые миелоидные лейкозы, возникшие в результате лечения других заболеваний.
- Болезни с пролиферацией миелоидного ростка при синдроме Дауна.
- Миелоидная саркома.
- Бластная плазмацитоидная дендритноклеточная опухоль.
- Другие виды острого миелоидного лейкоза.
Тактика лечения, прогноз и продолжительность ремиссий при разных видах ОМЛ могут существенно различаться.
Симптомы острого миелоидного лейкоза
Клиническая картина включает в себя токсический, геморрагический, анемический синдромы и синдром инфекционных осложнений. На ранних стадиях проявления острого миелоидного лейкоза неспецифичны. Отмечается повышение температуры без признаков катарального воспаления, слабость, утомляемость, потеря веса и аппетита. При анемии присоединяются головокружения, обморочные состояния и бледность кожных покровов. При тромбоцитопении наблюдаются повышенная кровоточивость и петехиальные кровоизлияния. Возможно образование гематом при незначительных ушибах. При лейкопении возникают инфекционные осложнения: частые нагноения ран и царапин, упорные повторные воспаления носоглотки и т. д.
В отличие от острого лимфобластного лейкоза при остром миелоидном лейкозе отсутствуют выраженные изменения со стороны периферических лимфатических узлов. Лимфоузлы небольшие, подвижные, безболезненные. Иногда выявляется увеличение лимфатических узлов в шейно-надключичной области. Печень и селезенка в пределах нормы или незначительно увеличены. Характерны признаки поражения костно-суставного аппарата. Многие больные острым миелоидным лейкозом предъявляют жалобы на боли различной степени интенсивности в области позвоночника и нижних конечностей. Возможны ограничения движений и изменения походки.
В числе экстрамедуллярных проявлений острого миелоидного лейкоза – гингивит и экзофтальм. В отдельных случаях наблюдаются припухлость десен и увеличение небных миндалин в результате инфильтрации лейкозными клетками. При миелоидной саркоме (составляет около 10% от общего количества случаев острого миелоидного лейкоза) на коже пациентов появляются зеленоватые, реже – розовые, серые, белые или коричневые опухолевидные образования (хлоромы, кожные лейкемиды). Иногда при поражениях кожи обнаруживается паранеопластический синдром (синдром Свита), который проявляется воспалением кожных покровов вокруг лейкемидов.
В развитии острого миелоидного лейкоза выделяют пять периодов: начальный или доклинический, разгара, ремиссии, рецидива и терминальный. В начальном периоде острый миелоидный лейкоз протекает бессимптомно или проявляется неспецифической симптоматикой. В периоде разгара токсический синдром становится более выраженным, выявляются анемический, геморрагический и инфекционный синдромы. В период ремиссии проявления острого миелоидного лейкоза исчезают. Рецидивы протекают аналогично периоду разгара. Терминальный период сопровождается прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика и лечение острого миелоидного лейкоза
Решающую роль в процессе диагностики играют лабораторные анализы. Используют анализ периферической крови, миелограмму, микроскопические и цитогенетические исследования. Для получения образца тканей выполняют аспирационную биопсию костного мозга (стернальную пункцию). В анализе периферической крови больного острым миелоидным лейкозом обнаруживается снижение количества эритроцитов и тромбоцитов. Количество лейкоцитов может быть как повышенным, так и (реже) пониженным. В мазках могут выявляться бласты. Основанием для постановки диагноза «острый миелоидный лейкоз» становится обнаружение более 20% бластных клеток в крови либо в костном мозге.
Основой лечения острого миелоидного лейкоза является химиотерапия. Выделяют два этапа лечения: индукцию и консолидацию (постремиссионную терапию). На этапе индукции выполняют лечебные мероприятия, направленные на уменьшение количества лейкозных клеток и достижение состояния ремиссии. На этапе консолидации устраняют остаточные явления болезни и предотвращают рецидивы. Лечебную тактику определяют в зависимости от вида острого миелоидного лейкоза, общего состояния больного и некоторых других факторов.
Наиболее популярная схема индукционного лечения – «7+3», предусматривающая непрерывное внутривенное введение цитарабина в течение 7 дней в сочетании с одновременным быстрым периодическим введением антрациклинового антибиотика в течение первых 3 дней. Наряду с этой схемой в процессе лечения острого миелоидного лейкоза могут применяться другие лечебные программы. При наличии тяжелых соматических заболеваний и высоком риске развития инфекционных осложнений в результате подавления миелоидного ростка (обычно – у больных старческого возраста) используют менее интенсивную паллиативную терапию.
Программы индукции позволяет добиться ремиссии у 50-70% пациентов с острым миелоидным лейкозом. Однако без дальнейшей консолидации у большинства больных наступает рецидив, поэтому второй этап лечения рассматривается, как обязательная часть терапии. План консолидационного лечения острого миелоидного лейкоза составляется индивидуально и включает в себя 3-5 курсов химиотерапии. При высоком риске рецидивирования и уже развившихся рецидивах показана трансплантация костного мозга. Другие методы лечения рецидивных ОМЛ пока находятся в стадии клинических испытаний.
Прогноз острого миелоидного лейкоза
Прогноз определятся разновидностью острого миелоидного лейкоза, возрастом больного, наличием или отсутствием миелодиспластического синдрома в анамнезе. Средняя пятилетняя выживаемость при разных формах ОМЛ колеблется от 15 до 70%, вероятность развития рецидивов – от 33 до 78%. У пожилых людей прогноз хуже, чем у молодых, что объясняется наличием сопутствующих соматических заболеваний, являющихся противопоказанием для проведения интенсивной химиотерапии. При миелодиспластическом синдроме прогноз хуже, чем при первичном остром миелоидном лейкозе и ОМЛ, возникшем на фоне фармакотерапии по поводу других онкологических заболеваний.
Хронический миелолейкоз - причины, симптомы, диагностика и лечение, прогноз
Хронический миелолейкоз – злокачественное миелопролиферативное заболевание, характеризующееся преимущественным поражением гранулоцитарного ростка. Может долгое время протекать бессимптомно. Проявляется склонностью к субфебрилитету, ощущением полноты в животе, частыми инфекциями и увеличением селезенки. Наблюдаются анемия и изменение уровня тромбоцитов, сопровождающиеся слабостью, бледностью и повышенной кровоточивостью. На заключительной стадии развиваются лихорадка, лимфоаденопатия и кожная сыпь. Диагноз устанавливается с учетом анамнеза, клинической картины и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
Общие сведения
Хронический миелолейкоз – онкологическое заболевание, возникающее в результате хромосомной мутации с поражением полипотентных стволовых клеток и последующей неконтролируемой пролиферацией зрелых гранулоцитов. Составляет 15% от общего количества гемобластозов у взрослых и 9% от общего числа лейкозов во всех возрастных группах. Обычно развивается после 30 лет, пик заболеваемости хроническим миелолейкозом приходится на возраст 45-55 лет. Дети до 10 лет страдают исключительно редко.
Хронический миелолейкоз одинаково распространен у женщин и у мужчин. Из-за бессимптомного или малосимптомного течения может становиться случайной находкой при исследовании анализа крови, взятого в связи с другим заболеванием или во время профилактического осмотра. У части больных хронический миелолейкоз выявляется на заключительных стадиях, что ограничивает возможности терапии и ухудшает показатели выживаемости. Лечение проводят специалисты в области онкологии и гематологии.
Хронический миелолейкоз
Этиология и патогенез хронического миелолейкоза
Хронический миелолейкоз считается первым заболеванием, при котором достоверно установлена связь между развитием патологии и определенным генетическим нарушением. В 95% случаев подтвержденной причиной хронического миелолейкоза является хромосомная транслокация, известная как «филадельфийская хромосома». Суть транслокации заключается во взаимной замене участков 9 и 22 хромосом. В результате такой замены формируется устойчивая открытая рамка считывания. Образование рамки вызывает ускорение деления клеток и подавляет механизм восстановления ДНК, что увеличивает вероятность возникновения других генетических аномалий.
В числе возможных факторов, способствующих появлению филадельфийской хромосомы у больных хроническим миелолейкозом, называют ионизирующее облучение и контакт с некоторыми химическими соединениями. Итогом мутации становится усиленная пролиферация полипотентных стволовых клеток. При хроническом миелолейкозе пролиферируют преимущественно зрелые гранулоциты, но аномальный клон включает в себя и другие клетки крови: эритроциты, моноциты, мегакариоциты, реже – В- и Т-лифоциты. Обычные гемопоэтические клетки при этом не исчезают и после подавления аномального клона могут служить основой для нормальной пролиферации кровяных клеток.
Для хронического миелолейкоза характерно стадийное течение. При первой, хронической (неактивной) фазе отмечается постепенное усугубление патологических изменений при сохранении удовлетворительного общего состояния. Во второй фазе хронического миелолейкоза – фазе акселерации изменения становятся явными, развиваются прогрессирующие анемия и тромбоцитопения. Заключительной стадией хронического миелолейкоза является бластный криз, сопровождающийся быстрой экстрамедуллярной пролиферацией бластных клеток. Источником бластов становятся лимфатические узлы, кости, кожа, ЦНС и т. д. В фазе бластного криза состояние больного хроническим миелолейкозом резко ухудшается, развиваются тяжелые осложнения, завершающиеся гибелью больного. У некоторых пациентов фаза акселерации отсутствует, хроническая фаза сразу сменяется бластным кризом.
Симптомы хронического миелолейкоза
Клиническая картина определяется стадией заболевания. Хроническая фаза в среднем продолжается 2-3 года, в некоторых случаях – до 10 лет. Для этой фазы хронического миелолейкоза характерно бессимптомное течение или постепенное появление «легких» симптомов: слабости, некоторого недомогания, снижения трудоспособности и чувства переполнения живота. При объективном осмотре больного хроническим миелолейкозом может обнаруживаться увеличение селезенки. По анализам крови выявляется повышение количества гранулоцитов до 50-200 тыс./мкл при бессимптомном течении заболевания и до 200-1000 тыс./мкл при «легких» признаках.
На начальных стадиях хронического миелолейкоза возможно некоторое снижение уровня гемоглобина. В последующем развивается нормохромная нормоцитарная анемия. При исследовании мазка крови пациентов с хроническим миелолейкозом отмечается преобладание молодых форм гранулоцитов: миелоцитов, промиелоцитов, миелобластов. Наблюдаются отклонения от нормального уровня зернистости в ту или иную сторону (обильная или очень скудная). Цитоплазма клеток незрелая, базофильная. Определяется анизоцитоз. При отсутствии лечения хроническая фаза переходит в фазу акселерации.
О начале фазы акселерации хронического миелолейкоза может свидетельствовать как изменение лабораторных показателей, так и ухудшение состояния пациентов. Возможно нарастание слабости, увеличение печени и прогрессирующее увеличение селезенки. У больных хроническим миелолейкозом выявляются клинические признаки анемии и тромбоцитопении или тробоцитоза: бледность, быстрая утомляемость, головокружения, петехии, кровоизлияния, повышенная кровоточивость. Несмотря на проводимое лечение, в крови пациентов с хроническим миелолейкозом постепенно увеличивается количество лейкоцитов. При этом отмечается возрастание уровня метамиелоцитов и миелоцитов, возможно появление единичных бластных клеток.
Бластный криз сопровождается резким ухудшением состояния больного хроническим миелолейкозом. Возникают новые хромосомные аномалии, моноклоновое новообразование трансформируется в поликлоновое. Отмечается нарастание клеточного атипизма при угнетении нормальных ростков кроветворения. Наблюдаются ярко выраженные анемия и тромбоцитопения. Суммарное количество бластов и промиелоцитов в периферической крови составляет более 30%, в костном мозге – более 50%. Пациенты с хроническим миелолейкозом теряют вес и аппетит. Возникают экстрамедуллярные очаги незрелых клеток (хлоромы). Развиваются кровотечения и тяжелые инфекционные осложнения.
Диагностика хронического миелолейкоза
Диагноз устанавливается на основании клинической картины и результатов лабораторных исследований. Первое подозрение на хронический миелолейкоз часто возникает при повышении уровня гранулоцитов в общем анализе крови, назначенном в порядке профилактического осмотра или обследования в связи с другим заболеванием. Для уточнения диагноза могут использоваться данные гистологического исследования материала, полученного при стернальной пункции костного мозга, однако окончательный диагноз «хронический миелолейкоз» выставляется при выявлении филадельфийской хромосомы при помощи ПЦР, флюоресцентной гибридизации или цитогенетического исследования.
Вопрос о возможности постановки диагноза хронический миелолейкоз при отсутствии филадельфийской хромосомы остается дискутабельным. Многие исследователи считают, что подобные случаи могут объясняться комплексными хромосомными нарушениями, из-за которых выявление данной транслокации становится затруднительным. В ряде случаев филадельфийскую хромосому можно обнаружить при использовании ПЦР с обратной транскрипцией. При отрицательных результатах исследования и нетипичном течении заболевания обычно говорят не о хроническом миелолейкозе, а о недифференцированном миелопролиферативном/миелодиспластическом расстройстве.
Лечение хронического миелолейкоза
Тактику лечения определяют в зависимости от фазы заболевания и выраженности клинических проявлений. В хронической фазе при бессимптомном течении и слабо выраженных лабораторных изменениях ограничиваются общеукрепляющими мероприятиями. Больным хроническим миелолейкозом рекомендуют соблюдать режим труда и отдыха, принимать пищу, богатую витаминами и т. д. При повышении уровня лейкоцитов используют бусульфан. После нормализации лабораторных показателей и уменьшения селезенки пациентам с хроническим миелолейкозом назначают поддерживающую терапию или курсовое лечение бусульфаном. Радиотерапию обычно используют при лейкоцитозе в сочетании со спленомегалией. При снижении уровня лейкоцитов делают паузу продолжительностью не менее месяца, а затем переходят на поддерживающую терапию бусульфаном.
В прогрессирующей фазе хронического миелолейкоза возможно использование одного химиопрепарата или полихимиотерапии. Применяют митобронитол, гексафосфамид или хлорэтиламиноурацил. Как и в хронической фазе, проводят интенсивную терапию до стабилизации лабораторных показателей, в последующем переходят на поддерживающие дозы. Курсы полиохимиотерапии при хроническом миелолейкозе повторяют 3-4 раза в год. При бластных кризах осуществляют лечение гидроксикарбамидом. При неэффективности терапии используют лейкоцитаферез. При выраженной тромбоцитопении, анемии выполняют переливания тромбоконцентрата и эритроцитарной массы. При хлоромах назначают радиотерапию.
Пересадку костного мозга проводят в первой фазе хронического миелолейкоза. Продолжительной ремиссии удается достичь у 70% пациентов. При наличии показаний осуществляют спленэктомию. Экстренная спленэктомия показана при разрыве или угрозе разрыва селезенки, плановая – при гемолитических кризах, «блуждающей» селезенке, рецидивирующих периспленитах и резко выраженной спленомегалии, сопровождающейся нарушением функций органов брюшной полости.
Прогноз хронического миелолейкоза
Прогноз при хроническом миелолейкозе зависит от множества факторов, определяющим из которых является момент начала лечения (в хронической фазе, фазе активации или в период бластного криза). В качестве неблагоприятных прогностических признаков хронического миелолейкоза рассматривают значительное увеличение печени и селезенки (печень выступает из-под края реберной дуги на 6 и более см, селезенка – на 15 и более см), лейкоцитоз свыше 100x109/л, тромбоцитопению менее 150x109/л, тромбоцитоз более 500х109/л, повышение уровня бластных клеток в периферической крови до 1% и более, повышение суммарного уровня промиелоцитов и бластных клеток в периферической крови до 30% и более.
Вероятность неблагоприятного исхода при хроническом миелолейкозе возрастает по мере увеличения количества признаков. Причиной гибели становятся инфекционные осложнения или тяжелые геморрагии. Средняя продолжительность жизни пациентов с хроническим миелолейкозом составляет 2,5 года, однако при своевременном начале терапии и благоприятном течении заболевания этот показатель может увеличиваться до нескольких десятков лет.
прогноз жизни, клинические рекомендации и анализ крови
Острый миелобластный лейкоз (ОМЛ) – это злокачественный процесс в костном мозге, нарушающий функцию кроветворения. Заболевание поражает миелоидный росток. Здоровая клетка лейкоцит не созревает и выходит в кровоток в изменённом виде. Начинается неконтролируемое деление. Лейкоциты лишены способности защищать организм от микроорганизмов и инфекций. Угнетается производство эритроцитов и тромбоцитов. Начинает развиваться анемия и тромбоцитопения. Изменяется состав периферической крови.
Причины, провоцирующие развитие болезни, до конца не изучены. Учёные связывают ряд факторов с мутациями кроветворной системы, к примеру, наследственность, облучения или генетические аномалии.
Миелоидная лейкемия наиболее часто диагностируется у взрослых пациентов. Болезнь поражает людей после 50 лет. Пик развития рака приходится на 63 года. Миелоидному лейкозу больше подвержены пожилые мужчины. Среди молодого поколения одинаково страдают представители обоих полов.
У детей заболевание носит первичный характер. Ребёнок подвергается лейкозу при аномалиях в генетическом коде, при контакте матери с тяжёлыми отравляющими веществами (радиация, канцерогены) или если история болезней кровных родственников содержит онкологические патологии. Симптомы болезни как у взрослых.
В начале заболевания клиническая картина смазана. Постепенно больной замечает необычные изменения в состоянии. При остром течении болезни пациент отмечает симптомы самочувствия:

- Утомляемость;
- Одышка;
- Синяки и мелкие кровоподтеки;
- Кровоточивость слизистой ротовой полости;
- Инфекционные поражения организма, не поддающиеся классическому лечению и имеющие ярко выраженную симптоматику.
Для лейкозов терминальной стадии развития костный мозг лишается работоспособности, метастазы поражают органы и системы человеческого тела. Для этого характерны признаки:
- Значительное снижение веса;
- Бледность кожных покровов;
- Желудочно-кишечные и носовые кровотечения;
- Слабость;
- Боль и ломота в костях;
- Обмороки;
- Рвота с кровью;
- Чёрный стул;
- Боли в животе;
- Если поражается мочеполовая система, отмечается частичная или полная задержка мочи.
Лечением занимаются онкогематологи. Код по МКБ-10 миелолейкоза С92.
Классификация онкологической патологии
Нелимфобластный лейкоз представляет группа подвидов болезни. Для каждого вида шансы выживаемости и тактика лечения подбираются индивидуально.
Система ФАБ состоит из 9 разновидностей острого миелоидного лейкоза. Формы отличаются по типам предшественников лейкоцитов и степеням их зрелости. Клетки определяют при проведении микроскопического и цитогенетического исследования.

Клетки крови при тысячекратном увеличении
- Показатель М0 означает минимально-дифференцированную острую миелоидную лейкемию.
- М1 характеризует миелоцитарный лейкоз без созревания. В единичных бластах обнаруживаются азурофильные гранулы и палочки Ауэра.
- При М2 для лейкоза характерно созревание. Бласты преимущественно с палочками Ауэра и азурофильными гранулами.
- М3 обозначает острую форму промиелоцитарного рака крови. Клетки гипергранулированы. Палочки Ауэра присутствуют множественно.
- М4 представляет острый миеломонобластный онкологический процесс.
- При М4ео наблюдается миеломоноцитарная патология с повышенным уровнем эозинофилов в костном мозге.
- М5 определяет острый монобластный (-цитарный) лейкоз.
- М6 характеризует острые эритроидные заболевания крови.
- М7 означает мегакариобластную лейкемию.
- Подвид М8 представляет базофильное малокровие.
Исследования при лейкозах
Диагностика лейкозов заключается в изучении состава крови и костного мозга. Точный диагноз определяется только после забора биоптата из бедра или ребра для дальнейшего исследования.
Вначале проводят анализ крови. Наблюдаются отклонения в показателях лейкоцитов. Результат может быть представлен от 0,1*109/л до 10*100*109/л. Небольшие нарушения свидетельствуют о монобластной лейкемии или о эритромиелозе. В сыворотке крови не обнаруживаются базофилы. Скорость оседания эритроцитов (СОЭ) увеличена.
Эритроциты представлены низкими показателями. В крови преобладают бласты и клетки зернистого ряда. Отмечаются созревшие моноциты. Снижен уровень гемоглобина.
С помощью биохимического исследования определяется количество общего белка, билирубина, альбумина, мочевины и креатинина.

Для острого лейкоза первой фазы анализ крови может иметь следующую картину:
- Показатели общего белка – 78 ммоль/л.
- Общего билирубина – 14-17 ммоль/л.
- Прямого билирубина – 3,5-4,5 ммоль/л.
- Уровень креатинина – 108 мкмоль/л.
Благодаря цитохимическим показателям изучается активность ферментов, состав крови, костного мозга и других тканей организма.
Иммунологический тест является комплексным исследованием нарушений в работе иммунитета. Для анализа используют венозную кровь. Определяются иммунные клетки, их функции, активность и способность уничтожать бактерии.
Для выявления метастазов в миокарде используют электрокардиограмму и эхокардиографию.
Ультразвуковая диагностика выявляет отклонения во внутренних органах человека. Метод позволяет изучить печень, органы желудочно-кишечного тракта и мочеполовой системы, лимфатические узлы.
Вариант глобальной диагностики всех органов и систем представлен проведением магнитно-резонансной и компьютерной томографии. Методы послойно сканируют участки тела. Выявляются даже незначительные изменения в тканях.
Лечебная тактика
Лечение проводится в стационарных условиях, где снижается контакт с окружающим миром. Клинические рекомендации заключаются в проведении химиотерапии. Онкогематолог выбирает соответствующий протокол для каждого случая. При диагнозе «Острый миелобластный лейкоз» врачи подбирают комбинацию препаратов. Интенсивная химиотерапия помогает вылечиться и войти в стойкую ремиссию.
Проведение процедуры химиотерапии
На первом этапе лечения назначенные препараты без разбора убивают здоровые и раковые клетки. Развиваются побочные явления:
- Тошнота;
- Рвота;
- Вялость;
- Язвенные поражения полости рта;
- Назальные кровотечения;
- Организм больного подвержен присоединению опасных инфекций.
На втором этапе назначают несколько курсов цитостатиков. Для уничтожения рака важен приём высокой дозы цитозин-арабинозида. Препарат препятствует созданию частиц, переносящих наследственную информацию. При печёночной и почечной недостаточностях или угнетении костного мозга приём препарата запрещен.
Для угнетения функций костного мозга и борьбы с опухолевыми клетками назначают Идарубицин.
Митоксантрон подавляет иммунитет и уничтожает опухоли.
Для достижения максимальной эффективности используют протоколы с тремя блоками постремиссионной химии.
Прогноз жизни на фоне химиопрепаратов значительно улучшается.
При поражении органов центральной нервной системы рекомендована лучевая терапия. Ионизирующее излучение вступает в реакцию с аномальными клетками, нарушает их структуру и провоцирует гибель.
Среди людей ходят истории об исцелении рака крови с помощью народной медицины. Однако ни один метод или препарат не показал 100% эффективности. Отказываясь от врачебного вмешательства, больной позволяет лейкозу стремительно развиваться и нарушать работу жизненно важных органов! Лечением может заниматься только квалифицированный врач онколог после проведения тщательной диагностики. Нетрадиционные методы обычно только усугубляют течение болезни.
Полное выздоровление наступает после пересадки костного мозга. Метод имеет нюансы и последствия:
- До начала проведения операции (вливание донорского материала через установленный в артерию катетер) больному уничтожают костный мозг с помощью ударных доз химиотерапии.
- При отсутствии иммунитета любые инфекции и болезни, к примеру, ОРЗ или царапина могут привести к летальному исходу.
- Трансплантируемый материал может не взаимодействовать с организмом пациента:
- В первом случае чужой костный мозг организм человека воспринимает за чужеродный и отторгает его. Нарушается работа всех органов. Иммунные клетки убивают все на своем пути. Однако при этом окончательно уничтожаются раковые клетки без возможности развиться снова. Иммуносупрессивная терапия помогает наладить нормальный кроветворный процесс.
- Организм пациента отвергает введенные стволовые клетки. Иммунитет не формируется. Выработка кровяных телец не начинается.
- При введении биоматериала развивается аллергия или анафилактический шок.
- Половина пациентов умирают в первый месяц после операции.
Пересадка костного мозга
Подходящий костный мозг трудно достать. Лучшими донорами являются однояйцевые близнецы, родные братья и сестры. Материал родителей подходит очень редко.
Стволовые клетки могут быть взяты у самого пациента в период ремиссии или у постороннего человека.
Прогнозы на жизнь
Шанс на полное выздоровление имеют 90% пациентов до 60 лет. Пожилой организм не справляется с раком и нагрузками при химиотерапии. Пациент до конца жизни использует паллиативное лечение. Пятилетняя выживаемость пожилых людей составляет 12-25%.
Шанс на выживаемость снижается при наличии сопутствующих онкологических проблем или заболеваний генетического типа (болезнь Дауна). Рецидив развивается в любой момент. Вторичное заболевание не поддаётся лечению.
Если больной в течение 5 лет не отмечал симптомы лейкоза и не обращался за помощью, его снимают с онкологического учёта и считают здоровым.
Специфическая профилактика лейкемии отсутствует.
что это такое? Хронический миелоидный лейкоз: причины, лечение, прогноз
Развитие опухолевых процессов с каждым годом набирает обороты. Большинство ученых мира изучают возможные факторы развития состояния и основные методы терапии для излечения пациентов, а профилактическими мероприятиями занимаются все виды лечебных учреждений. Развитие опухолевого процесса может коснуться любого органа или системы организма. Миелолейкоз – что это такое? Основные причины этого заболевания, методы диагностики и терапии рассмотрим далее.
Общие понятия
Система кроветворения основывается на созревании молодых клеток – тромбоцитов, эритроцитов и лейкоцитов в костном мозге. Параллельно с этим процессом происходит уничтожение старых клеток печенью и селезенкой.
Форменных элементов в крови столько же, сколько и плазмы. При этом самое большое количество приходится на белые кровяные клетки – лейкоциты. Они отвечают за реакцию организма на воздействие чужеродных агентов и соединений и позволяют поддерживать иммунную систему на должном уровне.
Неконтролируемая выработка большого количества лейкоцитов называется миелоидным лейкозом. Это опухолевое заболевание, которое сопровождается критическим увеличением в кровеносном русле незрелых форм. Со временем происходит распространение патологических форм клеток во все органы и системы организма, что вызывает прогрессирование болезни.
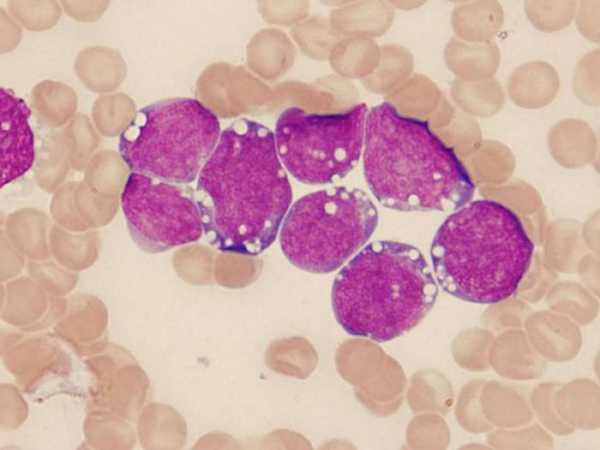
Этиология заболевания
На данном этапе однозначные факторы, приводящие к развитию заболевания, не определены. Существует несколько версий возникновения патологического состояния:
- Появление патологических клонов – это процесс развития патологических изменений в структуре стволовых клеток. Происходит мутация, во время которой клетки не только приобретают изменения в себе, но и передают их остальным структурам, создавая свои клоны. Это состояние излечить с помощью цитостатических препаратов невозможно.
- Воздействие химических веществ.
- Действие радиоактивного излучения на организм, которое происходит не только по профессиональной необходимости. Например, использование в анамнезе лучевой терапии для лечения другой опухоли.
- Прием цитостатиков и химиотерапевтических препаратов для терапии опухолей других органов может послужить пусковым механизмом развития миелолейкоза.
- Генетические заболевания, наследственность.
- Болезни, имеющие вирусный генез.

Кроме того, на появление опухолевого процесса влияют пол, возраст пациента и воздействие радиационного облучения в зоне проживания.
Хроническая форма болезни
Проявление симптоматики опухолевого процесса крови зависит от формы болезни. Наиболее распространенная форма – хронический миелоидный лейкоз. Это состояние имеет злокачественный характер.
Хронический миелолейкоз – что это такое? Это состояние, которое возникает вследствие того, что в организме появляется аномальный ген, который поражает кровяные клетки. Место локализации гена – костный мозг. С током крови происходит распространение патологических клеток по всем органам.
Заболевание не имеет острого начала и яркой клинической картины. Для него характерно медленное течение. Опасность состоит в том, что эта форма болезни может перейти в острую фазу в любой период, что может закончиться летальным исходом для пациента.
Миелоидный лейкоз имеет несколько стадий развития:
- хроническая;
- стадия акселерации;
- терминальная стадия.
Первая стадия хронической формы
Большинству пациентов ставят диагноз именно в этой стадии. Начало заболевания точно определить невозможно, поскольку оно имеет бессимптомный характер или легкие проявления. Сначала появляется утомляемость, тяжесть в желудке или в левом подреберье, одышка.
Во время приема пищи пациенты жалуются на чувство переполненности в эпигастрии. Пальпаторно ощущается увеличение селезенки. Осмотр сопровождается болезненными ощущениями со стороны селезенки, иррадиирущими в спину. В анализе крови определяется лейкоцитоз, нарастающий в динамике, а также тромбоцитоз и увеличение количества гранулоцитов.
Часто больные обращаются к врачу при развитии инфаркта селезенки. Появляется резкий болевой синдром в ее проекции, симптомы интоксикации организма, повышается температура тела.
Стадия акселерации
В этой стадии заболевание практически не имеет проявлений. У больного нет жалоб, кроме периодического подъема температуры до субфебрильных показателей и усталости. Продолжает увеличиваться уровень миелоцитов и лейкоцитов в крови.
Уровень базофилов увеличивается на треть. После этого больных начинает беспокоить чувство жара и желание чесаться. Это связано с увеличением выработки гистамина.
Острая стадия (терминальная)
Развитие третьей стадии описывает клиническую картину, схожую с острым течением болезни. Хронический миелоидный лейкоз прогрессирует, и появляется яркая клиническая картина. Пациенты жалуются на такие проявления:
- резкая слабость;
- высокая температура тела;
- боли в суставах;
- резкое уменьшение веса больного.
При обследовании пациента можно обнаружить увеличение различных групп лимфатических узлов, печени, селезенки, развитие геморрагического синдрома. Бластный криз – финальная стадия болезни, которая характеризуется следующими клиническими проявлениями:
- лимфо- или миелобластов становится больше на 20 % в костном мозге или кровеносном русле;
- биопсия костного мозга определяет большие группы бластов;
- развитие миелоидной саркомы – злокачественной опухоли из незрелых белых клеток крови.

На этой стадии заболевания жизнь пациента зависит исключительно от уровня паллиативной терапии.
Острый миелоидный лейкоз
Клиническая картина развивается быстро, имеет яркие признаки заболевания. Без назначения адекватной терапии результат может быть неблагоприятным уже по истечении нескольких недель или месяцев.
Острый миелолейкоз – что это такое? Это злокачественный опухолевый процесс миелоидного ростка крови. Больные клетки не способны противостоять инфекциям, хотя это является их основной функцией. Параллельно с увеличением бластных структур происходит уменьшение остальных форменных элементов крови.
Эритропения и недостаток гемоглобина проявляются бледностью кожных покровов, одышкой, усталостью. Снижение количества тромбоцитов приводит к увеличению склонности кожи к повреждениям, повышенной кровоточивости, появлению петехий и гематом.
Первые симптомы не являются специфичными. Очень легко перепутать их с проявлениями респираторной вирусной инфекции. Кроме того, острый миелолейкоз сопровождается прогрессированием болевых ощущений в костях и суставах.
Диагностические мероприятия
Успешность начала лечения зависит от скорости проведения диагностики и постановки правильного диагноза. Чтобы определить общее состояние и фазу заболевания пациента, у которого подозрение на миелолейкоз, анализы проводятся в следующих направлениях:
- Анализ периферической крови развернутый – фиксируется уровень всех форменных элементов крови в динамике.
- Биохимия крови показывает нарушения в работе печени и селезенки, которые вызваны развитием болезни.
- Биопсия костномозгового аспирата проводится после забора необходимого материала из бедренной кости. Определяется наличие бластных форм.
- Гибридизация позволяет определить мутационную или аномальную хромосому.
- ПЦР направлена на выявление аномального гена.
- Цитогенетические анализы направлены на определение аномальной хромосомы в лейкозной клетке.
- По необходимости проводится компьютерная томография, магнитно-резонансная томография и ультразвуковое исследование.
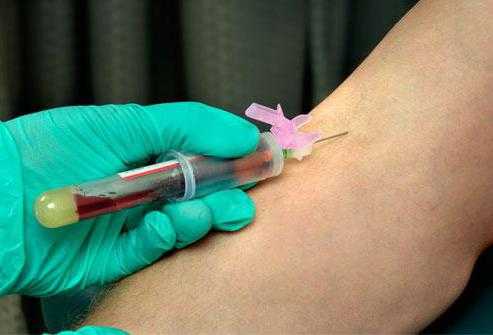
Принципы терапии заболевания
Миелоидный лейкоз требует безотлагательного начала лечения. Врач-онколог определяет схему терапии, исходя из стадии заболевания, его проявлений. На ранней стадии назначается витаминная диета, общеукрепляющие препараты.
Лечение миелолейкоза основывается на применении препаратов, способных угнетающе действовать на онкоген. Основные средства:
- «Иматиниб» - средство угнетает активность белка, который вырабатывается онкогеном миелолейкоза;
- «Дазатиниб» - препарат используется в случае неэффективности или непереносимости пациентом «Иматиниба»;
- «Нилотиниб» - средство с аналогичным действием, относящееся ко второму поколению онкогенных ингибиторов;
- «Понатиниб» - один из новых препаратов, сильный по своей эффективности против бластных клеток, но способен вызывать тяжелые осложнения со стороны организма больного.
Также для укрепления иммунной системы пациентам назначается прием «Интерферона». Препарат не способен самостоятельно справиться с заболеванием, однако его применяют в комплексной терапии в виде ежедневных подкожных инъекций.
Химиотерапия проводится с использованием цитостатических средств. Эту часть терапии используют как дополнительное лечение при трансплантации клеток костного мозга. Эффективными считаются «Гидроксикарбамид», «Бусульфан», «Винбластин», «Винкристин», «Цитарабин».
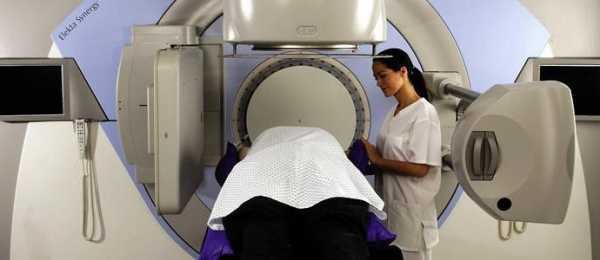
Облучение при онкологии проводится при помощи высокоэнергетических лучей, а также их частиц. Применяется индивидуально, в зависимости от необходимости. При миелолейкозе лучевая терапия используется для уменьшения болевых синдромов в костях и суставах. Также облучение при онкологии кроветворной системы используют перед трансплантацией костного мозга.
Трансплантация клеток костного мозга
Хирургическое вмешательство является довольно распространенным методом лечения, но при этом дорогостоящим. Не каждый пациент в состоянии себе это позволить. Онкоцентр на Каширке – один из знаменитых институтов терапии опухолевых новообразований – проводит подобные оперативные вмешательства, помогая излечиться своим пациентам.
Пересадка самого костного мозга сейчас используется не так часто, как трансплантация стволовых клеток, которые берут из периферической крови. Существуют два варианта проведения процедуры:
- Используют гемопоэтические клетки костного мозга донора. Это может быть кто-то из родственников, поскольку достаточно тяжело найти подходящего донора, который не состоял бы в родственных связях с больным.
- Пересадка собственных периферических клеток. Эта процедура сложна тем, что вместе со здоровыми клетками могут быть изъяты и бластные.
Онкоцентр на Каширке не только проводит хирургические вмешательства, которые позволили снизить смертность пациентов, но и использует современные методы термоаблации, криотермоаблации и радиоволновой хирургии.
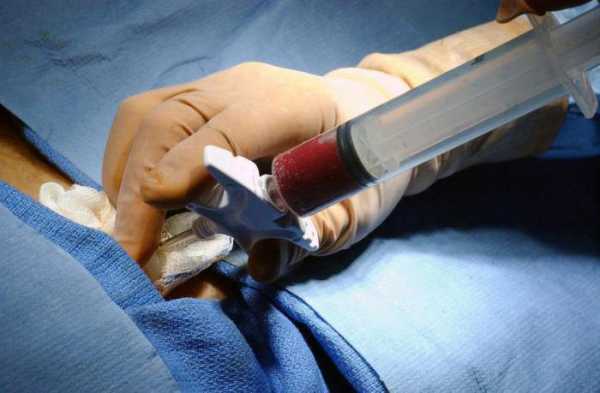
Заключение
В статье был рассмотрен термин «миелолейкоз». Что это такое, вам теперь известно. Благоприятный исход возможен при полном курсе лечения начальных стадий заболевания. Терминальная стадия предполагает исключительно паллиативную терапию. Поздние и злокачественные стадии болезни приводят к летальному исходу у пациентов.
Острый миелоидный лейкоз (ОМЛ), что это такое и как он развивается?
Острый миелоидный лейкоз (ОМЛ или миелолейкоз, как может быть указано в истории болезни пациента) – одна из многочисленных разновидностей онкологических поражений крови, провоцирующей нарушения нормального кроветворения. При этом заболевании эмбриональные кроветворные клетки, получившие способность к дальнейшему функционированию в форме лейкоцитов, по какой-либо причине останавливаются в своём развитии. Возникновение миелоидного лейкоза острой формы очень опасно необратимыми изменениями крови и высокой смертностью.
Возникновение патологического состояния имеет непосредственную связь с возникновением процесса мутации на одном из участков гемопоэза (кроветворения), происходящего в костном мозге. Острый миелоидный лейкоз, онкология, которую пациенты не совсем правильно называют «рак крови», ведь раковые структуры локализуются в основном в эпителиальных тканях, поражает гранулоциты, являющиеся подгруппой лейкоцитов, содержащих крупные ядра и цитоплазму, имеющую зернистую структуру. Эта разновидность белых кровяных телец, вследствие воздействия на них поражающего фактора, теряет способность к созреванию и естественному самоуничтожению через определённое время, присущую нормальным элементам крови.
Результатом патологического процесса становится:
- поступление в кровяное русло незрелых клеток, бластов, не несущих никакой функциональной значимости;
- активное деление этих элементов, приводящее к быстрому их разрастанию и вытеснению здоровых белых клеток крови;
- снижение и полная потеря организмом защитных функций, в результате чего он становится уязвим перед любым инфекционным поражением.
Увеличение количества бластов в кровеносном русле имеет очень большую скорость, поэтому от начала зарождения острого миелоидного лейкоза проходит короткий период времени. В некоторых случаях бывает достаточно нескольких недель от появления первой мутировавшей клетки крови, до того момента, когда острый лейкоз миелоидного типа становится неизлечимым. Высокая смертность от этого заболевания связана с необратимостью процесса изменения структуры клеток, его большой скоростью и появлению в них резистентности к терапевтическому воздействию.
Острый миелоидный лейкоз у детей
Это заболевание у детей встречается сравнительно редко, но всё-таки некоторые малыши подвержены риску его возникновения. Острый миелоидный лейкоз диагностируется в основном у крошек до трёхлетнего возраста, с одинаковой частотой у мальчиков и девочек.
Такая тенденция свидетельствует о том, что большую роль в возникновении патологий кроветворных органов играет генетический фактор:
- у малышей до 3-х лет ярко проявляются все наследственные патологии, способные привести к развитию онкологического поражения кроветворных элементов.
- в более старшем возрасте, от трёх до семи лет, их влияние значительно снижается и в то же время отсутствуют приобретённые патологические процессы, способные привести к онкопоражению миелоидного ростка.
Стоит знать! По достижению ребёнком семилетнего возраста у него снова возрастают риски заболеть острой формой миелоидного лейкоза. Чаще всего это заболевание диагностируют у малышей, подрастающих у курящих и выпивающих родителей. Также острый лейкоз миелоидного типа развивается у детей, проживающих в плохих экологических условиях (рядом с крупными промышленными предприятиями или атомными электростанциями).
Классификация онкологической патологии крови
Для более точного выявления разновидности онкозаболевания, помогающей подобрать оптимальный курс терапии, острый лейкоз миелоидного типа принято классифицировать. Подразделение патологического состояния на типы происходит в соответствии с наиболее значимыми с прогностической точки зрения признаками развивающегося заболевания.
Общепринятая при этом недуге классификация ВОЗ включает 7 вариантов течения ОМЛ:
- Миелобластный лейкоз, развивающийся при полном отсутствии признаков созревания в бластных клетках.
- Острый миелобластный лейкоз (ОМЛ) с неполной зрелостью клеточных элементов, давших ему начало.
- Промиелобластный (промилеоцитарный) лейкоз. При этой форме патологии мутации подвергаются промиелоциты, клетки, предшествующие появлению гранулоцитов.
- Миеломонобластный. В кровеносном русле преобладают бластные, эпителиальные клетки. Уровень начавших созревать и полностью созревших белых кровяных телец не достигает 10% от общего количества лейкоцитов.
- Монобластный. Основная масса крови заполнена клетками, получившими статус зернистых лейкоцитов, но мутировавших, так и не наяав функционировать в естественной для них роли.
- Мегакариобластный. Один из редких вариантов острого миелоидного лейкоза, который всегда развивается и прогрессирует одновременно с фиброзом костного мозга, что должно учитываться при подборе лечебной тактики.
- Эритролейкоз (острый синдром Ди Гульельмо). Самый редкий тип онкологического поражения крови, характеризующийся малигнизацией эритробластов.
Причины появления острого миелоидного лейкоза
Вопрос о том, почему становится возможным развитие в кроветворных органах процесса малигнизации, поражающего белые кровяные тельца с зернистой структурой, до сих пор не потерял среди специалистов своей актуальности. Непосредственные причины возникновения ОМЛ кроются в хромосомных нарушениях клетки, но почему они возникают, на сегодняшний день остаётся для гематоонкологов загадкой. Единственное, что специалисты могут с точностью утверждать, это существование определённой группы факторов риска, увеличивающих шансы человека на то, что в его кровеносной системе сможет развиться острый миелоидный лейкоз.
Среди основных предпосылок, способных вызвать у человека развитие опасного заболевания, особое место занимают:
- Повышенный уровень радиационного излучения. Для каждого человека опасная граница воздействующей радиации может быть разной, что связано с восприимчивостью его организма к ионизирующим лучам.
- Непосредственный длительный контакт (обычно для развития заболевания хватает 1-5 лет) с химическими веществами и токсинами, как на производстве, так и в быту. Данный фактор провоцирует развитие аплазии (уничтожения) части костного мозга, приводящей к продуцированию оставшейся кроветворной тканью неполноценных клеток.
- Употребление в превышающих допустимую дозу количествах некоторых лекарственных препаратов. Особую опасность представляют цитостатики. Также риск представляет банальный, знакомый всем с детства Аспирин и некоторые антибиотики, употребляемые бесконтрольно.
- Длительное воздействие на организм человека вирусов гриппа или герпеса. Эти патологические микроорганизмы способны спровоцировать в бластных клетках костного мозга начало процесса мутации.
Стоит знать! Острый лейкоз миелоидного типа очень часто диагностируется, если в анамнезе пациента имеются такие заболевания, как синдромы Дауна и Блума, а также анемия Фанкони. Но даже при отсутствии этих генетических патологий наследственный фактор риска развития симптомов острого миелоидного лейкоза очень высок. Если среди кровных родственников предыдущих поколений отмечались онкопатологии кровеносной системы, шансы на то, что их потомки пострадают от острого лейкоза, повышаются в несколько раз.
Как проявляется острый миелоидный лейкоз и какие симптомы его сопровождают?
Все негативные проявления, способные подсказать, что у человека поражены кроветворные структуры костного мозга и начал развиваться острый миелоидный лейкоз, спровоцированы недостатком здоровых, полностью созревших лейкоцитов, тромбоцитов и эритроцитов. Симптомы онкопатологии такого типа, вызванной исчезновением кровяных телец, которых не коснулась мутация, и замещением их аномальными, не способными к естественному функционированию, клетками крови, выражаются в следующем:
- постоянно преследующая человека усталость, не связанная с каким-либо физическим напряжением;
- анемия, выражающаяся в бледности кожных покровов;
- появление следов подкожных кровоизлияний и синяков без механического воздействия;
- нарушение терморегуляции тела, повышенная потливость или ознобоподобный синдром, не связанные с окружающей температурой;
- частые кровотечения, как внешние, так и внутренние, длительное заживление воспалительных повреждений слизистой и незначительных ранений кожи.
Эти негативные симптомы появляются неожиданно, и активно прогрессируют. Часто первым врачом, заподозрившим острый миелоидный лейкоз, становится терапевт или стоматолог, к которым пациент обращается с такими жалобами. Нередко первые симптомы болезни полностью неспецифичны и напоминают обычную простуду с той лишь разницей, что длительное время не поддаются купированию, несмотря на применение лучших медикаментозных препаратов.
На последних стадиях о протекании в кроветворных органах острого миелоидного лейкоза говорит увеличение лимфатических узлов, располагающихся на разных участках тела, также может увеличиться селезёнка или печень и появиться механическая желтуха.
Диагностика: анализы крови и инструментальная диагностика
Выявить это заболевание крови достаточно сложно, т. к. его симптомы зачастую настолько неспецифичны, что не вызывают у человека какой-либо тревоги и он не торопится посетить врача, провоцируя тем самым прогрессирование болезни и переход её в финальную, не поддающуюся излечению стадию. Обычно острый миелоидный лейкоз становится случайной находкой при проведении профилактического обследования или выявлении другого заболевания. Если у специалиста появилось подозрение на развитие болезни, пациента направляют к гематоонкологу, чтобы подтвердить или опровергнуть диагноз.
Назначается специфическая диагностика лейкоза, которая включает:
- Анализ крови, позволяющий выявить изменение количественного состава кровяных телец и обнаружить наличие повреждённых зернистых лейкоцитов.
- Гистология костного мозга. Биопсийный материал, предназначенный для дальнейшего исследования, берётся из тазовых костей с помощью специальной иглы.
Дополнительно, для выявления характера злокачественного поражения крови, позволяющего уточнить диагноз, проводится инструментальная диагностика – УЗИ, КТ или МРТ. С помощью этих диагностических методик возможно выявление распространённости опухолевого процесса и наличия вторичных злокачественных поражений, локализованных во внутренних органах.
Методы лечения миелоидного лейкоза – медикаментозная терапия (препараты выбора), хирургическое вмешательство и народные рецепты
Терапия при острой миелоидной форме лейкоза состоит из нескольких направлений. Для достижения лучшего результата, лечение заболевания крови проводится с применением различных процедур, подбираемых исходя из характера онкопоражения и общего состояния пациента.
Общая схема лечения опасного заболевания включает следующие мероприятия:
- Химиотерапия. Золотой стандарт, с помощью которого проводится лечение не только острого миелолейкоза, но и других злокачественных поражений крови. Для медикаментозного лечения, направленного на разрушение злокачественных клеток крови, применяют Цитарабин и Даунорубицин (в/в введение), а последующую поддерживающую терапию проводят Рубомицином или Бтиогуанином. Все курсы и схемы введения препаратов подбираются индивидуально, исходя из медицинских показаний каждого конкретного пациента.
- Трансплантация стволовых клеток. Пересадка тканей костного мозга от здорового донора считается в клинической практике гематоонкологов самым эффективным методом терапии, в большинстве случаев приводящим больного человека к полному выздоровлению.
- Облучение. Этот метод лечения практикуется в терапии онкопоражений крови давно, но до сих пор не приобрёл популярности, что связано с его негативным воздействием на организм человека. В клинической практике отмечается высокая смертность пациентов с онкологией кроветворных органов после проведения курсов лучевой терапии.
Прогноз на выздоровление при злокачественном поражении крови
При остром миелоидном лейкозе онкогематологи дают обычно условно неблагоприятный прогноз, т. к. это заболевание крови обладает повышенным коварством и сложно поддаётся выявлению.
Исходя из статистических данных, прогноз при остром миелоидном лейкозе выглядит следующим образом:
- Среди детей, у которых заболевание выявлено своевременно и проводится адекватное лечение, полное выздоровление наступает в 60% клинических случаев.
- Среди взрослых пациентов наступление длительной ремиссии отмечается только в 35% случаев.
- У пожилых людей старше 60 лет, имеющих в анамнезе острый миелоидный лейкоз, лечение обычно оказывается безрезультативным, поэтому шансы на продление жизни дольше 2-3 лет имеются только у 10% пациентов.
Стоит знать! При отсутствии лечебных мероприятий прогноз неутешительный – человек умирает через несколько недель после выявления острого лейкоза миелоидного типа. Самый большой срок жизни в этом случае составляет 5-6 месяцев. Народное лечение при этом заболевании не практикуется, т. к. не имеет результативности. Всё, чего можно добиться с помощью лечения отварами из трав – это снизить проявление мучительной симптоматики, но применять такую терапию самостоятельно, без согласования с лечащим врачом, категорически недопустимо.
Профилактика миелоидного лейкоза
К сожалению, предотвратить развитие этого заболевания не представляется возможным, так как специфических профилактических мероприятий, позволяющих избежать развития патологического состояния, не существует. Но любой человек, у которого диагностирован острый миелоидный лейкоз, может добиться увеличения шансов на жизнь.
Всё, что для этого требуется, это соблюдение после проведённой терапии некоторых правил:
- обязательное плановое посещение врача для прохождения профилактической диагностики;
- недопустимость смены места жительства с изменением климатических условий;
- запрет на любые физиопроцедуры.
При соблюдении этих правил у человека появляются шансы избежать рецидива заболевания и, соответственно, достигнуть условного выздоровления, когда стадия ремиссии может продолжаться до глубокой старости.
что это такое, анализ крови,симптомы и лечение миелоидной саркомы
Острый миелоидный лейкоз (ОМЛ) начинается в костном мозге (мягкой внутренней части определенных костей, где образуются новые клетки крови), но чаще всего он также быстро распространяется и на периферическую кровь. Иногда он может распространяться на другие части тела, включая лимфатические узлы, печень, селезенку, центральную нервную систему (головной и спинной мозг) и яички. Чаще всего ОМЛ развивается из клеток, которые превращаются в лейкоциты (кроме лимфоцитов), но иногда ОМЛ развивается в других типах кроветворных клеток.
Оглавление: Нормальный костный мозг, кровь и лимфатическая ткань Миелобластный лейкоз: что это такое? Генетика ОМЛ Факторы риска острого миелоидного лейкоза (ОМЛ) Развитие миелолейкоза Признаки и симптомы острого миелоидного лейкоза (ОМЛ) Симптомы, вызванные распространением лейкемии Диагностика миелолейкоза - Исследования костного мозга - Исследование цереброспинальной жидкости - Лабораторные тесты, используемые для диагностики и классификации ОМЛ - Визуализационные тесты при МЛ 9. Лечение миелоидной саркомы: химиотерапия - Побочные эффекты 10. Таргетные препараты для лечения острого миелоидного лейкоза (ОМЛ) 11. Хирургия острого миелоидного лейкоза (ОМЛ) 12. Лучевая терапия при остром миелобластном лейкозе (ОМЛ) 13. Трансплантация стволовых клеток при остром миелолейкозе (ОМЛ)
Обратите внимание
Острый миелоидный лейкоз (ОМЛ) имеет много других названий, в том числе острый миелоцитарный лейкоз, острый миелобластный лейкоз, острый гранулоцитарный лейкоз и острый нелимфоцитарный лейкоз.
Нормальный костный мозг, кровь и лимфатическая ткань
Чтобы понять развитие лейкоза, нужно узнать о крови и лимфатической системе. Костный мозг — мягкая внутренняя часть определенных костей. Он состоит из кроветворных клеток, жировых клеток и поддерживающих тканей. Небольшая часть кроветворных клеток — это стволовые клетки крови. Внутри костного мозга стволовые клетки крови развиваются в новые зрелые клетки крови. Во время этого процесса клетки становятся либо лимфоцитами (разновидностью лейкоцитов), либо другими кроветворными клетками, которые являются типами миелоидных клеток. Миелоидные клетки могут развиваться в эритроциты, лейкоциты (кроме лимфоцитов) или тромбоциты. Эти миелоидные клетки являются аномальными при ОМЛ.
Существует 3 основных типа клеток крови:
- Красные кровяные клетки (эритроциты) переносят кислород из легких во все другие ткани организма и возвращают углекислый газ в легкие.
- Тромбоциты представляют собой фрагменты клеток, образованные костным мозгом, называемые мегакариоцитами. Тромбоциты важны для остановки кровотечения. Они помогают закупорить отверстия в кровеносных сосудах, вызванные порезами или ушибами.
- Белые кровяные клетки помогают организму бороться с инфекциями. Существуют разные типы белых клеток крови:
- Гранулоциты — это зрелые лейкоциты, которые развиваются из миелобластов, типа кроветворных клеток в костном мозге. У гранулоцитов есть гранулы, которые обнаруживаются как пятна под микроскопом. Эти гранулы содержат ферменты и другие вещества, которые могут уничтожать бактерии. 3 типа гранулоцитов — нейтрофилы, базофилы и эозинофилы — различаются по размеру и цвету своих гранул.
- Моноциты — это лейкоциты, которые развиваются из кроветворных монобластов в костном мозге. После циркуляции в кровотоке в течение примерно одного дня моноциты попадают в ткани организма, превращаясь в макрофаги, которые могут уничтожать некоторые микробы, окружая и переваривая их. Макрофаги также помогают лимфоцитам распознавать микробы и вырабатывать антитела для борьбы с ними.
- Лимфоциты — это зрелые лейкоциты, которые развиваются из лимфобластов в костном мозге. Лимфоциты — это клетки, из которых состоит лимфатическая ткань, основная часть иммунной системы. Лимфатическая ткань находится в лимфатических узлах, тимусе (небольшой орган за грудиной), селезенке, миндалинах и аденоидах, плюс ее участки разбросаны по всей пищеварительной и дыхательной системе и костном мозге. Есть 2 основных типа лимфоцитов — это В-клетки и Т-клетки.
Миелобластный лейкоз: что это такое?
МЛ является одним из наиболее распространенных видов лейкемии у взрослых. Тем не менее, ОМЛ встречается довольно редко, на его долю приходится всего около 1% всех случаев рака. ОМЛ, как правило, является болезнью пожилых людей и редко встречается до 45 лет. Средний возраст людей, когда им впервые ставится диагноз ОМЛ, составляет около 68 лет. Но он может встречаться и у детей. ОМЛ несколько чаще встречается у мужчин, чем у женщин, но средний риск развития ОМЛ у обоих полов составляет примерно 0,5 от 1%.
Генетика ОМЛ
Был достигнут большой прогресс в понимании того, как изменения в ДНК (генах) внутри нормальных клеток костного мозга могут заставить их развиваться в клетки лейкемии. Более глубокое понимание изменений генов, которые часто происходят при ОМЛ, позволяет понять, почему эти клетки становятся ненормальными. После того, как исследователи обнаружили эти изменения, стало ясно, что существует много типов ОМЛ. У каждого могут быть различные генные изменения, которые влияют на развитие лейкемии и то, какие методы лечения могут быть наиболее полезными. Врачи сейчас учатся тому, как использовать эти изменения, чтобы помочь разработать более или менее интенсивное лечение.
Факторы риска острого миелоидного лейкоза (ОМЛ)
Фактор риска — это то, что влияет на ваш шанс заболеть раком. На некоторые факторы риска, такие как курение, можно влиять. Другие, такие как возраст человека или семейная история, не могут быть изменены. Но наличие даже нескольких факторов риска, не всегда означает, что человек заболеет, и многие люди заболевают раком без каких-либо известных факторов риска. Существуют некоторые известные факторы риска острого миелоидного лейкоза (ОМЛ).
Миелолейкоз может возникнуть в любом возрасте, но он становится все более распространенным с возрастом.
ОМЛ чаще встречается у мужчин, чем у женщин. Причина этого не ясна.
Единственный проверенный фактор риска, связанный с образом жизни, это курение.
Риск ОМЛ увеличивается, если вы подвергались воздействию определенных химических веществ. Например, длительное воздействие бензола, который является растворителем, используемым в резиновой промышленности, на нефтеперерабатывающих заводах, химических заводах, обувной промышленности и в отраслях, связанных с бензином. Некоторые исследования связывают риск МЛ с сильным воздействием формальдегида на рабочем месте.
Пациенты с раком, которых лечат определенными химиотерапевтическими препаратами, более склонны к развитию МЛ в последующие годы после лечения. Лекарства, называемые алкилирующими агентами, связаны с повышенным риском МЛ.
Высокодозное облучение (например, взрыв атомной бомбы или аварии на ядерном реакторе) увеличивает риск развития МЛ. У оставшихся в живых после бомбардировки Хиросимы был значительно повышенный риск развития острого лейкоза. Лучевое лечение рака также было связано с повышенным риском ОМЛ. Риск варьирует в зависимости от количества облучения и области лечения.
Люди с определенными заболеваниями крови подвергаются повышенному риску заболеть МЛ. К ним относятся хронические миелопролиферативные нарушения, такие как полицитемия вера, эссенциальная тромбоцитемия и идиопатический миелофиброз. Риск МЛ увеличивается, если эти расстройства лечат с помощью некоторых видов химиотерапии или облучения. У некоторых людей с миелодиспластическим синдромом (МДС) может развиться МЛ. Пациенты с МДС имеют низкое количество клеток крови и аномальные клетки в крови и костном мозге.
Некоторые синдромы, вызванные генетическими мутациями (аномальными изменениями), присутствующими при рождении, по-видимому, повышают риск МЛ. Они включают:
- Анемию Фанкони.
- Атаксия-телеангиэктазию.
- Синдром Швахмана-Даймонда.
- Синдром Ли-Фраумени.
- Нейрофиброматоз типа 1.
- Тяжелая врожденная нейтропения (также называемая синдромом Костмана).
Хромосомы — это длинные нити ДНК (гены) внутри наших клеток. Некоторые проблемы с хромосомами, присутствующие при рождении, также связаны с более высоким риском МЛ, в том числе:
- Синдром Дауна (рождение с дополнительной копией 21 хромосомы).
- Трисомия 8 (рождение с дополнительной копией хромосомы 8).
Обратите внимание
Хотя считается, что большинство случаев МЛ не имеют сильной генетической связи, наличие близкого родственника (например, родителя, брата или сестры) с ОМЛ повышает риск заболевания.
Развитие миелолейкоза
Определенные изменения в ДНК в нормальных клетках костного мозга могут привести к тому, что они станут клетками лейкемии. ДНК внутри наших клеток содержит гены, которые контролируют работу клеток. Некоторые гены контролируют, когда наши клетки растут, делятся, чтобы создать новые клетки, и умирают в нужное время:
- Гены, которые помогают клеткам расти, делиться или остаться в живых, называются онкогенами.
- Гены, которые помогают контролировать деление клеток или заставляют клетки умирать в нужное время, называются генами-супрессорами опухолей.
ДНК внутри каждой клетки состоит из длинных цепей, называемых хромосомами. Каждый раз, когда клетка делится на 2 новые клетки, она должна сделать новую копию своих хромосом. Этот процесс не идеален, и могут возникать ошибки, которые влияют на гены в хромосомах. Рак (включая ОМЛ) может быть вызван мутациями (изменениями), которые включают онкогены или выключают гены-супрессоры опухолей. Например, изменения в некоторых генах, таких как FLT3, c-KIT и RAS, распространены в клетках МЛ. Эти типы изменений мешают созреванию клеток костного мозга или помогают клеткам выйти из-под контроля.
Признаки и симптомы острого миелоидного лейкоза (ОМЛ)
Острый миелолейкоз (ОМЛ) может вызывать множество различных признаков и симптомов. Некоторые из них встречаются чаще при определенных подтипах лейкоза. Наиболее общие проявления – это:
Многие признаки и симптомы ОМЛ являются результатом нехватки нормальных клеток крови, которая возникает, если клетки лейкемии вытесняют нормальные кроветворные клетки в костном мозге. Вследствие этого людям не хватает нормальных эритроцитов, лейкоцитов и тромбоцитов. Эти недостатки обнаруживаются в анализах крови, и они также могут вызывать симптомы:
- Симптомы низкого количества эритроцитов (анемия). Эритроциты переносят кислород ко всем клеткам организма. Дефицит эритроцитов может вызвать усталость и слабость, ощущение холода, головокружения или спутанность мыслей, головные боли, бледность кожи, сбивчивое дыхание.
- Симптомы низкого количества белых кровяных клеток. Из-за нехватки нормальных лейкоцитов (лейкопения) могут возникать инфекции, в частности из-за дефицита борющихся с инфекцией лейкоцитов, называемых нейтрофилами (состояние, называемое нейтропенией). Люди с ОМЛ могут заразиться инфекциями, которые не проходят, или могут заражаться одной инфекцией за другой. Лихорадка часто сопровождает даже самую легкую инфекцию. Хотя люди с ОМЛ могут иметь высокое количество лейкоцитов из-за избыточного количества лейкозных клеток, эти клетки не защищают от инфекции, как нормальные лейкоциты.
- Симптомы низкого уровня тромбоцитов в крови. Тромбоциты обычно помогают остановить кровотечение. Нехватка тромбоцитов крови (так называемая тромбоцитопения) может привести к:
- Симптомы, вызванные большим количеством лейкозных клеток. Раковые клетки при ОМЛ (так называемые бласты) больше, чем нормальные лейкоциты, и у них больше проблем с прохождением крошечных кровеносных сосудов. Если количество бластов становится очень высоким, эти клетки могут засорить кровеносные сосуды и затруднить доступ нормальных эритроцитов (и кислорода) к тканям. Это называется лейкостазом. Лейкостаз встречается редко, но это неотложная медицинская патология, которую нужно лечить немедленно. Некоторые из симптомов похожи на те, которые наблюдаются при инсульте, и включают в себя:
- головную боль;
- слабость в одной стороне тела;
- невнятную речь;
- спутанность сознания;
- сонливость.
Обратите внимание
Когда поражены кровеносные сосуды в легких, у людей может быть одышка. Кровеносные сосуды в глазу также могут быть затронуты, что приводит к ухудшению зрения или даже его потере.
- Проблемы с кровотечением и свертываемостью. У пациентов с определенным типом ОМЛ, называемым острым промиелоцитарным лейкозом (ПМЛ), могут возникнуть проблемы с кровотечением и свертываемостью крови. У них может быть носовое кровотечение, которое не остановится, или порез, который не перестанет сочиться. Они также могут иметь отек голени из-за состояния, называемого тромбозом глубоких вен (ТГВ), или боль в груди и одышку от тромба в легких (так называемая легочная эмболия или ТЭЛА).
- Боль в костях или суставах. У некоторых людей с ОМЛ возникают боли в костях или суставах, вызванные накоплением лейкозных клеток в этих областях.
- Отек в области живота. Клетки лейкемии могут накапливаться в печени и селезенке, делая их больше. Это может быть замечено как полнота или опухоль живота. Нижние ребра обычно покрывают эти органы, но когда они увеличены, врач может почувствовать их.
Симптомы, вызванные распространением лейкемии
Если клетки лейкемии распространяются на кожу, они могут вызвать уплотнения или пятна, которые могут выглядеть как обычная сыпь. Опухолевая коллекция клеток ОМЛ под кожей или в других частях тела называется хлоромой, гранулоцитарной саркомой или миелоидной саркомой. Редко ОМЛ сначала появляется в виде хлоромы, без лейкозных клеток в костном мозге.
Определенные типы ОМЛ могут распространяться на десны, вызывая отек, боль и кровотечение.
Реже лейкозные клетки могут распространяться на другие органы. Распространение на головной и спинной мозг может вызвать такие симптомы, как:
В редких случаях ОМЛ может распространиться на глаза, яички, почки или другие органы. Редко ОМЛ может распространяться на лимфатические узлы (скопления иммунных клеток размером с бобовые по всему телу), делая их больше. Пораженные узлы в области шеи, паха, подмышек или над ключицей могут ощущаться как комки под кожей. Хотя любой из симптомов и признаков, приведенных выше, может быть вызван ОМЛ, они также могут быть вызваны другими заболеваниями.
Диагностика миелолейкоза
Некоторые признаки и симптомы могут свидетельствовать о том, что у человека может быть острый миелоидный лейкоз (ОМЛ), но для подтверждения диагноза необходимы анализы.
Врач собирает подробный медицинский анамнез, сосредоточив внимание на ваших симптомах и на том, как долго они у вас были. Он может также спросить о других проблемах со здоровьем, возможных факторах риска лейкемии.
Во время физического осмотра врач, скорее всего, будет уделять пристальное внимание органам зрения, полости рта, коже, лимфатическим узлам, печени, селезенке и нервной системе, а также будет искать места кровотечения или кровоподтеков или возможные признаки инфекции. Если есть основания полагать, что могут быть проблемы, вызванные низким уровнем клеток крови (анемия, инфекции, кровотечение или кровоподтеки и т. д.), врач, скорее всего, назначит анализы крови для проверки количества клеток крови. Вас также могут направить к гематологу, врачу, который специализируется на заболеваниях крови (включая лейкоз). Если врач считает, что у вас лейкемия, ему нужно будет проверить образцы клеток крови и костного мозга, чтобы быть уверенным в диагнозе.
Исследования костного мозга
Лейкемия начинается в костном мозге, поэтому биопсия костного мозга и проверка образцов на наличие лейкозных клеток является ключевой частью тестирования на МЛ. Образцы костного мозга получают при помощи двух методик, которые обычно проводятся одновременно:
- аспирации костного мозга;
- биопсии костного мозга.
Образцы обычно берутся из задней части тазовой кости, но иногда вместо этого используются другие кости. Если нужно сделать только аспирацию, ее можно взять из грудины (стернальная пункция).
Эти тесты помогают исследовать костный мозг и используются для диагностики лейкемии, их также можно повторить позже, чтобы определить, отвечает ли лейкоз на лечение.
Исследование цереброспинальной жидкости
Спинномозговая жидкость (цереброспинальная жидкость, ликвор) окружает головной и спинной мозг. ОМЛ может иногда распространяться на область вокруг головного и спинного мозга. Чтобы проверить этот факт, врачи могут взять образец ликвора для тестирования (процедура, называемая люмбальной пункцией).
Люмбальная пункция также иногда используется для доставки химиотерапевтических препаратов в ликвор, чтобы помочь предотвратить или лечить распространение лейкемии в спинной мозг и головной мозг.
Лабораторные тесты, используемые для диагностики и классификации ОМЛ
Для диагностики ОМЛ или для определения конкретного подтипа ОМЛ проводится ряд анализов крови и тестов.
Общий анализ крови и мазок периферической крови — это тест, который измеряет количество различных клеток в крови, таких как эритроциты, лейкоциты и тромбоциты. ОАК часто делается вместе с лейкоцитарной формулой, которая определяет количество различных типов лейкоцитов. При выполнении мазка периферической крови образец рассматривается под микроскопом. Изменения в количестве и появление различных типов клеток крови часто помогают диагностировать лейкоз. У большинства пациентов с ОМЛ в крови слишком много незрелых белых клеток и недостаточно эритроцитов или тромбоцитов. Многие из лейкоцитов могут быть миелобластами (бластами), которые являются очень ранними формами кроветворных клеток, обычно не обнаруживающихся в крови.
Биохимия крови и тесты на коагуляцию. Измеряют количество определенных химических веществ в крови и способность крови к свертыванию. Эти тесты не используются для диагностики лейкемии, но они могут помочь обнаружить проблемы с печенью или почками, аномальные уровни некоторых минералов в крови или проблемы со свертыванием крови.
Регулярные клеточные исследования под микроскопом. Образцы крови, костного мозга или ликвора рассматриваются под микроскопом гематологом / онкологом пациента (врачом, специализирующимся на раке и заболеваниях крови). Врач изучает размер, форму и другие признаки лейкоцитов в образцах, чтобы классифицировать их по определенным типам. Ключевым элементом является то, выглядят ли клетки зрелыми (как нормальные клетки крови) или незрелыми (без признаков нормальных клеток крови). Процент бластов в костном мозге или крови особенно важен. Наличие не менее 20% бластов в костном мозге или крови обычно требуется для диагностики ОМЛ. (В нормальном костном мозге количество бластов составляет 5% или менее, в то время как кровь обычно не содержит ни каких бластов.) МЛ также может быть диагностирован, если бласты обнаружены (с помощью другого теста), и есть изменение хромосом, которое происходит только в конкретном типе МЛ, даже если процент бластов не достигает 20%.
Цитохимия. Для цитохимических тестов клетки подвергаются воздействию химических соединений (красителей), которые реагируют только с некоторыми типами лейкозных клеток. Эти краски вызывают изменения цвета, которые можно увидеть под микроскопом, что может помочь врачу определить, какие типы клеток присутствуют.
Проточная цитометрия и иммуногистохимия. Как для проточной цитометрии, так и для иммуноцитохимии образцы клеток обрабатывают антителами, представляющими собой белки, которые прилипают только к определенным другим белкам на клетках. При иммуноцитохимии клетки просматривают под микроскопом, чтобы увидеть, прилипли ли к ним антитела (имеется в виду, что у них есть эти белки), в то время как для проточной цитометрии используется специальный аппарат.
Эти тесты используются для иммунофенотипирования — классификации лейкозных клеток по веществам (антигенам) на их поверхностях. Клетки лейкемии могут иметь разные антигены в зависимости от того, в каком типе клеток они начинаются и насколько они зрелые, и эта информация может быть полезна при классификации МЛ.
Хромосомные тесты. Эти тесты смотрят на хромосомы (длинные нити ДНК) внутри клеток. Нормальные клетки человека содержат 23 пары хромосом, каждая из которых имеет определенный размер и окрашивается определенным образом. Клетки ОМЛ иногда имеют хромосомные изменения, которые можно увидеть под микроскопом или обнаружить с помощью других тестов. Распознавание этих изменений может помочь выявить определенные типы ОМЛ и может иметь важное значение для определения тактики лечения.
Флуоресцентная гибридизация in situ (FISH). Этот тест более внимательно рассматривает ДНК клеток с использованием специальных флуоресцентных красителей, которые прикрепляются только к определенным генам или частям определенных хромосом. FISH может обнаружить изменения хромосом (такие как транслокации), которые видны под микроскопом в стандартных цитогенетических тестах, а также некоторые изменения, которые слишком малы, чтобы их можно было увидеть при обычном цитогенетическом тестировании.
Полимеразная цепная реакция (ПЦР): это очень чувствительный тест, который также может обнаружить некоторые изменения генов и хромосом, которые слишком малы, чтобы их можно было увидеть под микроскопом. Это полезно для обнаружения изменений гена, которые присутствуют только в нескольких клетках, и можно выявить небольшое количество лейкозных клеток в образце (как после лечения).
Визуализационные тесты при МЛ
Тесты визуализации используют рентгеновские лучи, звуковые волны, магнитные поля или радиоактивные частицы для создания изображений внутренней части тела. Лейкемия обычно не образует опухоли, поэтому визуальные тесты не часто помогают поставить диагноз. В некоторых случаях могут быть проведены визуальные тесты, чтобы помочь определить степень заболевания, если считается, что МЛ мог распространиться за пределы костного мозга и крови.
Лечение миелоидной саркомы: химиотерапия
Химиотерапия — это использование противораковых лекарств, которые вводятся в вену, под кожу или в спинномозговую жидкость (ликвор), или препаратов, которые принимаются внутрь для разрушения или контроля раковых клеток. За исключением случаев, когда препарат вводится в ликвор, эти средства попадают в кровоток и достигают всех областей тела, что делает это лечение полезным при раковых заболеваниях, таких как лейкемия, которые распространяются по всему организму. Химиотерапия является основным методом лечения для большинства людей с острым миелолейкозом (ОМЛ). Химиотерапия часто не рекомендуется для пациентов со слабым здоровьем, но пожилой возраст сам по себе не является препятствием для получения химиотерапии.
Лечение МЛ обычно делится на этапы:
- Индукция является первой фазой лечения. Цикл короткий и интенсивный, обычно длится около недели. Цель состоит в том, чтобы очистить кровь от лейкозных клеток (бластов) и уменьшить количество бластов в костном мозге до нормального уровня.
- Консолидация — химиотерапия после того, как пациент восстановился после индукции. Она предназначена для того, чтобы убить небольшое количество лейкозных клеток, которые все еще существуют, но их не видно (потому что их мало). Для консолидации химиотерапия проводится циклично, за каждым периодом лечения следует период отдыха, чтобы дать организму время восстановиться.
- Третья фаза, называемая поддержкой (или постконсолидацией), включает введение малой дозы химиотерапии в течение месяцев или лет после завершения консолидации. Это часто используется для лечения острого промиелоцитарного лейкоза, но редко используется для других типов ОМЛ.
Обратите внимание
Схемы химиотерапии, используемые для лечения МЛ, интенсивны и могут вызывать серьезные побочные эффекты, поэтому лечение обычно проводится в больнице.
Побочные эффекты
Химиопрепараты могут воздействовать на некоторые нормальные клетки в организме, что может привести к побочным эффектам. Они зависят от типа и дозы принимаемых лекарств и от того, как долго они принимаются. Побочные эффекты могут включать в себя:
- выпадение волос;
- потерю аппетита;
- тошноту и рвоту;
- диарею или запор.
Химиопрепараты также влияют на нормальные клетки костного мозга, что может снизить количество клеток крови. Это может привести к:
- Повышенному риску инфекций (из-за того, что слишком мало нормальных лейкоцитов).
- Легким кровоподтекам или кровотечениям (от слишком малого количества тромбоцитов).
- Усталости и одышке (из-за слишком малого количества эритроцитов).
Большинство побочных эффектов химиотерапии исчезают после окончания лечения. Низкое количество клеток крови может сохраняться несколько недель, но затем должно вернуться к норме.
Таргетные препараты для лечения острого миелоидного лейкоза (ОМЛ)
В последние годы были разработаны лекарства, которые нацелены на определенные части раковых клеток. Целевые препараты работают не так, как стандартные химиотерапевтические препараты, и, как правило, имеют разные побочные эффекты. Иногда они могут быть полезны, даже если химиотерапия уже проведена или они могут быть использованы вместе с химиотерапией, чтобы помочь препаратам работать лучше.
Химиотерапия является основным методом лечения большинства видов острого миелоидного лейкоза (ОМЛ). Но острый промиелоцитарный лейкоз (APL) отличается от других типов AML в некоторых важных отношениях.
Хирургия острого миелоидного лейкоза (ОМЛ)
Хирургия играет очень ограниченную роль в лечении острого миелоидного лейкоза (ОМЛ). Поскольку клетки лейкемии широко распространены по всему костному мозгу и крови, вылечить этот тип рака с помощью хирургии невозможно. Хирургия редко играет какую-либо роль даже в диагностике ОМЛ, так как обычно это можно сделать с помощью аспирата костного мозга и биопсии. В редких случаях изолированную опухоль лейкозных клеток (известную как миелоидная саркома, гранулоцитарная саркома или хлорома) можно лечить хирургическим путем.
Лучевая терапия при остром миелобластном лейкозе (ОМЛ)
Лучевая терапия использует высокоэнергетическое излучение, чтобы убить раковые клетки. Обычно она не является частью основного лечения для людей с острым миелолейкозом (ОМЛ), но есть несколько случаев, когда ее можно использовать:
- Радиация иногда используется для лечения лейкемии, которая распространилась за пределы костного мозга и крови, например, в мозг и спинномозговую жидкость, или в яички.
- Облучение всего тела часто является важной частью лечения перед трансплантацией стволовых клеток. Она используется (редко), чтобы помочь уменьшить опухоль (миелоидную саркому), если он давит на трахею (дыхательное горло) и вызывает проблемы с дыханием. Но вместо этого часто используется химиотерапия, поскольку она часто работает быстрее. Облучение можно использовать для уменьшения боли в области кости, пораженной лейкемией, если химиотерапия не помогла.
Трансплантация стволовых клеток при остром миелолейкозе (ОМЛ)
Дозы химиотерапевтических препаратов, которые врачи могут давать для лечения острого миелоидного лейкоза (ОМЛ), ограничены серьезными побочными эффектами, которые они могут вызвать. Хотя более высокие дозы этих лекарств могут убить больше раковых клеток, их нельзя принимать, потому что они могут серьезно повредить костный мозг, где образуются новые клетки крови. Это может привести к опасным для жизни инфекциям, кровотечениям и другим проблемам, вызванным низким количеством клеток крови.
Иногда врачи могут использовать трансплантацию стволовых клеток, также называемую трансплантацией костного мозга, чтобы дать более высокие дозы химиотерапии, чем обычно. Иногда также проводится лучевая терапия. После окончания лечения пациент получает инфузию кроветворных стволовых клеток для восстановления их костного мозга.
Кровеобразующие стволовые клетки, используемые для трансплантации, могут поступать либо из крови, либо из костного мозга. Иногда используются стволовые клетки пуповинной крови ребенка.
Парецкая Алена, врач, медицинский обозреватель
325 просмотров всего, 4 просмотров сегодня
Загрузка...