Формула изопропилового спирта
Изопропиловый спирт — Википедия
| Изопропанол | |||
|---|---|---|---|
| |||
| Систематическое наименование | Пропан-2-ол | ||
| Традиционные названия | Изопропиловый спирт | ||
| Хим. формула | C3H8O | ||
| Рац. формула | CH3CH(OH)CH3 | ||
| Состояние | жидкость | ||
| Молярная масса | 60,09 г/моль | ||
| Плотность | 0,7851 г/см³ | ||
| Динамическая вязкость | 0,00243 Па·с | ||
| Энергия ионизации | 10,1 ± 0,1 эВ[1] | ||
| Температура | |||
| • плавления | -89,5 °C | ||
| • кипения | 82,4 °C | ||
| • вспышки | 11,7 °C | ||
| • самовоспламенения | 400 °C | ||
| Пределы взрываемости | 2 ± 1 об.%[1] | ||
| Мол. теплоёмк. | 155,2 Дж/(моль·К) | ||
| Давление пара | 4,4 кПа при 20 °C | ||
| Константа диссоциации кислоты pKa{\displaystyle pK_{a}} | 16,5 | ||
| Растворимость | |||
| • в бензоле | хорошо растворим | ||
| • в ацетоне | растворим | ||
| Показатель преломления | 1,3776 (nD, 20°C) | ||
| Дипольный момент | 1,66 Д | ||
| Рег. номер CAS | 67-63-0 | ||
| PubChem | 3776 | ||
| Рег. номер EINECS | 200-661-7 | ||
| SMILES | |||
| InChI | |||
| RTECS | NT8050000 | ||
| ChEBI | 17824 | ||
| Номер ООН | 1219 | ||
| ChemSpider | 3644 | ||
| ЛД50 | 12800 мг/кг (кролик) | ||
| Токсичность | Класс опасности 3 | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, сокр. ИПС — широко используемое сокращение) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует 1 изомер изопропанола — пропанол-1, обладающий прямой цепью.
При нормальных условиях прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью[2].
Как и все летучие спирты, огнеопасен. В больших количествах ядовит (считается, что в 6 раз более этанола), требует осторожного обращения.
Химические свойства[править | править код]
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}} и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон[3].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства[править | править код]
Бесцветная жидкость с характерным спиртовым запахом, более резким и неприятным, чем у этанола, их можно отличить по запаху.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[4]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[5] [6].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH. -->
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {\ce {h4PO4}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[3].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора[7][8].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[9] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[8][10].
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности[11].
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание[12].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[13].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина[править | править код]
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства[править | править код]
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — doi:10.3109/15563650.2014.914527.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (неопр.) (недоступная ссылка). Дата обращения 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (неопр.) (26 февраля 2010). Дата обращения 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (неопр.) (недоступная ссылка). Дата обращения 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
описание вещества и способы получения, влияние на организм человека и где применяется раствор, помощь при отравлении
Что это такое — изопропиловый спирт? В каких сферах человеческой деятельности применяется это химическое соединение? Когда может произойти отравление им и как оно проявляется? Чем помочь пострадавшему человеку? Какие последствия для организма возможны после отравления?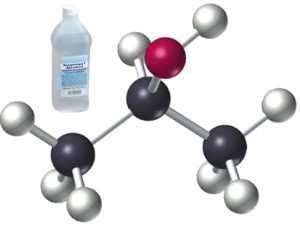
Что такое изопропиловый спирт
Изопропиловый спирт (ИПС) известен в химии под несколькими названиями:
- изопропанол, который по своему строению является изомером обычного пропанола, то есть соединением, сходным по химической формуле, но различающимся расположением одной из групп;
- втор-пропанол или пропанол-2;
- диметилкарбинол.
Под любым из этих терминов можно встретить изопропиловый спирт в быту. Но откуда возникло это химическое соединение и какие у него свойства?
Формула изопропилового спирта — Ch4CH(OH)Ch4. В отличие от своего предшественника он имеет необычное расположение одной из групп, а получен был в результате опытов над пропанолом. Оба они относятся к группе простейших спиртов алифатического ряда, поэтому и свойства их сходны.
Особенности изопропилового спирта, как химического соединения, следующие.
- Легко и быстро сгорает, после чего не образуется дыма, копоти, а получаются только вода и углекислый газ.
- Несмотря на общие свойства с метанолом у изопропилового спирта немного меньше токсичность, поэтому его широко применяют в косметологии и даже добавляют в некоторые лекарственные вещества или медицинские соединения.
- В нём хорошо растворяются эфирные масла, смолы и многие другие химические соединения.
- Важным свойством изопропилового спирта является его способность смешиваться с водой в любых соотношениях, от этого впоследствии зависит и температура замерзания смеси.
- После несложных химических превращений или при дегидрировании преобразуется в ацетон.
 Ещё одной отличительной чертой является его резкий запах.
Ещё одной отличительной чертой является его резкий запах.
- На вид — это обычная жидкость.
- Плотность изопропилового спирта — 0,7851 г/см3, но при температуре 20 ºC.
- Смешиваясь с воздухом, пар образует опасные взрывчатые вещества.
Попадание в организм человека приводит к опьянению, но его токсичность выше чем у этанола и по сравнению с последним приводит к более быстрому дурманящему эффекту, что зачастую является важным фактором для людей, желающих выпить.
Способы получения
В промышленности можно познакомиться с несколькими различными способами, благодаря которым появляется изопропиловый спирт. Продукт очень полезен в быту, он содержится как в косметических средствах, так и в бытовой химии. Поэтому его производством активно занимается химическая промышленность.
 Получить изопропиловый спирт можно путём гидрирования ацетона. То есть берут ацетон и добавляют к нему водород, для более быстрой реакции используют различные ускорители.
Получить изопропиловый спирт можно путём гидрирования ацетона. То есть берут ацетон и добавляют к нему водород, для более быстрой реакции используют различные ускорители.
- Второй наиболее распространённый вариант — гидратация пропилена (горючий газ). В отличие от первого способа химическая реакция происходит в две стадии. Сначала пропилен смешивают со серной кислотой и получают промежуточные продукты. А на втором этапе под воздействием воды и высокой температуры производят конечный продукт — изопропиловый спирт.
- Существуют менее распространённые способы производства изопропилового спирта — это окисление парафина воздухом, но он не так эффективен.
В промышленности существует два вида изопропилового спирта — это технический и абсолютированный, то есть более очищенный, содержащий меньшее количество примесей.
Где применяется
Исходя из всего вышесказанного изопропиловый спирт — это вредное или полезное вещество? Попытаемся разобраться. Применяют изопропиловый спирт почти во всех сферах деятельности человека, так как он является отличным растворителем.
 Последние годы в медицине вместо хорошо знакомого этилового спирта стали широко использовать изопропанол. Причиной тому являются его антисептические свойства, лёгкое соединение со многими химикатами, а так как изопропиловый спирт быстро растворяется, то при наружном использовании он практически не попадает в организм. То есть изопропиловый спирт, а также его производные применяют для дезинфекции в медицине.
Последние годы в медицине вместо хорошо знакомого этилового спирта стали широко использовать изопропанол. Причиной тому являются его антисептические свойства, лёгкое соединение со многими химикатами, а так как изопропиловый спирт быстро растворяется, то при наружном использовании он практически не попадает в организм. То есть изопропиловый спирт, а также его производные применяют для дезинфекции в медицине.
- Можно встретить это химическое вещество в составе косметических и парфюмерных средств, и даже гигиенической продукции. Мужчины с ним знакомы не понаслышке, ведь он присутствует в небольших количествах в лосьонах.
- ИПС используют при производстве репеллентов, так как он отличный растворитель и быстро испаряется. Тем не менее такие средства нужно применять с осторожностью маленьким детям.
- Из него получают перекись водорода, при дегидрировании ИПС образуется ацетон.
- В авиации пользуются химическими соединениями, содержащими изопропиловый спирт. Это стабилизатор авиационного бензина, а также веществ, которые применяются для профилактики обледенения стёкол и металлических поверхностей.
 Изопропиловый спирт используют, как универсальный растворитель в лакокрасочной промышленности. Так как он легко вступает во взаимодействие со многими химическими веществами, поэтому с его добавлением получают нитролаки, соединения целлюлозы, краски.
Изопропиловый спирт используют, как универсальный растворитель в лакокрасочной промышленности. Так как он легко вступает во взаимодействие со многими химическими веществами, поэтому с его добавлением получают нитролаки, соединения целлюлозы, краски.
- В чём ещё польза изопропилового спирта? С его помощью извлекают смолы из дерева, он входит в состав бытовой химии.
- Какие ещё есть продукты на основе изопропанола? — это всем знакомый антифриз — специальное химическое соединение, незамерзающее при низких температурах, которое добавляют в холодную пору года в охлаждающую систему автомобилей.
- Клей и вещества для обработки печатных плат создают на основе изопропанола.
Можно сказать, что химические соединения с изопропиловым спиртом в составе, окружают абсолютно каждого человека на протяжении всей жизни. Может ли такое полезное вещество причинить вред?
Причины отравления

Изопропанол относится к группе спиртов, а значит, полностью сохраняет их свойства как положительные, так и отрицательные.
Возможно ли отравление изопропиловым спиртом и в каких случаях это бывает? Чистое вещество, как и сложные химические соединения в составе с ним, применяются в быту, на производстве, в офисах, дома. То есть изопропанол доступен каждому. В последние годы многие любители употребить спиртосодержащие жидкости то ли вследствие незнания, то ли по ошибке его используют.
При сжигании ИПС в закрытом помещении у человека появятся симптомы отравления. От его горения образуется вода и углекислый газ, который в избытке опасен для здоровья. Температура вспышки изопропилового спирта — 82,5 °C.
Можно ли употреблять изопропиловый спирт? — нет, это равносильно распитию яда, пусть даже и с замедленным действием. Дело в том, что при поступлении в организм любое вещество преобразуется в печени, а фермент, который расщепляет изопропиловый спирт (алкогольдегидрогеназа) превращает его в ацетон. Всем известно, что последний не должен в норме присутствовать в тканях и органах человека.
В чём отличие изопропилового и этилового спирта? Изопропанол более токсичен, у него более сильное опьяняющее действие, а привыкание или наркотический эффект развивается быстрее. Употребление всего 50 мл изопропанола или интенсивное вдыхание его паров приведёт к развитию симптомов отравления.
Дети могут отравиться и меньшим количеством, чаще с признаками интоксикации в больницу поступают малыши до 6 лет.
Попав в организм человека, изопропиловый спирт может долго разлагаться от 2,5 до 8 часов. За это время вещество успевает повлиять негативно на все внутренние органы.
Симптомы
Вреден ли для здоровья изопропиловый спирт? — без сомнения. Именно поэтому в медицине большинство препаратов с ним в составе выпускают не для внутреннего, а для наружного применения. В закрытом помещении при большой концентрации даже его пары причинят вред человеку. На открытом воздухе он практически безопасен.
В составе химических соединений и органических растворителей он неопасен в случае, когда соблюдены все условия хранения и транспортировки.

Симптомы отравления изопропиловым спиртом, следующие.
- На первое место выходят признаки обычного алкогольного опьянения с нарушением координации движения, речи, походки.
- Иногда человек под воздействием изопропилового спирта просто засыпает.
- Немного позже при избытке изопропанола в крови возникают головные боли, слабость, выраженные головокружения, тошнота, нередко появляется многократная рвота.
- Затем появляются боли в мышцах, животе, поясничной области и даже в груди или сердце.
- Большие дозы изопропилового спирта приведут к нарушению зрения, когда под воздействием отравляющего вещества появляется туман, мелькание мушек перед глазами, а нередко даже двоение.
 раздражение дыхательных путей
раздражение дыхательных путей
Изопропанол вызывает раздражение дыхательных путей вплоть до остановки дыхательного центра.
- Токсичность изопропилового спирта в целом невысокая. Но если принять внутрь, то его ядовитые свойства сильнее чем у этанола в 3,5 раза.
- При тяжёлом отравлении кожа человека холодная на ощупь, мраморного оттенка, дыхание становится поверхностным, может, резко повыситься артериальное давление, появляются токсические судороги.
- В больших концентрациях от 12 промилле в крови изопропиловый спирт вызовет наркоз и смертельный исход.
Можно ли пить изопропиловый спирт? — однозначно нельзя. Ведь даже после употребления небольшого количества, возможны появление общей слабости, периодического подташнивания и головокружения. Серьёзные отравления изопропанолом возникают очень редко, поэтому смертельные случаи практические не встречаются.
Помощь при отравлении
Изопропиловый спирт относится к третьему классу опасности. И хотя он является умеренно опасным веществом — всё зависит от его концентрации в организме человека.
 Одним из отрицательных моментов в лечении интоксикации является отсутствие антидота или средства, выпив которое можно будет обезвредить изопропанол. Поэтому при первых признаках отравления человека надо как можно скорее доставить в ближайшую больницу.
Одним из отрицательных моментов в лечении интоксикации является отсутствие антидота или средства, выпив которое можно будет обезвредить изопропанол. Поэтому при первых признаках отравления человека надо как можно скорее доставить в ближайшую больницу.
Как оказать первую помощь?
- Пострадавшему следует незамедлительно промыть желудок обычной тёплой водой.
- Ввести слабительное.
- Если человек находится в сознании, то нужно дать ему выпить активированный уголь или любой другой сорбент.
Следующее, что действительно необходимо сделать при отравлении изопропиловым спиртом — вызвать скорую помощь или самостоятельно отвести пострадавшего в стационар.
Лечение
В стационаре проводится симптоматическое лечение:
- в больнице пациенту вводят в больших объёмах физиологический и плазмозамещающие растворы;
- применяют витамины;
- при необходимости назначают приём гормональных препаратов;
- корректируют кислотно-щелочное равновесие.
Последствия
В употреблении изопропилового спирта опасно не только само отравление, но и возможные следующие реакции со стороны внутренних органов.
- Нарушение работы печени и почек.
- Проблемы системы пищеварения — развитие гастрита или язвенной болезни желудка и двенадцатипёрстной кишки.
- Возможно, появление параличей и других нарушений в работе нервной системы.
Опасен ли изопропиловый спирт? — да, как и любое другое химическое соединение. Но правильное его использование не приведёт к трагедии. А вот употребление жидкостей, содержащих изопропанол, вызовет серьёзное отравление и отдалённые последствия для здоровья.
Источник: https://otravleniya.net/ximicheskie-otravleniya/izopropilovyj-spirt.html
Изопропиловый спирт вреден ли для здоровья
Изопропиловый спирт не предназначен для внутреннего употребления, так как вреден для здоровья человека. Вещество относится к третьему классу токсичности, который считается умеренно ядовитым.
Применение и правила безопасности

Опасно не только пить спирт, но и долго находиться в комнате, которая наполнена его парами.
Испарения могут вызвать:
- Сильную головную боль;
- Тошноту, рвоту;
- Резь в глазах;
- Потерю сознания;
- Коматозное состояние;
- Поражение дыхательной системы.
Опасен для человека состав окружающего воздуха, содержащий пары газообразного изопропилового спирта количеством 10 мг на кубометр и больше.
Чтобы уменьшить вред от испарения жидкости, рекомендуется при работе соблюдать требования безопасности:
- Надевать противогаз, если превышена максимальная норма концентрации паров спирта в помещении;
- При разливе средства следует помнить, что жидкость – легко воспламеняется. В здании обязательно должна быть вентиляция установленного образца для работы с горючими веществами;
- Контроль за предельно допустимым количеством паров должен выполняться автоматически;
- Руководство предприятия обеспечивает коллектив современными средствами пожаротушения;
- Регулярно проверять состояние электрической проводки помещения;
- Хранить спирт надо в специальных емкостях, обеспечивающих уменьшение взрывоопасности продукта.
Изопропиловый спирт обладает наркотическим влиянием при вдыхании пара или употреблении жидкости вовнутрь.
 Сфера применения вещества:
Сфера применения вещества:
- Парфюмерно-косметическая продукция – основа гигиенических жидкостей для бритья, лосьонов. Способствует отслоению туалетного мыла для придания продукту нескольких окрашенных пластов;
- В домашнем быту используется способность спирта растворять загрязнения – им можно очищать клавиатуру компьютера, удалять пятна чернил или фломастера на натуральных тканях. Очищающее воздействие препарата помогает сохранить целостность и яркость окраски тканей;
- Автолюбители используют изопропиловый спирт для смыва наледи на лобовом стекле. В западных странах используется метиловый спирт, но все смеси против замерзания автомобильных стекол в России изготовлены на основе изопропилового препарата, чтобы сохранить жизнь незадачливым любителям выпить. Кроме того, сырье намного дешевле питьевого спирта, который отягощен акцизами. Применяется вещество также для добавления к авто топливу;
- В химической промышленности из спирта получают ацетон, перекись водорода, как наиболее дешевый метод производства качественого продукта;
- Медициной успешно применяются антисептические свойства продукта. 70% концентрация вещества заменяет этанол при пропитке стерильных салфеток;
- Пищевая промышленность использует препарат для производства концентратов.
Отравление спиртом

Работая в помещении, необходимо использовать средства индивидуальной защиты от отравляющего вещества. Также надо оборудовать вентиляционную систему, достаточную для качественного очищения площади от повышенного количества газообразного продукта.
Отравиться можно, надышавшись парами с увеличенной концентрацией средства, или выпив жидкость.
При этом наступает наркотическое поражение организма, выраженное стандартными признаками:
- Возникновение сильной головной боли, тошноты, рвоты;
- Расстройство пищеварительной системы;
- Интоксикация всего организма.
Вред здоровью компенсируется оказанием своевременной медицинской помощи.
Если человек потерял сознание, надо без промедления вызвать бригаду “скорой помощи” для спасения жизни потерпевшего. Причиной может быть падение артериального давления, создающего опасность комы.

Изопропиловый спирт разлагается в печени с образованием ацетона, который выводится из организма почками. Главный симптом алкогольного отравления изопропилом – запах ацетона при выдохе. Частое употребление спиртного продукта вовнутрь вызывает отвращение к данному спирту, аллергические реакции, гиперчувствительность.
Отравление спиртом провоцирует вред здоровью:
- Ожог слизистой оболочки пищевода;
- Хронический гастрит желудка;
- Понижение артериального давления;
- Сердечная аритмия;
- Почечная недостаточность;
- Поражение печени.
При проявлении сильного опьянения, потере больным сознания необходимо оказать первую помощь и вызвать врача на дом.
Как помочь больному дома
 Доврачебные приемы помощи в домашних условиях своими силами:
Доврачебные приемы помощи в домашних условиях своими силами:
- Если человек без сознания, требуется уложить его в постель, приподнять голову и повернуть ее набок, чтобы рвотные массы не попали в дыхательную систему;
- Промыть желудок пациенту, находящемуся в сознании. Дать 10-15 измельченных таблеток активированного угля, рассчитав дозу: 1 таблетка на 10 кг веса человека;
- При попадании средства в глаза уменьшить вред помогает тщательное промывание органа под струей чистой воды. Если не принять вовремя меры по нейтрализации воздействия, возможна потеря зрения;
- Если во время работы с отравляющим веществом чувствуется жжение в дыхательных путях, необходимо срочно вывести человека на свежий воздух, а помещение проветрить. Слизистые оболочки рекомендуется прополоскать прохладной водой;
- В случае, когда неприятные ощущения не проходят после принятых мер, следует обратиться за помощью в лечебное учреждение.
В стационаре промывают организм с помощью гемодиализа, подключив аппарат «искусственной почки». Мера принимается, если состояние человека крайне тяжелое. Затем уточняется диагноз с помощью забора необходимых анализов, проводится соответствующее лечение. Назначается специальное лечебное питание на определенный срок.
Употреблять технические жидкости вовнутрь опасно для здоровья.
Систематическое питье изопропилового спирта приносит значительный вред организму человека:
- Желудок поражается гастритом различной этиологии, переходящий в хроническую форму. Регулярные ожоги слизистой оболочки ведут к изъязвлению поверхности, образованию язв и эрозий;
- Печень, отягощенная выводом препарата, отравляется производными переработки ацетона. Ее клетки отмирают и во время постоянной интоксикации не успевают восстанавливаться;
- Мочеполовая система страдает от ацетонового воздействия, ощутимый вред наносится почкам;
- Сердце не выдерживает повышенную нагрузку отравляющего вещества, отвечая возникновением патологий, опасных для жизни;
- Страдает головной мозг, омываемый кровью с ацетоновым содержанием. Увеличивается возможность возникновения необратимого поражения;
- Нарушается гормональный обмен, вызывая сбой в работе поджелудочной железы, щитовидки. Усиленная или наоборот уменьшенная выработка гормонов ведет к расстройству работы всего организма человека.
Употребление напитков, не предназначенных для питья, ведет к сбою в слаженной работе внутренних органов человека. Отравляющие вещества приводят к необратимым изменениям в человеческом организме, вызывая тяжелые заболевания, злокачественные новообразования, а нередко и летальный исход.
Источник: https://alcogolizm.com/questions/izopropilovyj-spirt-vreden-li-dlya-zdorovya.html
Изопропиловый спирт: вреден ли для здоровья, отравление
Это химическое вещество применяется в медицинских целях для первичной обработки, в промышленности. Узнаем, что представляет собой изопропиловый спирт, вреден ли он для здоровья, симптомы отравления таким веществом.
В химии спирт изопропиловый имеет такие названия, как изопропанол, диметилкаринол. В быту можно встретить любой из таких терминов. Отличие его от пропанола в том, что он имеет другое расположение радикала СН3. Имеет сходство с этанолом, поэтому его выпивают по неосторожности, приняв за алкогольный напиток.
Ознакомимся со свойствами изопропилового спирта:
- Он очень быстро горит, при этом не образует дыма или копоти. В процессе горения образуются углекислота и вода.
- Имеет меньшую, чем у пропанола токсичность. Поэтому его применяют в ряде случаев в косметологии.
- Является очень хорошим растворителем.
- Может растворяться в воде в каких угодно пропорциях.
- В процессе реакции дегидрирования превращается в ацетон.
- Имеет резкий запах.
- Плотность его ниже воды.
- При смешивании с воздухом образуется взрывоопасная смесь.
Что будет, если выпить изопропиловый спирт? При попадании в организме небольших количеств такого вещества наступит алкогольное опьянение. Причем одурманивающий эффект развивается от приема внутрь даже небольшого объема спирта. По токсичности он превосходит этанол.
Его применяют во многих отраслях промышленности. Главное его достоинство — это отличные свойства как растворителя.
- В последнее время его все чаще применяют вместо этанола в качестве растворителя.
- В медицинских целях его применяют в качестве отличного дезинфицирующего средства.
- Это вещество входит в состав многих косметических и парфюмерных продуктов.
- Используется в качестве репеллента.
- Является отличным стабилизатором авиационного топлива.
- Применяется как растворитель при производстве разнообразной лакокрасочной продукции.
- Изопропиловый спирт входит в состав многих товаров бытовой химии.
- Это вещество входит в состав антифризов — специальных составов, не замерзающих при низких температурах.
- На основе изопропилового спирта получают клеи и другие вещества, пригодные для производства печатных плат.
Отравление изопропиловым спиртом случается в быту или на производстве. Это связано с тем, что он доступен практически каждому. В последнее время из-за распространения алкогольных суррогатов возможно отравление из-за его употребления внутрь.
Вреден ли изопропиловый спирт для здоровья? Его категорически нельзя употреблять внутрь как суррогат алкоголя. Это действие равносильно употреблению яда, который действует на организм человека замедленно. При попадании этого спирта в организм происходит его преобразование в ацетон. Повышенное количество ацетона в клетках и тканях человеческого организма вызывает тяжелые отравления.
Главная причина отравления этим веществом — это его попадание внутрь. Он вызывает очень сильное алкогольное опьянение. При этом привыкание к нему развивается очень быстро. Пероральное употребление даже 50 мл спирта приводит к острому отравлению.
Отравиться можно и парами изопропилового спирта. Такое может быть, если вещество было разлито внутри закрытого помещения, и человек длительное время вдыхал пары ядовитого вещества.
Наиболее часто отравление изопропиловым спиртом происходит среди социально неблагополучных лиц без определенного места жительства и страдающих последними стадиями алкоголизма.
Схема отравления изопропанолом такая:
- Всасывание вещества в слизистой желудка.
- Попадание в кровь.
- Метаболизм изопропилового спирта в печени с помощью алкогольдегидрогеназы (так перерабатывается примерно 90 процентов яда).
- Выделение незначительного количества химически неизмененного вещества с легкими и почками.
- Расщепление изопропанола в крови до диметилкетона.
- Развитие токсической кетонемии и поражение почек, печени и головного мозга.
Время полувыведения такого вещества — около 7 часов. Смертельное количество спирта — около 250-300 мл при пероральном приеме. 50 миллилитров достаточно для того, чтобы человек почувствовал себя очень пьяным (как правило, дальнейшее употребление изопропанола прекращается).
Следует помнить и о том, что главным поражающим фактором при внутреннем употреблении небольших доз изопропилового спирта (до 50 мл) является продукт его распада, то есть ацетон.
Признаки интоксикации спиртом следующие:
- Острое алкогольное опьянение. У человека нарушается походка, слаженность движений, речи.
- При попадании изопропилового спирта внутрь человека может наступать глубокий сон.
- При избыточном количестве изопропанола у человека возникают болезненные ощущения в голове, сильная усталость, головокружение, тошнота и очень сильная, многократная рвота.
- Появляются сильные болевые ощущения в области мышц, поясницы, суставах, грудной клетке, теле.
- Повышенное количество изопропилового спирта может приводить к выраженным расстройствам зрения: появлению тумана в поле зрения, мушек, диплопия.
- При вдыхании концентрированных паров изопропилового спирта может происходить рефлекторная остановка дыхания. В тяжелых случаях у человека происходит расстройство работы дыхательного центра.
- При тяжелых степенях отравления кожа становится холодной, мраморного или синеватого оттенка. Дыхание у такого человека поверхностное, пульс не прощупывается, резко повышается артериальное давление и развиваются токсические судороги.
- Если в крови концентрация отравляющего вещества достигает 1,2 промилле, то возможен глубокий сон и летальный исход.
- Развивается поражение кишечника с выделением кровянистых выделений.
- Появляется запах ацетона из воздуха.
Вред изопропилового спирта очевиден. Его нельзя принимать внутрь ни при каких обстоятельствах.
Изопропиловый спирт является веществом средней степени токсичности. Но его действие будет зависеть от того, сколько человек употребил его внутрь.
Наиболее неблагоприятным моментом в лечении интоксикаций изопропиловым спиртом может быть отсутствие в конкретных условиях противоядия — средства, которое может обезвредить его.
Поэтому при начальных признаках интоксикации следует обратиться к лечащему врачу.
Этапы первой помощи такие:
- Больному надо промыть желудок большим количеством теплой воды.
- Необходимо ввести слабительное средство.
- При условии, что пациент находится в сознании, ему надо дать сорбент — например, активированный уголь.
Другие действия (например, приложение грелки к животу или ногам, дача сильного слабительного, алкоголя и других напитков) категорически противопоказана. Запрещено давать любые спазмолитики или анальгетики, сильное солевое слабительное. Отравившегося надо доставить в лечебное учреждение.
В условиях стационарного лечения назначается симптоматическая терапия:
- Пациенту в больших количествах вводят физраствор и плазмоподобные компоненты.
- Применяется внутривенное капельное введение витаминов.
- При необходимости назначаются гормональные средства (например, Преднизолон).
- Проводятся меры для коррекции кислотно-щелочного баланса.
Стабилизация состояния здоровья пациента производится еще на догоспитальном этапе — то есть, когда его помещают в отделение интенсивной терапии.
Для проведения реанимационных мероприятий проводится катетеризация центральной вены, очищение рта и носа пациента (чтобы обеспечить нормальное дыхание).
Если у отравившихся отмечается острое нарушение дыхания, то их подключают к аппарату искусственной вентиляции легких.
Яд можно удалить способом промывания желудка. Для этого вводят толстый желудочный зонд. Если больной выпил спирт больше, чем три часа назад, то промывание бесполезно. Если надо выделить всосавшийся яд, то применяют следующие процедуры:
- Диализ.
- Форсированный диурез.
- Энтеросорбцию.
- Промывание ЖКТ.
В качестве специфического антидота используют этиловый спирт. Пить его внутрь при отравлении категорически запрещено! Этанол вводится в организм капельно внутривенно (применяется 0,5 л 10-процентного раствора в глюкозе — 5 или 10 проц.). Если больной не переносит глюкозу, то можно использовать изотонический раствор хлористого натрия.
При своевременно начатой терапии наступает выздоровление.
Лабораторное определение отравления включает в себя:
- анализ крови;
- обследование крови на электролиты;
- биохимическое исследование крови;
- электрокардиограмма;
- рентгенография органов грудной клетки.
Употребление изопропанола опасно не только симптомами отравления, но и последствиями. У человека есть большой риск развития:
- Заболеваний печени и почек (печень отравляется продуктами переработки вещества).
- Гастрита.
- Язвы желудка и ДПК.
- Параличей.
- Тяжелых дисфункций в работе нервной системы.
- Тяжелых расстройств гормональной системы.
Прогноз при отравлении заметно ухудшается, если больной выпил значительное количество спирта. Исход лечения будет зависеть от того, насколько квалифицированно и качественно проводилось лечение.
- Чтобы при работе с изопропиловым спиртом не допустить интоксикации, нужно соблюдать такие меры.
- Если в помещении повышается предельно допустимая концентрация такого вещества, то необходимо использовать противогаз.
- Если вы работаете с жидкостью и разливаете ее, то следует помнить о том, что ее пары тоже могут попадать в организм через дыхательные пути. В таком случае помещение должно быть хорошо вентилируемым.
- Желательно, чтобы в помещении была аппаратура для контроля за концентрацией изопропанола в воздухе.
- Спирт надо хранить в упаковках, исключающих испарение.
Жидкость хранится в местах, недоступных для детей. Из-за своей неосведомленности они могут употребить изопропанол внутрь. Тяжелые отравления в таких случаях могут наступить даже в результате употребления 10 граммов вещества.
Изопропанол является ядовитым веществом, и его внутреннее употребление недопустимо. При появлении первых признаков интоксикации следует немедленно начать промывание желудка и вызвать скорую медицинскую помощь.
Источник: https://otravleniehelp.ru/drugoe/izopropilovyy-spirt-vreden-li-otravlenie.html
Изопропиловый спирт — Википедия
| Изопропанол | |
|---|---|
 | |
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Дипольный момент | 1,66 Д |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, сокр. ИПС — широко используемое сокращение) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует 1 изомер изопропанола — пропанол-1, обладающий прямой цепью.
При нормальных условиях прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью[2].
Как и все летучие спирты, огнеопасен. Токсичен (считается, что в 6 раз более этанола), требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}} и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон[3].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким и неприятным, чем у этанола, их можно отличить по запаху.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[4]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[5][6].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH. -->
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[3].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора[7][8].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[9] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[8][10].
Применение
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности[11].
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание[12].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[13].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (неопр.) (недоступная ссылка). Дата обращения 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (неопр.) (26 февраля 2010). Дата обращения 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (неопр.) (недоступная ссылка). Дата обращения 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
Формула Изопропилового спирта структурная химическая
Структурная формула
Истинная, эмпирическая, или брутто-формула: C3H8O
Химический состав Изопропилового спирта
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12,011 | 3 | 60% |
| H | Водород | 1,008 | 8 | 13,4% |
| O | Кислород | 15,999 | 1 | 26,6% |
Молекулярная масса: 60,096
Изопропиловый спирт, пропанол-2 (2-пропанол), втор-пропанол, изопропанол, диметилкарбинол, ИПС - простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
Прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом.
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, автохимии, медицинских изделиях, в средствах для очистки стёкол, оргтехники и как растворитель в промышленности.
В развитых странах пропанол-2 широко используется в товарах личной гигиены и в медицине, благодаря низкой токсичности. 75 % Водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь мембраны пор бактерий, таким образом обеспечивая высокую эффективность и более качественное обеззараживание. Изопропиловый спирт используется в качестве вспомогательного компонента профилактического средства от наружного отита.
Как и все спирты, огнеопасен, токсичен, требует осторожного отношения. Эффективен для лечения дерматита в качестве средства для протирания пораженных участков кожи, негативное влияние на кожу не отмечается.
Свойства
Химические свойства
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон.
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола (по этому признаку их можно в некоторых случаях отличить), tплавления −89,5 °C, tкипения 82,4 °C, плотность 0,7851 г/см³ (при 20 °C), tвспышки 11,7 °C. Нижний предел взрываемости в воздухе 2,5 % по объёму (при 25 °C). Температура самовоспламенения 456 °C. Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К).
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические вещества) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 80,2 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице:
| Концентрация спирта об % |
Концентрация спирта вес % |
Температура замерзания °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | -4 |
| 20 | 17 | -7 |
| 30 | 26 | -15 |
| 40 | 34 | -18 |
| 50 | 44 | -21 |
| 60 | 54 | -23 |
| 70 | 65 | -29 |
| 80 | 76 | -37* |
| 90 | 88 | -57* |
| 100 | 100 | -90* |
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена.
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH.
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (CH3)2CHOSO2OH, H2SO4 и H2O, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами.
Современный способ:
{CH3COCH3 + H2 →kat CH3CH(OH)CH3
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора.
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск) и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:- косметики
- парфюмерии
- бытовой химии
- дезинфицирующих средств
- средства для автомобилей (антифриз, растворитель в зимних стеклоомывателях)
- Репеллентов
- промывок печатных плат после пайки с флюсом, продается под названием «Очиститель универсальный».
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
Ингаляционное.
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0.6 мг/м³(ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает. Необходимо отметить, что изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству, изопропиловый спирт заменил этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пышное пламя, полностью разлагается на простые составляющие — воду и углекислый газ, не вызывая раздражений и иных побочных эффектов. Горение изопропанола не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций.
Пероральное.
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко.
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола (если только не выпил единовременно от 500 мл).
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием. Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола. Концентрация 1,2 %, воздействующая в течение 4 часов, оказывает опьяняющее действие.
При длительном воздействии больших концентраций паров вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Отравление изопропиловым спиртом возникает нечасто.
Изопропиловый спирт — Википедия
| Изопропанол | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание[4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}}.
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Видео по теме
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
Изопропиловый спирт — Википедия
| Изопропанол | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание[4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}}.
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
Изопропиловый спирт - это... Что такое Изопропиловый спирт?
| Изопропанол | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Сокращения | Изопропанол, 2-пропанол |
| Традиционные названия | Изопропиловый спирт |
| Химическая формула | CH3CH(OH)CH3 |
| Эмпирическая формула | C3H8O |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 60,09 а. е. м. |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость (ст. усл.) | 0,00243 Па·с (при 20 °C) |
| Термические свойства | |
| Температура плавления | -89,5 °C |
| Температура кипения | 82,4 °C |
| Температура вспышки | 11,7 °C |
| Температура самовоспламенения | 400 °C |
| Молярная теплоёмкость (ст. усл.) | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| SMILES | CC(O)C |
| Безопасность | |
| Токсичность | довольно высокая |
Изопропиловый спирт, пропанол-2 (2-пропанол), изопропанол, диметилкарбинол, ИПС — простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — 1-пропанол. Принадлежит к веществам 3-го класса опасности (умеренно опасные вещества) по степени воздействия на организм, обладает наркотическим действием. Граница ПДК для паров изопропанола в воздухе составляет 10 мг/м3. Отравление изопропиловым спиртом возникает в результате вдыхания паров, содержащих концентрацию, превышающую ПДК, кумулятивными свойствами не обладает[1]. Потребление внутрь уже в небольших дозах вызывает отравление. Широко используется как технический спирт в средствах для чистки стёкол, оргтехники и т. п. и как растворитель в промышленности (где растворители необходимы).
Свойства
Химические свойства
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон.[2]
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резковатым по сравнению с этанолом (по чему их можно в некоторых случаях отличить), tплавления −89,5 °C, tкипения 82,4 °C, плотность 0,7851 г/см³ (при 20 °C), tвспышки 11,7 °C. Нижний предел взрываемости в воздухе 2,5 % по объёму (при 25 °C). Температура самовоспламенения 456 °C. Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К).
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 83,38 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице[3]:
| Концентрация спирта об % | Концентрация спирта вес % | Температура замерзания °C |
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена.[4][5]
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
- CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH.
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH, H2SO4 и Н2О, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами.[2]
Современный способ:
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора.[6][7]
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[8] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[9][7]
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители).
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
Оказывает раздражающее воздействие на глаза и дыхательные пути, при кратком воздействии больших концентраций паров вызывает головную боль. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обуславливает его токсическое действие. Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто уже при дозах порядка 50 мл и более.
Предельно допустимая концентрация изопропанола в воздухе равна 10 миллиграммов на кубический метр.
Изопропанол органолептически заметно отличается от этанола и не может быть ошибочно принят за этанол. Имеет отличный от этанола запах, более «грубый». При приеме внутрь вызывает опьянение, сходное с алкогольным. Изопропанол окисляется в организме при участии альдегиддегидрогеназы до ацетона. Скорость окисления в среднем в 2 — 2,5 раза ниже, чем у этанола, поэтому опьянение изопропанолом очень стойкое. При частом употреблении к изопропанолу быстро развивается непереносимость, а в отдельных случаях — гиперчувствительность и аллергия. Хотя токсичность изопропанола примерно в 3,5 раза больше, чем у этанола, но при этом опьяняющее действие его также выше в 10 раз[источник не указан 546 дней]. По этой причине смертельных отравлений изопропанолом не зафиксировано, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием.[1] Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола.[10] Концентрация 1,2 %, воздействующая в течение 4 часов оказывает наркотический эффект. При аналогичном воздействии в течение 8 часов — в половине случаев наблюдается смертельный исход.[11]
Примечания
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
- ↑ Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse
Изопропиловый спирт Википедия
| Изопропанол | |||
|---|---|---|---|
| |||
| Систематическое наименование | Пропан-2-ол | ||
| Традиционные названия | Изопропиловый спирт | ||
| Хим. формула | C3H8O | ||
| Рац. формула | CH3CH(OH)CH3 | ||
| Состояние | жидкость | ||
| Молярная масса | 60,09 г/моль | ||
| Плотность | 0,7851 г/см³ | ||
| Динамическая вязкость | 0,00243 Па·с | ||
| Энергия ионизации | 10,1 ± 0,1 эВ[1] | ||
| Температура | |||
| • плавления | -89,5 °C | ||
| • кипения | 82,4 °C | ||
| • вспышки | 11,7 °C | ||
| • самовоспламенения | 400 °C | ||
| Пределы взрываемости | 2 ± 1 об.%[1] | ||
| Мол. теплоёмк. | 155,2 Дж/(моль·К) | ||
| Давление пара | 4,4 кПа при 20 °C | ||
| Константа диссоциации кислоты pKa{\displaystyle pK_{a}} | 16,5 | ||
| Растворимость | |||
| • в бензоле | хорошо растворим | ||
| • в ацетоне | растворим | ||
| Показатель преломления | 1,3776 (nD, 20°C) | ||
| Дипольный момент | 1,66 Д | ||
| Рег. номер CAS | 67-63-0 | ||
| PubChem | 3776 | ||
| Рег. номер EINECS | 200-661-7 | ||
| SMILES | |||
| InChI | |||
| RTECS | NT8050000 | ||
| ChEBI | 17824 | ||
| Номер ООН | 1219 | ||
| ChemSpider | 3644 | ||
| ЛД50 | 12800 мг/кг (кролик) | ||
| Токсичность | Класс опасности 3 | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, сокр. ИПС — широко используемое сокращение) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует 1 изомер изопропанола — пропанол-1, обладающий прямой цепью.
При нормальных условиях прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью[2].
Как и все летучие спирты, огнеопасен. В больших количествах ядовит (считается, что в 6 раз более этанола), требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}} и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон[3].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким и неприятным, чем у этанола, их можно отличить по запаху.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[4]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[5][6].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH. -->
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {\ce {h4PO4}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[3].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора[7][8].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[9] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[8][10].
Применение
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности[11].
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание[12].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[13].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — doi:10.3109/15563650.2014.914527.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ "Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke", Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (неопр.) (недоступная ссылка). Дата обращения 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (неопр.) (26 февраля 2010). Дата обращения 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (неопр.) (недоступная ссылка). Дата обращения 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
| Изопропанол | |||
|---|---|---|---|
| |||
| Систематическое наименование | Пропан-2-ол | ||
| Традиционные названия | Изопропиловый спирт | ||
| Хим. формула | C3H8O | ||
| Рац. формула | CH3CH(OH)CH3 | ||
| Состояние | жидкость | ||
| Молярная масса | 60,09 г/моль | ||
| Плотность | 0,7851 г/см³ | ||
| Динамическая вязкость | 0,00243 Па·с | ||
| Энергия ионизации | 10,1 ± 0,1 эВ[1] | ||
| Температура | |||
| • плавления | -89,5 °C | ||
| • кипения | 82,4 °C | ||
| • вспышки | 11,7 °C | ||
| • самовоспламенения | 400 °C | ||
| Пределы взрываемости | 2 ± 1 об.%[1] | ||
| Мол. теплоёмк. | 155,2 Дж/(моль·К) | ||
| Давление пара | 4,4 кПа при 20 °C | ||
Изопропиловый спирт
Изопропиловый спирт
ТУ 6-09-402-85 или ТУ 2632-015-11291058-95
(CH3)2CHOH
Изопропиловый спирт (пропанол-2, втор-пропанол, изопропанол, диметилкарбинол, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
Изопропиловый спирт — бесцветная жидкость с запахом спирта. Обладает теми же свойствами, что и вторичные спирты жирного ряда.
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, автохимии, медицинских изделиях, в средствах для очистки стёкол, оргтехники и как растворитель в промышленности.
В развитых странах пропанол-2 широко используется в товарах личной гигиены и в медицине, благодаря низкой токсичности. 75 % Водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь мембраныпор бактерий, таким образом обеспечивая высокую эффективность и более качественное обеззараживание. Изопропиловый спирт используется в качестве вспомогательного компонента профилактического средства от наружного отита.
Как и все спирты, огнеопасен, умеренно токсичен, требует осторожного отношения. Эффективен для лечения дерматита в качестве средства для протирания пораженных участков кожи, негативное влияние на кожу не отмечается.
Химические свойства
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениямиизопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон.
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола (по этому признаку их можно в некоторых случаях отличить).Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 80,2 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице:
| Концентрация спирта об % |
Концентрация спирта вес % |
Температура замерзания °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена.
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
- CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH.
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH, H2SO4 и Н2О, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами.
Современный способ:
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора.[10][11]
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)
Применение
Изопропиловый спирт используют для получения:
- ацетона (дегидрированием или неполным окислением)
- пероксида водорода
- метилизобутилкетона
- изопропилацетата
- изопропиламина.
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
- косметики
- парфюмерии
- бытовой химии
- дезинфицирующих средств
- средства для автомобилей (антифриз, растворитель в зимних стеклоомывателях)
- Репеллентов
- промывок печатных плат после пайки с флюсом, продается под названием «Очиститель универсальный».
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0.6 мг/м³(ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает. Необходимо отметить, что изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству, изопропиловый спирт заменил этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пышное пламя, полностью разлагается на простые составляющие — воду и углекислый газ, не вызывая раздражений и иных побочных эффектов. Горение изопропанола не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций.[15]
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко.
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола (если только не выпил единовременно от 500 мл).
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием. Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола.[16] Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние наркоза и смерть.
При длительном воздействии больших концентраций паров вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Отравление изопропиловым спиртом возникает нечасто.
| Общие | |
|---|---|
| Систематическое наименование |
Пропанол-2 |
| Традиционные названия |
Изопропиловый спирт |
| Хим. формула |
C3H8O |
| Рац. формула |
CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние |
жидкость |
| Молярная масса |
60,09 г/моль |
| Плотность |
0,7851 г/см³ |
| Динамическая вязкость |
0,00243 Па·с |
| Энергия ионизации |
10,1±0,1 эВ[1] |
| Термические свойства | |
| Т. плав. |
-89,5 °C |
| Т. кип. |
82,4 °C |
| Т. всп. |
11,7 °C |
| Т. свспл. |
400 °C |
| Пр. взрв. |
2±1 об.%[1] |
| Мол. теплоёмк. |
155,2 Дж/(моль·К) |
| Давление пара |
4,4 кПа при 20 °C |
| Химические свойства | |
| pKa |
16,5 |
| Растворимость в бензоле |
хорошо растворим |
| Растворимость в ацетоне |
растворим |
| Оптические свойства | |
| Показатель преломления |
1,3776 |
Используется для денатурации этилового спирта, получения пероксида водорода, ацетона, изопропиламина, изопропилацетата, метилизобутилкетона. Также употребляется в промышленности, в токарных и фрезерных работах, при резании алюминия. Изопропиловый спирт входит в состав бытовой химии, косметики, дезинфицирующих средств, репеллентов, средств для автомобилей, к примеру, в состав антифриза, тормозной жидкости, используется в качестве растворителя для зимних стеклоомывателей, входит в состав промывок для печатных плат после пайки с флюсом.