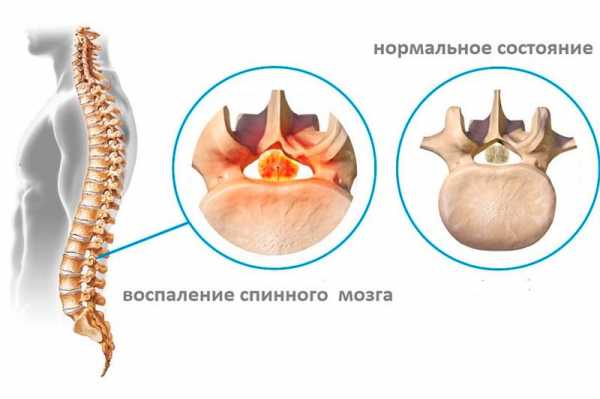
Ядерный сдвиг влево в нейтрофильном ряду встречается при
Ядерный сдвиг нейтрофилов
В этом изменении нормального процентного соотношения между клетками нейтрофильного ряда различают:
1. Ядерный сдвиг нейтрофилов влево - характеризуется появлением в гемограмме молодых и дегенеративных форм нейтрофилов, что наблюдается при:
- инфекционных заболеваниях,
- воспалительных процессах,
- злокачественных новообразованиях,
- интоксикациях.
По характеру ядерного сдвига нейтрофилов различают:
а) регенеративный сдвиг - при котором увеличивается количество палочкоядерных (П) и юных (Ю) нейтрофилов на фоне лейкоцитоза, что является показателем повышенной деятельности костного мозга; наблюдается при воспалительных и гнойно-септических процессах;
б) дегенеративный сдвиг - отмечается увеличение количества только палочкоядерных нейтрофилов и появление дегенеративных изменений в клетках. Это является показателем функционального угнетения костного мозга. Может протекать как с лейкоцитозом, так и с лейкопенией.
Дегенеративный сдвиг на фоне лейкоцитоза характерен для:
- сальмонеллеза,
- токсической дизентерии,
- острого перитонита,
- уремической и диабетической комы.
Дегенеративный сдвиг на фоне лейкопении характерен для:
- вирусных инфекций,
- тифопаратифозных заболеваний.
в) лейкемоидные реакции характеризуются появлением незрелых форм: миелоцитов (М), промиелоцитов и даже миелобластов на фоне выраженного лейкоцитоза.
Характерны для:
- инфекционных болезней,
- туберкулеза,
- злокачественных новообразований (рак желудка, молочной железы, толстой кишки).
Отношение суммы всех несегментированных форм нейтрофилов к сегментированным называется "индексом сдвига" нейтрофилов и определяется по следующей формуле:
Индекс сдвига = (М+Ю+П)/C, где
М - миелоциты, Ю - юные нейтрофилы, П - палочкоядерные, С - сегментоядерные нейтрофилы.
В норме индекс сдвига равен 0,05-0,08.
Тяжесть степени заболевания по индексу сдвига:
- тяжелая степень - индекс от 1,0 и выше,
- средней степени - индекс 0,3-1,0,
- легкая степень - индекс не более 0,3.
2. Ядерный сдвиг нейтрофилов вправо - среди нейтрофилов преобладают зрелые формы с 5-6 сегментами вместо обычных трех.
Индекс сдвига - менее 0,04.
Ядерный сдвиг нейтрофилов вправо встречается:
- в норме у 20 процентов практически здоровых людей,
- при аддисонобирмеровской анемии,
- полицетемии,
- при лучевой болезни.
Ядерный сдвиг нейтрофилов вправо при инфекционных и воспалительных заболеваниях указывает на благоприятное течение.
Сдвиг лейкоцитарной формулы влево
Сдвиг лейкоцитарной формулы влево – появление в периферической крови повышенного количества молодых форм нейтрофилов – палочкоядерных и юных. Наблюдается при активной борьбе организма с возбудителем. Благоприятный признак течения болезни.
Сдвиг лейкоцитарной формулы вправо
Сдвиг вправо – проявление старения популяции нейтрофилов без пополнения молодыми формами. В мазке крови только сегментноядерные нейтрофилы с признаками старения (гиперсегментация ядра).
Клиническое значение
При различных патологических состояниях лейкоцитарная формула может претерпевать значительные изменения: увеличение или уменьшение содержания какого-либо вида лейкоцитов или появлении клеточных форм, в норме в периферической крови не встречающихся.
Увеличение количества базофилов обозначается как базофилия, эозинофилов – как эозинофилия, нейтрофилов – как нейтрофилия или нейтрофилез, лимфоцитов – как лимфоцитоз, моноцитов – как моноцитоз. Уменьшение соответствующих видов клеток - эозинопения, нейтропения, лимфопения и моноцитопения.
Увеличение или уменьшение количества отдельных видов лейкоцитов может быть абсолютным и относительным. Изменение процентного содержания не всегда соответствует колебанию абсолютных величин, что необходимо принимать во внимание при анализе лейкоцитарной формулы.
Базофилия - увеличение количества базофилов наблюдается при хроническом миелолейкозе, полицитемии, гипотиреозе, нефрите, сахарном диабете, при длительном рентгеновском воздействии, у женщин в начале менструаций.
Эозинофилия встречается при аллергических заболеваниях (бронхиальная астма, крапивница, отек Квинке, вазомоторный ринит), глистных инвазиях, хроническом миелолейкозе, некоторых инфекциях (скарлатина, оспа).
Уменьшение количества эозинофилов в периферической крови (эозинопения) или полное их отсутствие (анэозинофилия) наблюдается в начальном периоде острых инфекций, воспалительных процессов, инфаркта миокарда. Появление эозинофилов в крови в таких случаях является хорошим признаком.
Увеличение количества нейтрофилов в периферической крови (нейтрофилез) отмечается при острых воспалительных заболеваниях, гнойных процессах, различных интоксикациях, опухолях.
Сдвигом лейкоцитарной формулы вправо называется увеличение количества более зрелых нейтрофилов (сегментоядерных) –сегментоядерный нейтрофилез.
Сдвиг лейкоцитарной формулы влево –появление незрелых нейтрофилы с круглым ядром – метамиелоцитов (юные нейтрофилы), или их предшественников – миелоцитов. При этом степень выраженности нейтрофилеза и его характер могут указывать на тяжесть процесса, приведшего к изменению периферической крови.
Незначительный нейтрофилез с небольшим сдвигом влево обычно указывает на легкое течение заболевания, а значительный – на тяжелое. В последнем случае в периферической крови появляются нейтрофилы с токсической зернистостью и вакуолизацией цитоплазмы.
Нейтропения наблюдается при ряде инфекционных заболеваний (брюшной тиф), вирусных инфекциях (грипп), при действии ионизирующей радиации, после рентгенотерапии, при гемобластозах. Временное уменьшение количества нейтрофилов в периферической крови встречается у больных, принимающих некоторые медикаменты (бутадион, цитостатические препараты).
Лимфоцитозчасто наблюдается при заболеваниях, сопровождающихся нейтропенией, и является в таких случаях относительным.
Абсолютный лимфоцитоз встречается при инфекционном мононуклеозе, хроническом лимфолейкозе, туберкулезе и некоторых детских инфекциях (корь, краснуха, ветряная оспа, коклюш).
В раннем детском возрасте и после приема внутрь большого количества жиров может отмечаться физиологический лимфоцитоз.
Лимфоцитопения может встречаться у больных с нейтрофилезом, т. е. является относительной.
Абсолютная лимфоцитопения наблюдается при всех заболеваниях, сопровождающихся замещением лимфоидной ткани другими клеточными элементами (лимфогранулематоз, лимфосарком, острый и хронический миелоидный лейкоз), а также при уремии, тяжелых септических процессах, туберкулезе, при лучевой болезни, длительном приеме гормонов.
Моноцитозсвидетельствует о развитии патологических иммунных процессов в организме. Увеличение количества моноцитов в периферической крови с одновременным увеличением нейтрофилов наблюдается при затяжном септическом эндокардите, нагноительных процессах. Абсолютный моноцитоз характерен для инфекционного мононуклеоза, при котором он развивается как специфическая реакция на вирус.
Моноцитопения встречается при тяжелых септических заболеваниях и гипертоксических формах инфекционных процессов.
5. Понятие о гемостазе. Сосудисто-тромбоцитарный и коагуляционный гемостаз. Факторы и фазы свертывания крови. Тромбоциты и их роль в гемокоагуляции. Взаимодействие свертывающей и противосвертывающей систем крови. Фибринолиз.



Свертывание крови (гемокоагуляция) является защитным механизмом организма, направленным на сохранение крови в сосудистой системе. В результате свертывания кровь из жидкого состояния переходит в желеобразный сгусток за счет превращения фибриногена (растворимого в воде белка плазмы) в фибрин (не растворимый в воде белок). Первые шаги по раскрытию механизма свертывания крови были открыты физиологом А.А. Шмидтом (1863-1864). Он обнаружил некоторые факторы свертывания, признал ферментативную природу реакций и их фазность. По современным представлениям в процессе свертывания крови принимают участие много факторов: плазменные, тромбоцитарные, сосудистого эндотелия и субэндотелия, а также форменные элементы.
В свертывании крови принимают участие много факторов
Они получили название – факторы свертывания крови.
Содержатся в плазме крови, форменных элементах (эритроцитах, лейкоцитах, тромбоцитах) и в тканях.
По международной номенклатуре они обозначаются арабскими цифрами и
латинскими буквами (от слова пластинка). Важнейшими из них являются:

Огромное значение в адгезии тромбоцитов играет фактор Виллебранда, содержащийся в плазме и α-гранулах пластинок, а также фибронектин. Фибронектин обнаружен, как в сосудистой стенке, так и в α-гранулах тромбоцитов.
Необходимо отметить, что адгезия резко усиливается при реакции «освобождения» кровяных пластинок, когда фибронектин и фактор Виллебранда покидают тромбоциты и поступают непосредственно в плазму крови. Адгезия и агрегация тромбоцитов, как уже указывалось, зависит от соотношения тромбоксанов, выделяемых из кровяных пластинок, и простациклина, синтезируемого преимущественно эндотелием сосудистой стенки (рис. 14).
Важная роль в агрегации кровяных пластинок принадлежит фактору, активирующему тромбоциты (ФАТ), который синтезируется лейкоцитами, мононуклеарами, макрофагами, тромбоцитами, сосудистой стенкой.
Таким образом, тромбоциты, осуществляя адгезию, агрегацию и реакция «освобождения» активно участвуют в образовании и консолидации тромбоцитарной пробки, запускают процесс свертывания крови, чем способствуют остановке кровотечения.

Процесс свертывания крови и его значение.
У здорового человека кровотечение из мелких сосудов при их ранении останавливается за 1-3 мин. Этот первичный гемостаз почти целиком обусловлен сужением сосудов и
механической закупоркой их агрегатами тромбоцитов и получил название сосудисто-тромбоцитарного
гемостаза, который складывается из ряда последовательных процессов:
Сосудисто-тромбоцитарный механизм гемостаза.
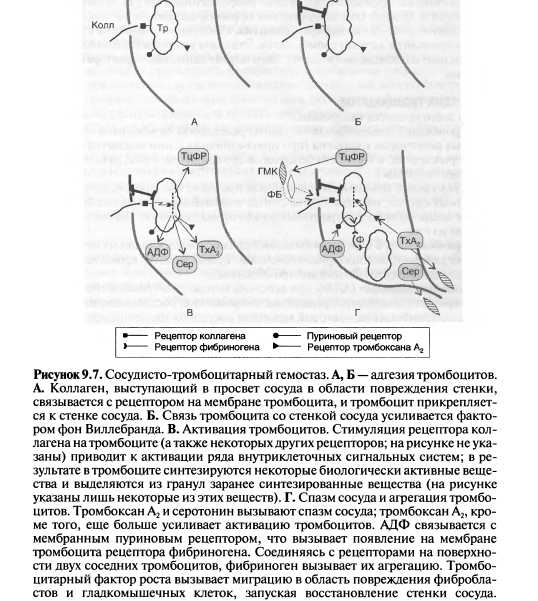
Остановка кровотечения за счет сосудисто-тромбоцитарного механизма гемостаза осуществляется следующим образом.
1) Рефлекторный спазм поврежденных сосудов. Обеспечивается сосудосуживающими веществами, освобожденными из тромбоцитов (серотонин, адреналин, норадреналин). Спазм приводит к временной остановке или уменьшению кровотечения.
• 2) Адгезия тромбоцитов (приклеивание к месту травмы). В месте повреждения стенка сосуда становится заряженной
положительно. Отрицательно заряженные тромбоциты прилипают к обнажившимся волокнам коллагена базальной
мембраны. Адгезия завершается за 3-10 сек.
• 3) Обратимая агрегация (скучивание) тромбоцитов. Стимулятором является «внешняя» АДФ, выделяющаяся из поврежденного сосуда и «внутренняя» АДФ, освобождающаяся из тромбоцитов и эритроцитов. Образуется рыхлая тромбоцитарная пробка, пропускающая через себя плазму крови.
Сосудисто-тромбоцитарные реакции обеспечивают гемостаз лишь в микроциркуляторных сосудах, однако тромбоцитарные тромбы не выдерживают высокого давления и вымываются. В таких сосудах гемостаз может быть достигнут путем образования фибринового тромба. Его образование осуществляется ферментативным коагуляционным механизмом, протекающим в 3 фазы .
Фаза I. Формирование протромбиназы.
Различают внешнюю (тканевую) и внутреннюю (кровяную) систему. Внешний путь запускается тканевым тромбопластином, который выделяется из стенок поврежденного сосуда и окружающих тканей. Во внутренней системе фосфолипиды и другие факторы поставляются самой кровью. Тканевая система (тканевая протромбиназа) образуется за 5-10 сек.
тромбоцитарная
5-10 мин. протромбиназы
эритроцитарная
Толчком для образования тканевой протромбиназы служит повреждение стенок сосудов с выделением из них в кровь тканевого тромбопластина. В формировании тканевой протромбиназы участвуют плазменные факторы VII, V, X, и Ca++.
Кровяная протромбиназа образуется медленнее. Инициатором ее образования являются обнажающиеся при
повреждении сосуда волокна коллагена. Начальной реакцией является активация фактора Хагемана при контакте с данными волокнами. После этого он с помощью активированного им калликреина и кинина активирует фактор XI, образуя с ним комплекс- продукт контактной активации. К этому времени происходит разрушение эритроцитов и тромбоцитов, на фосфолипидах, которых завершается образование комплекса фактор XII + фактор XI.
Эта реакция самая продолжительная, на нее уходит 5-7 мин. из 5-10 мин. всего времени свертывания. Под влиянием
фактора XI активизируется фактор IX, который реагирует с фактором VIII и Ca. Образующийся кальциевый комплекс, адсорбируется на фосфолипидах, образуя последний комплекс фактор X +фактор V + Ca++ и завершение образования кровяной протромбиназы.
Фаза II. Появление протромбиназы свидетельствует о начале II фазы свертывания крови – образование тромбина ( 2-5 сек.) Протромбиназа адсорбирует протромбин и превращает его в тромбин при участии факторов V, X и Ca++.
Фаза III. Превращение фибриногена в фибрин в 3 этапа.
Тромбин 1). Фибриноген → фибрин-мономер Ca 2). Фибрин-мономер → полимеризация и образование фибрин - полимера (растворимый фибрин «S» ). 3). Образуется окончательный нерастворимый фибрин «1» при участии фактора XIII и фибриназы тканей, тромбоцитов и эритроцитов. Завершается образование кровяного тромба.
Таким образом, свертывание крови представляет собой цепной ферментативный процесс, в котором на матрице фосфолипидов последовательно активируются факторы свертывания и образуются их комплексы. Фосфолипиды клеточных мембран выступают как катализаторы взаимодействия и активации факторов свертывания, ускоряя
течение гемокоагуляции.
Коагуляционный механизм гемостаза.
Процесс свертывания крови (гемокоагуляция) заключается в переходе растворимого белка плазмы крови фибриногена в нерастворимое состояние –фибрин. В результате процесса свертывания кровь из жидкого состояния переходит в студнеобразное, образуется сгусток, который закрывает просвет поврежденного сосуда.
Кровяные пластинки (тромбоциты): размеры, строение, функции, продолжительность жизни.
Тромбоциты представляют собой свободно циркулирующие в крови безъядерные фрагменты цитоплазмы гигантских клеток красного костного мозга — мегакариоцитов. Размер тромбоцитов 2—3 мкм, их количество в крови составляет 200-300х109л. Каждая пластинка в световом микроскопе состоит из двух частей: хромомера, или грануломера (интенсивно окрашенная часть), и гиаломера (прозрачная часть). Хромомер находится в центретромбоцита и содержит гранулы, остатки органелл (митохондрии, ЭПС), а также включения гликогена.
Гранулы делятся на четыре вида.
1. а-гранулы содержат фибриноген, фибропектин, ряд факторов свертывания крови, ростовые факторы, тромбоспондин (аналог актомиозинового комплекса, участвует в адгезии и агрегации тромбоцитов) и другие белки. Окрашиваются азуром, давая базофилию грануломера.
2. Второй тип гранул называется плотными тельцами, или 5-гранулами. Они содержат серотонин, гистамин (по-ступающие в тромбоциты из плазмы), АТФ, АДФ, кальцин, фосфор, АДФ вызывает агрегацию тромбоцитов при повреждении стенки сосуда и кровотечении. Серотонин стимулирует сокращение стенки поврежденного кровеносного сосуда, а также вначале активирует, а затем ингибирует агрегацию тромбоцитов.
3. λ-гранулы — типичные лизосомы. Их ферменты выбрасываются при ранении сосуда и разрушают остатки неразрешенных клеток для лучшего прикрепления тромба, а также участвуют в растворении последнего.
4. Микропероксисомы содержат пероксидазу. Их количество невелико.
Кроме гранул в тромбоците есть две системы канальцев: 1) канальцы, связанные с поверхностью клеток. Эти канальцы участвуют в экзоцитозе гранул и эндоцитозе. 2) система плотных трубочек. Образуется за счет деятельности комплекса Гольджи мегакариоцита.
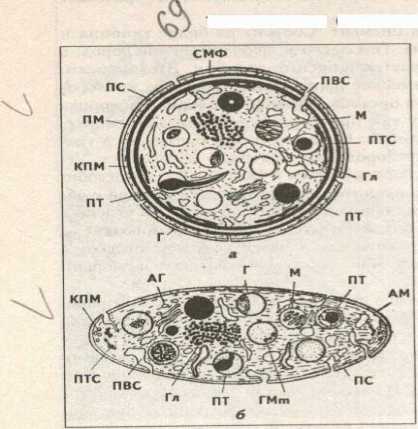
Рис. Схема ультраструктуры тромбоцита:
АГ — аппарат Гольджи, Г — А-гранулы, Гл — гликоген. ГМт — гранулярные микротрубочки, КПМ — кольцо периферических микротрубочек, ПМ — плазматическая мембрана, СМФ — субмембранные микрофиламенты, ПТС — плотная тубулярная система, ПТ — плотные тельца, ЛВС — поверхностная вакуолярная система, ПС — примембраммый слой кислых гликозаминогликанов. М — митохондрии (по Уайту).
Ядерный сдвиг нейтрофилов вправо характеризуется
Патфиз ч.3
ИЗМЕНЕНИЯ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ ПРИ ЛЕЙКОЦИТОЗАХ
Истинные (регенераторные, абсолютные) лейкоцитозы, развивающиеся за счёт усиления пролиферации клеток миелоцитарного ряда, сопровождаются изменениями лейкоцитарной формулы.
Изменения лейкоцитарной формулы обусловлены увеличением или уменьшением в периферической крови числа молодых форм миелоцитарных клеток и появлением форм, в норме в ней отсутствующих. В таком случае говорят об изменении соотношения зрелых и незрелых форм лейкоцитов — о ядерном сдвиге гранулоцитов влево или вправо. Применение этих терминов связано с расположением названий молодых форм нейтрофилов (палочкоядерных, метамиелоцитов, миелоцитов, промиелоцитов) в левой части лабораторного бланка, а зрелых — в их правой части.
ЯДЕРНЫЕ СДВИГИ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ
Поскольку при микроскопии мазка крови основным критерием для идентификации разных форм зрелости зернистых лейкоцитов является характер ядра (форма, размер, интенсивность окраски), сдвиги лейкоцитарной формулы обозначают как «ядерные» (рис. 21–20).
Рис. 21–20. Виды ядерных сдвигов нейтрофилов в лейкоцитарной формуле.
Сдвиг влево характеризуется увеличением количества молодых и незрелых форм нейтрофилов.
Сдвиг вправо проявляется повышением числа сегментированных ядерных форм нейтрофилов.
• Сдвиг вправо
Нередко сочетается с увеличением признаков дегенерации лейкоцитов и уменьшением содержания палочкоядерных нейтрофилов.
• Сдвиг влево
Сдвиги лейкоцитарной формулы нейтрофилов влево определяются появлением незрелых форм нейтрофилов. Различают гипорегенераторный, регенераторный, гиперрегенераторный и регенераторнодегенераторный типы сдвига влево.
† Гипорегенераторный. О нём говорят при увеличении содержания палочкоядерных нейтрофилов выше нормы (более 6%), умеренном лейкоцитозе (обычно до 10–11×109/л).
† Регенераторный. Характеризуется увеличением выше нормы процентного содержания палочкоядерных нейтрофилов, появлением в периферической крови метамиелоцитов, лейкоцитозом до 13–18×109/л.
† Гиперрегенераторный (его иногда тоже обозначают как регенераторный). Проявляется значительным увеличением содержания палочкоядерных нейтрофилов, наличием в периферической крови большого числа метамиелоцитов и появлением миелоцитов, увеличением общего числа лейкоцитов до 20–25×109/л. Вместе с тем общее количество лейкоцитов может быть нормальным или даже сниженным. В отдельных случаях последнее наблюдается после длительного периода значительного лейкоцитоза и обусловлено истощением миелоидного ростка гемопоэтической ткани.
† Регенераторнодегенераторный. Наблюдается при некоторых инфБ, хронических гнойных процессах, протекающих со значительной интоксикацией. Характеризуется более или менее выраженным увеличением уровня палочкоядерных нейтрофилов, метамиелоцитов и миелоцитов, снижением числа сегментоядерных нейтрофилов (как правило), признаками дегенеративных изменений цитолеммы, цитоплазмы и ядра, увеличением общего числа лейкоцитов.
• Индекс ядерного сдвига
Указанные выше изменения соотношения зрелых и незрелых форм нейтрофилов могут быть оценены количественно — путём расчёта индекса ядерного сдвига. Он отражает отношение процентного содержания суммы всех молодых форм нейтрофилов (палочкоядерных, метамиелоцитов, миелоцитов, промиелоцитов) к их зрелым формам.
У здоровых взрослых людей индекс ядерного сдвига колеблется в диапазоне от 0,05 до 0,10. Увеличение его свидетельствует о ядерном сдвиге нейтрофилов влево, уменьшение — о сдвиге вправо.
Перераспределительные и гемоконцентрационные (ложные) лейкоцитозы не сопровождаются изменением лейкоцитарной формулы.
При значительных лейкоцитозах в пунктатах костного мозга и лимфатических узлов отмечаются признаки гиперплазии лимфопоэтической ткани в виде увеличения размеров лимфоидных фолликулов и их зародышевых центров.
ВИДЫ И ЗНАЧЕНИЕ ЛЕЙКОЦИТОЗОВ
Виды и значение лейкоцитозов приведены на рис. 21–21.
Рис. 21–21. Виды лейкоцитозов по их биологическому значению.
• Физиологические лейкоцитозы.
К ним относят большую часть лейкоцитозов. Они характеризуются адаптивным характером и адекватностью факторам, вызывающим их. Среди физиологических лейкоцитозов выделяют функциональные и защитно-приспособительные.
† Функциональный лейкоцитоз. Обусловлен выполнением организмом определённой функции (например, лейкоцитоз во время беременности, увеличение числа лейкоцитов в крови сосудов кишечника после приёма пищи или мышц после длительной физической работы).
† Защитноприспособительный. Развивается при воспалительных процессах, повреждении клеток и тканей (например, после инфарктов или инсультов, травмы мягких тканей), стрессреакции.
В названных и других подобных случаях лейкоцитоз сопровождается активацией функций лейкоцитов, в том числе — одной из важнейших среди них — фагоцитарной. Это способствует повышению резистентности организма к инфекционным и неинфекционным патогенным воздействиям.
• Патологический лейкоцитоз. Наблюдается при лейкозах. Такая разновидность лейкоцитоза, развивающаяся за счёт увеличения числа лейкоцитов опухолевой природы, не имеет адаптивного значения для организма. Лейкозные лейкоциты характеризуются нарушением функциональной активности лейкоцитов: снижена их способность синтезировать и высвобождать цитокины и низка их фагоцитарная активность. В связи с этим у пациентов с лейкозами снижена эффективность реакций иммунитета, нередко развиваются аллергические реакции и болезни иммунной аутоагрессии.
ТИПОВЫЕ ИЗМЕНЕНИЯ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ
Лейкоцитарная формула — численное описание соотношения различных видов циркулирующих в периферической крови лейкоцитов. Изменения лейкоцитарной формулы являются следствием увеличения или уменьшения содержания отдельных видов лейкоцитов и в связи с этим — изменения соотношения между ними.
• Увеличение сверх нормы числа отдельных видов лейкоцитов обозначают терминами нейтрофилия (нейтрофилёз), базофилия, эозинофилия (эозинофилёз), лимфоцитоз, моноцитоз.
• Уменьшение ниже нормального диапазона отдельных разновидностей лейкоцитов обозначают как нейтропения, эозинопения, лимфопения (лимфоцитопения), моноцитопения.
† Агранулоцитоз — отсутствие или значительное снижение абсолютного числа всех видов зернистых лейкоцитов: гранулоцитов (нейтрофилов, эозинофилов и базофилов). Это состояние сочетается, как правило, с лейкопенией.
† Термин «базопения» не употребляют, так как и в норме базофилы могут отсутствовать в периферической крови.
ОТНОСИТЕЛЬНЫЕ И АБСОЛЮТНЫЕ ИЗМЕНЕНИЯ В ЛЕЙКОЦИТАРНОЙ ФОРМУЛЕ
При изменениях относительного (относительно к 100 лейкоцитам, т.е. — процентного) содержания того или иного вида лейкоцитов в лейкоцитарной формуле говорят либо об относительной нейтропении, эозинопении, лимфопении, моноцитопении (при уменьшении процентного содержания лейкоцитов соответствующего вида), либо об относительной нейтрофилии, эозонофилии, относительном моноцитозе, лимфоцитозе (при увеличении их относительного содержания).
Изменения реального (абсолютного) содержания лейкоцитов в единице объёма крови обозначают как абсолютная нейтропения, эозинопения, лимфопения, моноцитопения (при уменьшении их абсолютного числа в единице объёма крови) или абсолютная нейтрофилия, эозинофилия, абсолютный моноцитоз или лимфоцитоз (в случае увеличения количества соответствующих разновидностей лейкоцитов).
При характеристике изменений состава лейкоцитов необходимо оценивать как относительное, так и (обязательно!) абсолютное их содержание.
Это определяется тем, что именно абсолютные величины отражают истинное содержание тех или иных видов лейкоцитов в крови, а относительные характеризуют только соотношение различных клеток между собой в единице объёма крови.
† Во многих случаях направленность изменений совпадает. Часто встречается, например, относительная и абсолютная нейтрофилия или нейтропения.
† Отклонение относительного (процентного) содержания клеток в единице объёма крови не всегда отражает изменение их истинного, абсолютного количества. Так, относительная нейтрофилия может сочетаться с абсолютной нейтропенией (подобная ситуация возникает, если относительная нейтрофилия наблюдается в условиях значительной лейкопении: например, содержание нейтрофилов равно 80%, а общее число лейкоцитов составляет лишь 1,0×109/л).
† Для определения абсолютного количе
Условия, влияющие на течение и исходы кровопотери
• Особенности кровопотери.
† Объём потерянной крови.
‡ Выход из сосудистого русла до 20–25% ОЦК, как правило, не опасен и компенсируется вследствие включения экстренных механизмов компенсации.
‡ Потеря 25–35% ОЦК сопровождается значительными расстройствами центральной, органотканевой и микрогемоциркуляции.
‡ Потеря 50% и более от общего объёма крови (особенно быстрая) является летальной.
† Скорость кровопотери. Чем меньше скорость кровопотери, тем менее выражены расстройства жизнедеятельности. Так, утрата даже половины общего объёма крови в течение нескольких дней (при маточном, желудочном, геморроидальном и других видах кровопотери), как правило, не приводит к смерти.
• Соотношения активности факторов свёртывающей, противосвёртывающей и фибринолитической систем организма. Снижение активности или содержания факторов свёртывающей и/или повышение противосвёртывающей и фибринолитической систем, ведущее к понижению свёртываемости крови может обусловить увеличение скорости и объёма кровопотери, что усугубляет её течение и последствия.
• Реактивность организма. Течение и последствия кровопотери в существенной мере зависят от реактивности организма, определяемой полом (женщины менее чувствительны к кровопотере), возрастом (взрослые переносят кровопотерю легче, чем дети), текущим состоянием организма (при перегревании или охлаждении последствия кровопотери тяжелее, чем при нормальной температуре; в условиях глубокого наркоза расстройства жизнедеятельности более выражены, чем в бодрствующем состоянии).
Патогенез
Механизм развития постгеморрагических состояний представлен на рис. 21–1.
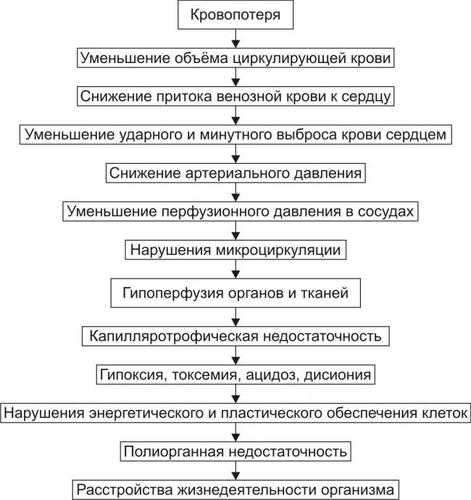
Рис. 21–1. Основные звенья патогенеза постгеморрагических состояний.
На начальном этапе кровопотери в большей или меньшей мере снижается ОЦК при сохранении нормального Ht, т.е. развивается нормоцитемическая гиповолемия. В связи с этим уменьшаются приток венозной крови к сердцу, его ударный и минутный выброс. Это приводит к падению АД и, как следствие, — перфузионного давления в сосудах органов и тканей. В результате уменьшается транспорт кислорода и субстратов метаболизма из крови к клеткам, а от последних — углекислого газа и продуктов обмена веществ. Развивается капилляро-трофическая недостаточность, интоксикация организма продуктами нарушенного метаболизма, гипоксия. Это, в свою очередь, вызывает расстройства энергетического обеспечения клеток и пластических процессов в них. Нарушается функция органов и тканей, что нередко сопровождается выраженной в большей или меньшей мере недостаточностью их. Существенно расстраивается жизнедеятельность организма в целом. Крайняя степень этих расстройств обозначается как постгеморрагический шок.
Нарушение системной гемодинамики и снижение интенсивности биологического окисления в клетках обусловливает включение или активацию адаптивных механизмов.
Адаптивные механизмы
К основным адаптивным механизмам компенсации кровопотери относят:
• Активацию свёртывающей системы крови и процесса тромбообразования.
• Реакции сердечнососудистой компенсации кровопотери (гидремическая компенсация кровопотери): сужение просвета резистивных сосудов, выброс крови из депо, повышение сердечного выброса, поддержание ОЦК на максимально возможном уровне (за счёт поступления в сосуды жидкости из интерстиция, а также — тока лимфы).
• Восстановление белкового состава крови (вследствие синтезов в печени) — реакция белковой компенсации кровопотери.
• Устранение дефицита форменных элементов крови вследствие активации гемопоэза — клеточная, костномозговая компенсация.
• Активация механизмов экстренной и долговременной адаптация к гипоксии (подробнее см. раздел «Адаптивные реакции организма при гипоксии» главы 15 «Гипоксия»).
Нейтрофилез - причины, диагностика и лечение
Классификация
Сами нейтрофильные лейкоциты бывают двух основных видов: сегментоядерные (зрелые) и палочкоядерные (молодые). Палочкоядерные нейтрофилы в норме составляют от 1 до 5% от общего количества лейкоцитов, сегментоядерные – от 35 до 65% . По соотношению молодых и зрелых клеток выделяют нейтрофилезы с ядерным сдвигом и без него. Ядерный сдвиг влево подразумевает увеличение количества молодых форм нейтрофилов и подразделяется на следующие виды:
- Гипорегенераторный. Незначительное увеличение палочкоядерных нейтрофильных лейкоцитов. Причиной являются инфекционные, воспалительные заболевания с легким течением.
- Регенераторный. Характеризуется появлением в крови метамиелоцитов (промежуточных форм между миелобластными клетками и гранулоцитами). Встречается во время инфекций со средней степенью тяжести (брюшной тиф, пневмония).
- Гиперрегенераторный. Выраженная гиперактивация гранулоцитарного ростка костного мозга с нарушением созревания гранулоцитов. В крови резко увеличено число палочкоядерных нейтрофилов, метамиелоцитов, промиелоцитов, иногда присутствуют миелобласты. Возможна анэозинофилия (полное отсутствие эозинофилов). Такая форма нейтрофилеза наблюдается в самом начале гнойно-воспалительных процессов (сепсис, абсцессы, флегмоны).
- Дегенеративный. Наряду с увеличенным числом палочкоядерных лейкоцитов в крови появляется большое количество деструктивно измененных сегментоядерных нейтрофилов (токсическая зернистость, пикноз ядер). Свидетельствует об угнетении функциональной активности костного мозга. Характерен для разгара тяжелых инфекций.
При нейтрофилезе, имеющем ядерный сдвиг вправо, в гемограмме отмечается отсутствие молодых форм гранулоцитов и появление гиперсегментированных (содержащих более 5 сегментов) нейтрофилов. Нейтрофилез без ядерного сдвига сопровождается увеличением только сегментоядерных нейтрофилов. По отношению к другим видам лейкоцитов выделяют:
- Относительный нейтрофилез. Увеличение процентного соотношения нейтрофилов (у взрослых более 75%, у детей до 5 лет – более 55%) в лейкоцитарной формуле, общее количество лейкоцитов нормальное.
- Абсолютный нейтрофилез. Увеличение числа нейтрофилов при одновременном повышении уровня лейкоцитов.
Причины нейтрофилеза
Физиологические причины
Существует так называемый физиологический нейтрофилез, или псевдонейтрофилез. Его возникновение связано не с усилением продукции нейтрофилов, а их перераспределением, т.е. изменением соотношения пристеночного и циркулирующего пула нейтрофилов в сторону последних. Псевдонейтрофилез наблюдается при стрессе, интенсивной физической нагрузке, воздействии тепла или холода, после приема пищи. Также нередко нейтрофилы увеличены во время беременности, у новорожденного ребенка.
Инфекции у детей
У ребенка дошкольного возраста (до 5-6 лет) из-за физиологического снижения уровня нейтрофилов вследствие лейкоцитарного перекреста имеется повышенная восприимчивость к бактериальным инфекциям. У детей нейтрофилы увеличиваются главным образом при скарлатине, стрептококковой ангине. В детской популяции довольно часто встречается такая опасная инфекция, как дифтерия. Также среди дошкольников распространены паразитарные инвазии (аскаридоз, энтеробиоз, токсокароз). При этих заболеваниях помимо нейтрофилеза в крови наблюдается высокая эозинофилия.
Инфекции у взрослых
Наиболее часто нейтрофилы бывают увеличены при бактериальных инфекциях. Основная функция нейтрофилов – противоинфекционная защита макроорганизма, а именно, уничтожение бактерий. Также они принимают участие в борьбе с вирусами, паразитами. Мигрируя через сосудистую стенку, нейтрофилы направляются к очагу локализации патогенного микроорганизма. Выделяя цитокины и медиаторы воспаления, нейтрофилы активируют другие компоненты иммунной системы (комплемент, Т-В-лимфоциты).
Нейтрофильные лейкоциты сначала фагоцитирут (поглощают) инфекционный агент, затем секретирует ферменты деградации (лизоцим, лактоферрин, фосфатазы) и активные формы кислорода (супероксид-анион, гидроксильный радикал, перекись водорода), что способствует гибели микроорганизмов. Нейтрофилез быстро нарастает, достигает максимума параллельно разгару заболевания, постепенно снижается после антибактериальной терапии.
Наиболее распространенной причиной нейтрофилеза у взрослых являются острые локализованные бактериальные (пневмония, синусит, пиелонефрит) или специфические инфекции (брюшной тиф). Для них типичен умеренный нейтрофилез. Реже причиной становятся тяжелые генерализованные инфекции (бактериальный эндокардит, сепсис, менингококковый менингит), характеризующиеся высоким нейтрофилезом с гиперрегенераторным или дегенеративным сдвигом.
Острые хирургические патологии
Довольно часто нейтрофилы бывают увеличены при острой абдоминальной патологии (холецистит, панкреатит, прободение язвы желудка или 12-перстной кишки), гнойных процессах (флегмона, абсцесс). Нейрофилия у ребенка часто встречается при аппендиците. Увеличение числа нейтрофильных лейкоцитов при данных заболеваниях выступает как реакция на воспалительный процесс. Точно установлена коррелирующая связь между тяжестью воспаления и степенью повышения нейтрофилов. Обычно наблюдается высокий нейтрофилез с дегенеративным сдвигом лейкоцитарной формулы влево, который быстро регрессирует после экстренного оперативного вмешательства. Однако нейтрофилы могут оставаться и в пределах нормы.
Повреждение или распад тканей
К таким состояниям относятся инфаркты различных органов (миокарда, легких, кишечника), полостные операции, гангрены, панкреонекроз. Причиной нейтрофилеза является стимуляция продуктами распада гранулоцитопоэза в костном мозге. Дополнительную роль играет реактивная нейтрофилия, возникающая из-за выброса в кровь большого количества гормонов стресса (катехоламинов, глюкокортикостероидов).
Также возникновению нейтрофилеза при данных состояниях способствует присоединение вторичной инфекции (например, пневмонии вследствие инфаркта легкого). Степень нейтрофилеза коррелирует с объемом поврежденной, некротизированной ткани, зачастую достигает очень высоких значений (особенно у ребенка), может сохраняться длительное время, снижается по мере выздоровления.
Ревматологические заболевания
Нейтрофилез может наблюдаться при некоторых хронических воспалительных патологиях ревматической природы. Есть предположение, что медиаторы, цитокины, аутоантитела, которые образуются в процессе ревматического воспаления, стимулируют костномозговую выработку нейтрофильных гранулоцитов. Обычно появление нейтрофилеза наряду с другими лабораторными маркерами, такими как повышенная скорость оседания эритроцитов, С-реактивный белок, свидетельствует об обострении заболевания.
После противовоспалительного лечения концентрация нейтрофилов постепенно возвращается к норме. У взрослых особенно высокий нейтрофилез характерен для острой подагрической атаки, некротизирующих васкулитов (узелкового полиартериита, гранулематоза с полиангиитом). У ребенка нейтрофилы увеличены чаще всего при дерматомиозите.
- Болезни суставов: ревматоидный артрит, анкилозирующий спондилоартрит (болезнь Бехтерева).
- Диффузные болезни соединительной ткани (коллагенозы): системная красная волчанка, системная склеродермия, болезнь Шегрена.
- Воспалительные заболевания кишечника: болезнь Крона, неспецифический язвенный колит.
- Системные васкулиты: неспецифический аортоартериит Такаясу, гигантоклеточный артериит Хортона.
Онкологические заболевания
Нейтрофилез иногда может свидетельствовать о злокачественной опухоли. Его возникновению способствуют два механизма – распад опухолевой ткани и способность некоторых опухолевых клеток секретировать гранулоцитарные колониестимулирующие факторы роста (паранеопластический синдром). Наиболее часто нейтрофилез встречается у пациентов с раком молочной железы, легкого, толстого кишечника, яичников. Нейтрофилез нарастает медленно, по мере роста опухоли, достигает умеренных цифр, постепенно регрессирует после химиотерапии либо быстро приходит в норму после хирургического удаления неоплазии.
Гематологические болезни
Высокий нейтрофилез наблюдается при онкогематологических заболеваниях. Он может достигать очень высоких цифр (до 100 тыс.) при миелопролиферативных болезнях (острый, хронический миелолейкоз). При лимфопролиферативных патологиях (неходжкинские лимфомы, лимфосаркомы) нейтрофилез чуть менее выражен, практически всегда сопровождается абсолютным лимфоцитозом. У ребенка чаще причиной становится лимфогранулематоз (лимфома Ходжкина).
Помимо самого нейтрофилеза, у больных с острыми лейкозами в крови встречается базофильно-эозинофильная ассоциация, большое количество бластных клеток и отсутствие промежуточных форм (лейкемический провал). Механизм нейтрофильного лейкоцитоза лежит в злокачественной трансформации гемопоэтической стволовой клетки. Показатели гранулоцитов приходят в норму только после нескольких курсов полихимиотерапии или пересадки костного мозга.
Редкие причины
- Эндокринные расстройства: болезнь или синдром Иценко-Кушинга, тиреотоксический криз.
- Заболевания крови: гемолитические анемии, истинная полицитемия, злокачественная анемия Аддисона-Бирмера.
- Эндогенная интоксикация: хроническая почечная недостаточность, печеночная недостаточность, диабетический кетоацидоз.
- Феномен гиперактивации костного мозга: после агранулоцитоза, лечения мегалобластной анемии.
- Использование лекарственных препаратов: адреналин, сердечные гликозиды, глюкокортикостероиды, литий.
- Интоксикация ртутью, свинцом.
- Воздействие ионизирующего излучения.
Диагностика
Обнаружение нейтрофилеза требует проведения дифференциальной диагностики. Для этого нужно обратиться к врачу-терапевту. В целях получения первичной информации проводится сбор анамнеза – как давно появились симптомы, имелся ли в последнее время контакт с инфекционными больными, было ли повышение температуры тела, боли, кожные высыпания.
Если есть подозрение на острую хирургическую абдоминальную патологию, обязательно производится пальпация живота на предмет напряженности мышц передней брюшной стенки, наличие положительного симптома Щеткина-Блюмберга. Однако необходимо учитывать, что у ребенка в возрасте до 9 лет данные признаки выявить затруднительно. Для подтверждения диагноза назначается дополнительное обследование, включающее:
- Анализы крови. Проводится подсчет общего количества и процентного содержания всех видов лейкоцитов. Измеряется концентрация эритроцитов, тромбоцитов, воспалительных маркеров (СОЭ, СРБ). Изучается морфология гранулоцитов (токсическая зернистость, кариопикноз). При септическом состоянии определяется уровень пресепсина, прокальцитонина. Проверяется наличие аутоантител (антител к ДНК, топоизомеразе, антинейтрофильные).
- Выявление возбудителя. Для идентификации патогенного микроорганизма проводится бактериологический посев, микроскопия мокроты, мочи, мазка с зева и миндалин. Для диагностики гельминтозов выполняется анализ кала на яйца глист, анализ крови на специфические иммуноглобулины, у ребенка берется соскоб с перианальных складок.
- УЗИ. Признаком пиелонефрита на УЗИ брюшной полости является расширение, уплотнение чашечно-лоханочной системы почек, панкреатита – увеличение, диффузные изменения паренхимы поджелудочной железы, холецистита – утолщение стенок желчного пузыря, часто наличие камней.
- Рентген. На рентгенограммах грудной клетки при пневмонии видны очаги инфильтрации, затемнения. При прободении язвы на снимках находят наличие свободного газа в брюшной полости («симптом серпа»). При воспалительных заболеваниях суставов на рентгене отмечается сужение суставной щели, краевой остеопороз.
- ЭКГ. На электрокардиографии при инфаркте миокарда выявляется подъем сегмента ST, блокада левой ножки пучка Гиса, желудочковая тахикардия, другие нарушения ритма сердца. При тромбоэмболии легочной артерии, приводящей к инфаркту легкого, обнаруживаются признаки перегрузки правых отделов сердца – глубокий зубец Q в III, зубец S в I отведении, высокий остроконечный зубец P (P-пульмонале) в отведениях II, III, aVF.
- Гистологические исследования. Окончательно поставить диагноз онкологического заболевания можно только на основании биопсии. Основной признак солидных опухолей – большое количество атипичных клеток. При лейкозах в биоптате костного мозга отмечают гиперплазию гранулоцитарного ростка, преобладание бластных клеток, в тканях лимфоузла при лимфомах – диффузную пролиферацию клеток с бластной морфологией.
Коррекция
Консервативная терапия
Прямых способов нормализации числа нейтрофильных гранулоцитов не существует. Для борьбы с нейтрофилезом необходимо проводить лечение основного заболевания, на фоне которого он развился. Кратковременная нейтрофилия после еды, стресса или физической работы не требует никакого вмешательства, так как не является признаком болезни или патологического состояния. Нейтрофилез, возникший вследствие оперативного вмешательства, также лечить не нужно. В случае же стойкого нейтрофилеза стоит обратиться к врачу для выяснения причины и назначения дифференцированного лечения:
- Противомикробной (антипаразитарной) терапии. При бактериальной инфекции применяются антибиотики (амоксициллин, цефиксим). При генерализованных инфекциях (сепсис, бактериальный эндокардит) необходимо использовать комбинацию из 2-х антибактериальных препаратов. При глистной инвазии у ребенка назначаются противогельминтные средства (мебендазол).
- Гемореологической терапии. При инфарктах любой локализации, вызванных тромбозами или тромбоэмболиями, применяются антиагрегантные (ацетилсалициловая кислота), антикоагулянтные (низкомолекулярный, нефракционированный гепарин), иногда тромболитические лекарства (алтеплаза).
- Антисекреторной и антиферментной терапии. С целью уменьшения выделения соляной кислоты при язвенной болезни используются ингибиторы протонной помпы (омепразол, пантопразол), h3-блокаторы (фамотидин, ранитидин). Для подавления деструктивного действия протеолитических ферментов поджелудочной железы при остром панкреатите и панкреонекрозе эффективны ингибиторы ферментов (апротинин).
- Противовоспалительного лечения. Для достижения ремиссии ревматологических заболеваний назначаются лекарственные средства, купирующие воспалительный процесс. К ним относятся глюкокортикостероиды (преднизолон), производные 5-аминосалициловой кислоты (сульфасалазин), иммуносупрессанты (циклофосфамид, метотрексат).
- Химиотерапии. Для терапии злокачественных опухолей применяются химиотерапевтические препараты (цитостатики, антиметаболиты, антагонисты гормонов) в сочетании с радиотерапией. При онкогематологических болезнях необходима комбинация нескольких противоопухолевых средств.
Хирургическое лечение
Многие заболевания, сопровождающиеся нейтрофилезом (в основном, это острые абдоминальные патологии), требуют экстренного хирургического вмешательства – лапароскопической аппендэктомии, лапаротомии и ушивания язвенного дефекта, холецистэктомии, вскрытия и дренирования гнойника и пр. При миелопролиферативных патологиях в случае неэффективности консервативной терапии прибегают к трансплантации стволовых клеток.
Прогноз
Только по одному нейтрофилезу невозможно предсказать прогноз. Все зависит от заболевания, которое послужило фоном для возникновения нейтрофилии. Например, транзиторное увеличение количества нейтрофилов после стресса, приема пищи или у ребенка в первые сутки жизни носит абсолютно доброкачественный, преходящий характер. И наоборот, тяжелые гнойно-септические патологии, онкологические болезни имеют довольно большую частоту летальных исходов. Поэтому любое превышение референсных значений нейтрофилов (тем более высокое и стойкое) требует обращения к врачу.
Нейтрофильный лейкоцитоз (нейтрофилия)
Нейтрофильный лейкоцитоз – увеличение содержания нейтрофилов в гемограмме свыше 65%
Патологическая нейтрофилия наблюдается при:
острых инфекционных заболеваниях
гнойно-воспалительных процессах
инфаркте миокарда
злокачественных новообразованиях
острой кровопотере
укусах ядовитых насекомых
Физиологическая нейтрофилия бывает при:
Важное практическое значение при интерпретации диагноза и выстраивании тактики лечения имеет определение степени ядерного сдвига в лейкоцитарной формуле. Классификация по этому признаку приведена в учебнике.
Виды нейтрофильного лейкоцитоза (в зависимости от степени ядерного сдвига в лейкоцитарной формуле)
Без ядерного сдвига – увеличивается количество зрелых сегменто-ядерных нейтрофилов на фоне общего лейкоцитоза ( после приема пищи, мышечной работы, кровопотери, при легком течении инфекций).
С ядерным сдвигом влево:
а) с гипорегенераторным (простым) ядерным сдвигом влево – увеличение палочкоядерных нейтрофилов ( более 5%) на фоне нейтрофилии.
Характерен для легкого течения инфекций и воспаления (ангина, малярия, катаральный аппендицит).
б) с регенераторным ядерным сдвигом влево – на фоне нейтрофилии и увеличенного содержания полиморфно-ядерных нейтрофилов обнаруживаются метамиелоциты.
Характерно для гнойно-септических процессов (пневмония, сыпной тиф, скарлатина, дифтерия). Количество лейкоцитов может увеличиться до 12-15-25 Г/л
в) с гипергенераторным ядерным сдвигом влево – появляется еще больше молодых клеток – миелоцитов, промиелоцитов вплоть до бластов; при этом эозинофилы вообще отсутствуют (анэозинофилия).
Это указывает на неблагоприятное течение инфекционных заболеваний и гнойно-септических процессов (ангина)
С дерегенераторным ядерным сдвигом – появляется значительное число
деструктивно измененных сегментоядерных форм (пикноз ядер, токсическая зернистость, вакуолизация и т.д.), что указывает на угнетение функции костного мозга и может быть при тяжелом течении инфекций, эндогенной интоксикации
4. С ядерным сдвигом вправо – в лейкоцитарной формуле появляются гиперсегментированные (более 5 сегментов). Могут быть у практически здоровых людей, анемии Аддисона-Бирмера
Механизмы развития нейтрофильного лейкоцитоза
Увеличение продукции нейтрофилов в костном мозге (развивается в течение нескольких дней).
Ускоренное высвобождение клеток из костного мозга (происходит в течение нескольких часов.
Высвобождение маргинального пула нейтрофилов (развивается в течение нескольких минут).
Снижение выхода нейтрофилов из крови в ткани.
Сочетание факторов.
Нейтрофилия за счет выхода маргинального пула (псевдонейтрофилия, демаргинация)
Такой путь развития нейтрофилии обусловливает возникновение физиологического лейкоцитоза. Развивается при эмоциональной и тяжелой физической нагрузке, при введении катехоламинов (которые увеличивают сердечный выброс). Механизм ее развития связан с возрастанием скорости кровотока по сосудам, в которых лейкоциты занимают краевое положение. При этом возрастает число моноцитов и лимфоцитов.
Острая нейтрофилия развивается вследствие выхода нейтрофилов из костного мозга
Этот механизм реализуется преимущественно при остром воспалении. Он возможен благодаря наличию костномозгового резерва нейтрофилов- сегментоядерных и палочкоядерных форм. Метамиелоциты и миелоциты выходят в кровь только при чрезмерной стимуляции. В случае, когда продукций нейтрофилов в костном мозге нарушена (например, в условиях проведения химиотерапии опухолей), выход палочкоядерных и сегментоядерных клеток даже в условиях действия бактерийного, крово патогенных факторов будет снижен.
Нейтрофилия вследствие ускорения созревания нейтрофилов в костном мозге
Характерна при гнойной инфекции, злокачественных новообразованиях.
Механизм образования нейтрофилов в костном мозге выглядит следующим образом. При воспалении и бактериальной инфекции происходит активирование моноцитов и макрофагов, которые секретируют ИЛ-1 и ФНО-. Эти цитокины стимулируют стромальные фибробласты костного мозга к увеличению секреции ими ГМ-КСФ и Г-КСФ. Эти гемопоэтические ростовые факторы напрямую активируют клетки гранулоцитарного ряда в процессе их созревания, а также стимулируют ускоренный выход лейкоцитов из депо.
В результате скорость гранулоцитопоэза может увеличиваться в 3 раза, например, при гнойной инфекции. Более выраженное увеличение наблюдается при заболеваниях системы крови или при чрезмерной стимуляции (опухоли /опухолевые клетки вырабатывают КСФ/, тяжелые септические заболевания). Таким образом, даже при ускоренном созревании нейтрофилов в костном мозге для этого требуется несколько дней, поэтому максимальный лейкоцитоз развивается при таких состояниях минимум через неделю.
Такой механизм иногда называют хронической нейтрофилией, поскольку происходит повторная продолжительная стимуляция предшественников гранулоцитопоэза. Однако, при длительной и тяжелой инфекции способность костного мозга генерировать нейтрофилы падает, что ведет к развитию нейтропении истощения. При этом снижается не только генерация гранулоцитов костным мозгом, но и уменьшается время их жизни в циркулирующей крови. Нейтропения истощения при тяжелой гнойной бактериальной инфекции – крайне неблагоприятный прогностический признак.
Нейтрофилия вследствие снижения выхода лейкоцитов в ткани
Выход нейтрофила из сосудов в ткани может нарушаться при разных дефектах его строения, когда клетки теряют способность к продвижению через узкие щели между смежными эндотелиоцитами сосуда.
Примером такой патологии могут служить заболевания, связанные с врожденными или приобретенными нарушениями мембраны нейтрофилов. Такие нейтрофилы не могут занимать краевое положение, а следовательно – и выходить за пределы сосудистого русла. В то же время, пролиферация нейтрофилов в костном мозге идет нормально, поэтому любая инфекция вызывает сильнейшую нейтрофилию.
Следует помнить, что нейтрофилия, обусловленная ускоренным освобождением гранулоцитов костным мозгом, снижением его выхода в ткани и мобилизацией маргинального пула, является в определенной степени мерой защиты организма на повреждающее воздействие. Биологический смысл этой реакции вполне понятен. Это один из вариантов элементов неспецифической системной защиты, в ходе которой организм, готовясь к возможному повреждению, быстро создает в крови мобильный пул циркулирующих нейтрофилов. Эти гранулоциты после активации готовы как клеточные эффекторы острого воспаления уничтожить патогенные микроорганизмы, свои омертвевшие либо поврежденные ткани и в конечном счете – локализовать эти повреждения. Однако, лишенное своего защитного значения воспаление может приобретать чисто патогенный характер и служить одной из причин множественной системной недостаточности.
Индекс ядерного сдвига
Сдвиг лейкоцитарной формулы характеризуется индексом ядерного сдвига (ИЯС) — отношением суммы всех несегментированных нейтрофилов (миелоцитов, метамиелоцитов, палочкоядерных) к количеству сегментоядерных клеток (индекс Боброва):
-
ИЯС =
миелоциты + метамиелоциты + палочкоядерные (%)
сегментоядерные (%)
У здоровых взрослых людей индекс ядерного сдвига нейтрофилов колеблется в диапазоне от 0,05 до 0,10. Увеличение его свидетельствует о ядерном сдвиге нейтрофилов влево, уменьшение – о сдвиге вправо.
Перераспределительные и гемоконцентрационные (ложные) лейкоцитозы не сопровождаются изменением лейкоцитарной формулы нейтрофилов.
При значительных лейкоцитозах в костном мозге и лимфатических узлах отмечаются признаки гиперплазии лимфопоэтической ткани в виде увеличения размеров лимфоидных фолликулов и их зародышевых центров.
Реактивные, или регенераторные, лейкоцитозы сопровождаются изменениями в лейкоцитарной формуле. Особое значение приобретают изменения соотношения молодых и зрелых нейтрофилов. Тогда говорят о ядерном сдвиге гранулоцитов. Это название произошло от того, что в формуле крови слева направо указываются различные формы нейтрофилов от молодых к зрелым: промиелоциты — миелоциты — метамиелоциты (юные) — палочкоядерные — зрелые нейтрофилы. Так как эти элементы находятся в левой части лейкоформулы Арнета-Шиллинга, то говорят о сдвиге влево. При увеличении числа гиперсегментированных ядерных форм говорят о ядерном сдвиге вправо (дегенеративный сдвиг вправо), который может сопровождаться лейкопенией и свидетельствовать о подавлении гранулопоэза (лучевая болезнь, дефицит витамина В12 и фолиевой кислоты, цинга).
Особенности лейкоцитарной формулы у детей
Картина белой крови у детей со временем меняется, и даже в одном и том же возрасте количество различных видов лейкоцитов может колебаться в широких пределах. У новорожденных в первые дни жизни наблюдается лейкоцитоз (10–30×109/л) за счет нейтрофилеза (рис. 1). Число нейтрофилов составляет 65–66%, лимфоцитов — 16–34%. К 5–6 дню процентное содержание нейтрофилов и лимфоцитов уравнивается и составляет примерно по 45%. Это расценивается как «первый перекрест» в лейкоцитарной формуле у детей. К концу 1-го месяца жизни число нейтрофилов уменьшается до 25–30%, а лимфоцитов возрастает до 55–60%. В возрасте до 4–5 лет у детей наблюдается лимфоцитоз в связи с формированием их иммунной системы.
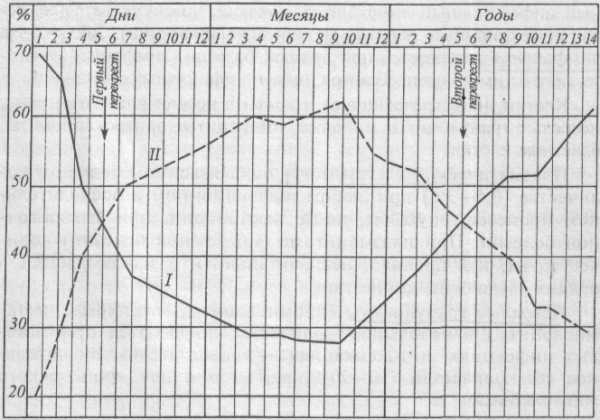 Затем количество нейтрофилов начинает увеличиваться, а лимфоцитов — снижаться, и в возрасте 5–6 лет наблюдается «второй перекрест», когда количества этих клеток вновь уравниваются. К 12–14 годам лейкоцитарная формула детей аналогична формуле взрослых.
Затем количество нейтрофилов начинает увеличиваться, а лимфоцитов — снижаться, и в возрасте 5–6 лет наблюдается «второй перекрест», когда количества этих клеток вновь уравниваются. К 12–14 годам лейкоцитарная формула детей аналогична формуле взрослых.
Рисунок 5 – Схема соотношения количества нейтрофилов и
лимфоцитов в зависимости от возраста
Агранулоцитоз
Клинико-гематологический синдром. Агранулоцитоз – крайне тяжелая степень нейтропении (нейтропения – снижение числа нейтрофилов <1,5х109/л).
Классификация:
-
Врожденный
-
Приобретенный
По течению:
-
Молниеносный
-
Острый
-
Подострый
-
Рецидивирующий
-
Циклический
По механизмам:
-
Иммунный
-
Миелотоксический
Патогенез:
В основе миелотоксического агранулоцитоза лежит угнетающее действие медикаментозных препаратов и других повреждающих факторов на пролиферативную активность гранулоцитарных элементов костного мозга, вследствие чего развивается гипоплазия гранулоцитопоэза; возможность возникновения тяжелой гранулоцитопении при этом определяется суммарной дозой принятого препарата. Миелотоксический агранулоцитоз обычно сочетается с анемией и тромбоцитопенией.
Ведущее значение в патогенезе иммунных (гаптеновых) агранулоцитозов имеет появление в организме антител (агглютинины, лизины и т.д.), действие которых направлено против собственных гранулоцитов периферической крови или их клеток-предшественниц в костном мозгу. Медикаментозные препараты выступают в роли гаптенов, образующих комплексные соединения с белками плазмы и мембран лейкоцитов. Вырабатываемые на образовавшийся «чужеродный» комплекс (антиген) антитела, фиксируясь на поверхности клеток, вызывают их разрушение. Как правило, при иммунном агранулоцитозе снижается содержание только лейкоцитов.
Клинические проявления агранулоцитоза: язвеннонекротическая ангина, развивающаяся вследствие подавления защитных реакций организма (снижения резистентности к бактериальной флоре).
Нейтрофилия — Википедия
Материал из Википедии — свободной энциклопедии
Нейтрофилез (или нейтрофилов лейкоцитоз) представляет собой патологическое состояние, при котором у человека наблюдается высокое содержание нейтрофильных гранулоцитов в крови.[1]
Данное патологическое состояние может возникать при острых инфекционных заболеваниях, гнойных воспалительных процессах, инфаркте миокарда, укусах ядовитых насекомых, после острой кровопотери, а также при алиментарном и эмоциональном физиологических лейкоцитозах. Важное практическое значение имеет определение степени ядерного сдвига в лейкоцитарной формуле.
По данному критерию выделяют шесть видов нейтрофильного лейкоцитоза:
- без ядерного сдвига — увеличение количества зрелых сегментоядерных нейтрофилов на фоне общего лейкоцитоза;
- с гипорегенеративным ядерным сдвигом влево — увеличение содержания палочкоядерных форм нейтрофилов (свыше 5 %) на фоне нейтрофилии; характерен для легкого течения ряда инфекций и воспалений;
- с регенеративным ядерным сдвигом влево — на фоне нейтрофилии и увеличенного содержания палочкоядерных форм обнаруживаются метамиелоциты; общее количество лейкоцитов, как правило, увеличено; характерен для гнойно-септических процессов;
- с гиперрегенеративным ядерным сдвигом влево — характеризуется появлением в гемограмме ещё более молодых форм лейкоцитов (миелоциты и даже отдельные промиелоциты и миелобласты), при этом эозинофилы часто вообще отсутствуют (анэозинофилия). Подобная картина является тревожным показателем, указывающим на неблагоприятное течение инфекционных и гнойно-септических заболеваний;
- с дегенеративным ядерным сдвигом влево — повышение содержания палочкоядерных нейтрофилов сопровождается появлением значительного числа деструктивно измененных сегментоядерных форм (пикноз ядер, токсогенная зернистость и вакуолизация цитоплазмы и т. д.). Дегенеративный ядерный сдвиг влево является показателем угнетения функциональной активности костного мозга и может иметь место при тяжелом течении инфекционных заболеваний, при эндогенной интоксикации и т. д.;
- с дегенеративным ядерным сдвигом вправо — характеризуется появлением в гемограмме гиперсегментированных (свыше 5 сегментов) нейтрофилов; отмечается при лучевой болезни, злокачественной анемии Аддисона-Бирмера, но в ряде случаев может обнаруживаться и у практически здоровых людей.
ПАТОФИЗИОЛОГИЯ: учебник для медицинских вузов/Под ред. В. В. Новицкого и Е. Д. Гольдберга. — Томск: Изд-во Том. ун-та, 2001.
Сдвиг лейкоцитарной формулы влево или вправо
Чтобы поставить какой-либо точный диагноз, любой из нас проходит такую процедуру, как сдача крови на анализ. В большинстве случаев хватает забора из пальца, но иногда приходится брать биоматериал из вены. Нередко врачи в ходе исследования используют такое определение, как сдвиг лейкоцитарной формулы. Услышав где-либо такое выражение, не каждый сможет понять, о чем, собственно, идет речь.
Стоит заметить, что у каждого человека состав крови носит индивидуальный характер, причем он может изменяться вследствие протекания различных биологических процессов. Об этих изменениях как раз и рассказывает лейкоцитарная формула. И именно о ней дальше и пойдет речь в теме данной статьи.
Что такое лейкоцитарная формула?
В нашей крови насчитывается несколько типов лейкоцитов (более подробно об этом в следующем разделе) и каждый из них выполняет свою задачу. Лейкоцитарная формула, или лейкограмма, является процентным соотношением всех разновидностей кровяных клеток. Она также позволяет определить общий уровень содержания лейкоцитов, тем самым выявляя возможный сдвиг лейкоцитарной формулы. Ничего общего с математикой здесь нет. Благодаря этой формуле можно оценить общее состояние здоровья человека, а также выявить разные вероятные отклонения.
В ряде случаев можно не только распознать заболевание, но и определить степень его протекания с дальнейшим исходом. В большинстве случаев анализ на определение лейкоцитарной формулы назначается с общими исследованиями в ходе планового медицинского обследования, при подозрении на лейкоз, а также в качестве контрольной профилактической меры.
Разновидности лейкоцитов
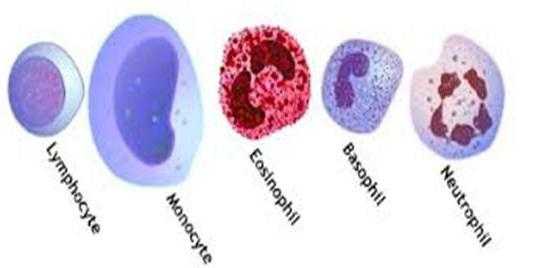
В крови человеческого организма, как выше было упомянуто, присутствует не один вид лейкоцитов. Эти важные клетки, которые борются с инфекционной угрозой и реагируют на повреждение тканей, образуются в костном мозге. Их насчитывается пять видов:
- лимфоциты;
- нейтрофилы;
- моноциты;
- базофилы;
- эозинофилы.
При этом тяжелыми считаются моноциты, базофилы и эозинофилы, а легкими лимфоциты и нейтрофилы. Каждая из этих разновидностей кровяных телец отличается друг от друга не только структурой, но и выполняет свою функцию. Разбирая вопрос, связанный со сдвигом лейкоцитарной формулы, стоит познакомиться с ними поближе.
Лимфоциты – эти клетки принадлежат группе агранулоцитов и представляют собой фундамент нашей иммунной системы. Их главная задача заключается в распознавании и ликвидация чужеродных антигенов, включая раковые клетки. Также они принимают участие в выработке антител. В свою очередь, разделяются на три типа:
- B-клетки;
- T-клетки;
- NK-клетки.
Моноциты – представляют собой клетки, относящиеся к одноядерной лейкоцитной группе. Они имеют овальную форму и содержат ядро крупных размеров, в котором содержится хроматин, большое количество цитоплазмы с множеством лизосом. В зрелом виде имеют диаметр 18-20 мкм. Моноциты отвечают за удаление из организма разрушающихся клеток, а также бактерий и прочих чужеродных тел. Помимо нейтрализации микроорганизмов, участвуют в фагоцитозе.
Нейтрофилы – относятся к гранулоцитарной группе и являются фагоцитами в классическом понимании. Во многом именно по их причине происходит сдвиг лейкоцитарной формулы вправо или влево. Делятся на палочкоядерные и сегментоядерные. Помимо того, что они подвижны, клетки отличаются способностью к хемотаксису и могут захватывать бактерии. Но при этом нейтрофилы поглощают клетки или частицы относительно небольшого размера. Принимают участие в производстве некоторых бактерицидных веществ, выполняя тем самым дезинсекционную функцию.
Базофилы – тоже относятся к гранулоцитарным лейкоцитам и имеет ядро S-образной формы. В большом количестве содержат такие вещества, как:
- гистамин;
- серотонин;
- лейкотриен;
- простагландин.
Гранулы рождаются в костном мозгу и проникают в кровь уже зрелыми. По размеру они довольно крупные, больше чем нейтрофилы и эозинофилы. При возникновении воспалительного процесса, базофилы отвечают за транспортировку белых клеток к месту очага поражения. Еще они принимают активное участие в аллергических реакциях.
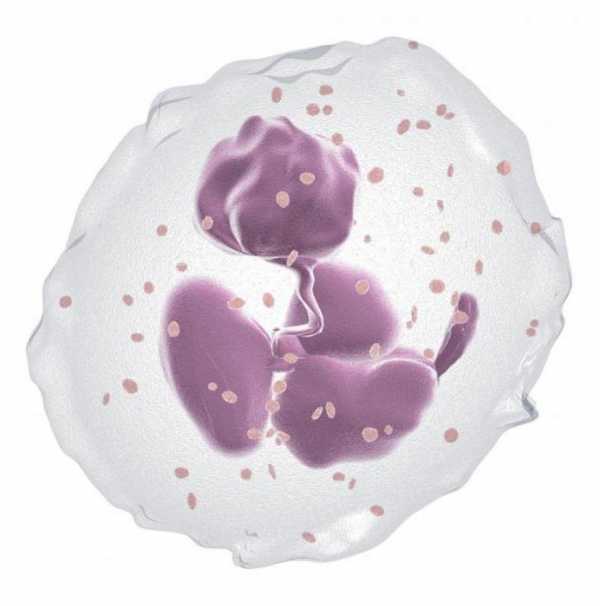
Эозинофилы – также как и нейтрофилы подвижны и участвуют в фагоцитозе. Могут поглощать чужеродные тела, но являясь микрофагами не способны бороться с крупными микроорганизмами. Помимо этого, эозинофилы отличаются способностью поглощать и связывать гистамин и некоторые прочие медиаторы аллергии и воспаления. При необходимости они могут освободить эти вещества подобно тому, как это делают базофилы.
Детский организм
В юном возрасте, в особенности это касательно новорожденных, наблюдается более выраженный сдвиг лейкоцитарной формулы детей. И этому есть простое объяснение – организм ребенка или только что появившегося на свет малыша еще полностью не сформирован и в нем активно протекают разные биологические процессы.
Причем в отличие от взрослых количество лейкоцитов в крови, смотря какого возраста ребенок, разное. На протяжении всего детского периода жизни у ребенка дважды происходит перекрест лейкоцитарной формулы. Первый раз это случается после рождения малыша. Поскольку организм матери выполнял основную защитную функцию для плода, то состав крови новорожденного приближен к показателю нормы у взрослых людей.
Появляясь на свет, малыш сразу же начинает привыкать к окружению, что отражается на различных процессах, протекающих в его организме. К концу первого месяца жизни значительно повышается уровень лимфоцитов.
Находясь в возрасте от года до трех, детский организм отличается нестабильным составом крови. То есть время от времени происходит сдвиг лейкоцитарной формулы влево у детей или же вправо. При этом концентрация лимфоцитов и нейтрофилов может меняться в течение всего дня. Также причиной такой смены могут послужить определенные условия:
- переохлаждение;
- длительная прогулка на солнце;
- хронические заболевания;
- изменения на генном уровне.
С 4 до 6 лет нейтрофилы выходят на лидирующую позицию. Однако у детей старше 6-7 лет состав крови идентичен параметрам взрослых. В течение всего этого периода гормональных изменений может наблюдаться сдвиг формулы на 10-15%, что является нормой.
Более наглядную картину покажет таблица ниже.
Возраст | Наименование клеток крови | Норма, % |
Новорожденные | лимфоциты | 20-35 |
нейтрофилы | 65 | |
моноциты | 3-5 | |
базофилы | 0-1 | |
эозинофилы | 1-2 | |
Первый месяц жизни | лимфоциты | 65-70 |
нейтрофилы | 20-25 | |
моноциты | 3-6 | |
базофилы | 1-2 | |
эозинофилы | 0,5-1 | |
от 1 до 3 лет | лимфоциты | 35-55 |
нейтрофилы | 32-52 | |
моноциты | 10-12 | |
базофилы | 0-1 | |
эозинофилы | 1-4 | |
от 4 до 6 лет | лимфоциты | 33-50 |
нейтрофилы | 36-52 | |
моноциты | 10-12 | |
базофилы | 0-1 | |
эозинофилы | 1-4 | |
Старше 6-7 лет | лимфоциты | 19-35 |
нейтрофилы | 50-72 | |
моноциты | 3-11 | |
базофилы | 0-1 | |
эозинофилы | 1-5 |
Благодаря таким изменениям формируется иммунитет детского организма, в то время как ребенок знакомится и познает окружающий его мир.
Вероятные отклонения от нормы у детей
Каждый тип лейкоцита уникален по своей природе в силу индивидуальной роли в организме. Любые отклонения, которые претерпевает лейкоцитарная формула, сдвиг влево и вправо, свидетельствует о наличии какого-либо заболевания.
Повышенный уровень лимфоцитов или лимфоцитоз наблюдается в случае возникновения вирусной и бактериальной инфекции (коклюша, гриппа, краснухи, кори, туберкулеза). Кроме них, на высокую концентрацию клеток указывает наличие бронхиальной астмы, заболевания аутоиммунного характера (болезнь Крона или Лайма), а также врожденной склонности к аллергии. Кормление ребенка преимущественно углеводистой пищей в первый год его жизни обычно приводит к увеличению численности лимфоцитов. Существенный их недостаток (лимфоцитопения) говорит о том, что костный мозг подвержен воздействию патологии и уже не может воспроизводить кровяные клетки в необходимом количестве.
Высокое содержание нейтрофилов тоже имеет свое название – Нейтрофилез или сдвиг лейкоцитарной формулы влево. В некоторых случаях это объясняется естественной защитной реакцией организма на какую-нибудь угрозу. К примеру, обширный воспалительный процесс и системная красная волчанка (СКВ). Если в организме происходит гормональный сбой, то наступает нейтропения или недостаток нейтрофилов. Но кроме него на это влияет обширная интоксикация организма.
Высокая концентрация моноцитов приводит к моноцитозу, который может появиться вследствие грибкового или вирусного заболевания. Здесь уже о клинической картине можно судить по внешним признакам:
- лимфоаденопатия;
- воспаление носоглотки и гортани с новообразованиями;
- увеличенная печень и характерные болевые ощущения в правом подреберье.
Помимо этого, измененная лейкоцитарная формула со сдвигом влево или вправо, может быть связана с недостатком этих клеток (моноцитопения). Такое часто случается, если организм не получает в достаточном количестве витамины группы B, фолиевую кислоту. Нередко возникает железонедостаточная анемия.
Большое количество базофилов называется базофилией. Однако это явление очень редкое и развивается в единичных случаях. Причиной может быть опасное патологическое изменение такое, как туберкулез, поражение лимфотических узлов, миелолейкоз, онкология крови.
На сдвиг лейкоцитарной формулы может указывать высокий уровень эозинофилов, что происходит по одной из двух возможных причин. Первая заключается в том, при употреблении молочных продуктов, включая лактозу, глютен, проявляется аллергическая реакция. Вторая причина связана с присутствием паразитических червей, на которые долгое время не обращали внимание. Стоит заметить, что эозинофилию невозможно определить по внешним признакам. Но процесс может протекать в стремительном темпе и породить необратимые процессы.
Показания к сдаче анализа
Показанием для сдачи крови в целях определения лейкоцитарной формулы являются такие случаи:
- Обязательное обследование у врача, которое следует проходить ежегодно.
- При наличии осложнения после заболевания.
- Если наблюдается сильная утомляемость.
Как отмечают многие специалисты, не стоит недооценивать такой анализ крови. Сдвиг лейкоцитарной формулы позволит диагностировать практически любое заболевание острого или хронического характера, включая онкологию.
Только исследование даст точные ответы, если его проводить в комплексе с другими анализами. Только в этом случае можно поставить точный диагноз заболевания, а также его развитие и исход.
Процедура анализа
Перед тем как пройти процедуру сдачи крови с целью определить лейкоцитарную формулу, нужна подготовка. Она несложная, ведь все что требуется это не принимать пищу за 3-4 часа до анализа и исключить употребление алкоголя. Также нужно не злоупотреблять физическими и эмоциональными нагрузками. Для исследования берется венозная кровь.
Переходя непосредственно к работе, лаборант помещает материал на специальную стеклянную пластинку, которую располагает под микроскопом. Далее, определяется лейкоцитарная формула крови, сдвиг влево или вправо выявляется в ходе отсеивания кровяных клеток в количестве нескольких сотен, чтобы можно было определить общий уровень содержания всех лейкоцитов. На следующем этапе следует распределить клетки по всей поверхности. При этом тяжелые гранулы сосредотачиваются по краям, а легкие помещаются в центре.
Зачастую при подсчете белых кровяных телец используются два основных способа:
- Метод Шиллинга – мазок условно делится на 4 части.
- Метод Филипченко – мазок делится на три части.
Расшифровка результата будет готова после нескольких дней исследования, а ее анализом занимается уже лечащий врач.
Расшифровка результатов
Расшифровку лейкоцитарной формулы должен проводит только сотрудник, специально обученный по этому профилю. Но можно просто сравнить полученные результаты с показателями нормы. Зачастую когда анализируется лейкоцитарная формула крови, сдвиги определяются в ходе ручного расчета. Но некоторые клиники пошли современным путем и используют для этого специальное оборудование – анализатор.
Как правило, он работает в автоматическом режиме, но в случае резкого отклонения от нормы, в работу вступает специалист. Для сравнения человек сможет осмотреть 100-200 клеток, аппарат гораздо больше – несколько тысяч. Но, несмотря на то что современное оборудование позволяет производить более точный расчет, ошибки неизбежно случаются. На это могут влиять несколько причин: неправильный забор крови, не так подготовлен мазок и прочие факторы.
Сдвиг формулы влево
Под термином сдвиг лейкоцитарной формулы влево понимается высокая концентрация палочкоядерных нейтрофилов, что говорит о протекании воспалительного процесса. Это еще может происходить из-за:
- Инфекционного заболевания.
- Нарушения кислотно-щелочного баланса.
- Коматозного состояния.
- Физического перенапряжения.
Наряду с увеличением концентрации нейтрофилов, в кровь попадает некоторое количество метамиелоцитов (еще не созревшие лейкоциты).
В здоровом организме они находятся только в красном мозге. Однако из-за сильной воспалительной реакции большинство здоровых нейтрофилов быстро погибает. В этом случае костному мозгу приходится отправлять в очаг поражения еще не созревшие кровяные клетки.
Сдвиг формулы вправо
Под определением сдвиг лейкоцитарной формулы вправо понимается пониженное содержание палочкоядерных нейтрофилов. Но вместе с этим растет число сегментоядерных клеток. Зачастую сопровождается хроническим заболеванием печени, почек, включая мегабластическую анемию. На это также может влиять переливание крови.
Важность лейкоцитарной формулы сложно переоценить, так как большинство изменений, происходящих в организме, приводят к ее сдвигу. Концентрация одних кровяных клеток увеличивается за счет уменьшения количества других.
Показатели нормы
Как уже известно, любое отклонение от нормы предполагает наличие существенных изменений в организме. Нормальные показатели лимфоцитов составляют 19-37 % или 1,2-3х109 шт./л; нейтрофилов (именно сегментоядерных) – 47-72 % или 2-5,5х109 шт./л; палочкоядерных нейтрофилов – 1-6% или 0,04-0,3х109 шт./л; моноцитов – 3-11 % или 0,09-0,6х109 шт./л; базофилов – 0-1 % или 0-0,065х109 шт./л; и наконец, концентрация эозинофилов равна 0,5-5 % или 0,02-0,3х109 шт./л.
На основании данных, полученных с результатов исследования, врач подтверждает либо отвергает предполагаемый диагноз. А если сдвиг лейкоцитарной формулы не произошел и все в пределах нормы, значит, повода для беспокойства не существует.
ПРОЯВЛЕНИЯ ЛЕЙКОЦИТОЗОВ - Патфиз ч.3
ПРОЯВЛЕНИЯ ЛЕЙКОЦИТОЗОВ
Увеличение числа всех форм лейкоцитов или отдельных их видов (лимфоцитов, моноцитов, разных гранулоцитов) в значительной мере определяется характером причинного фактора.
• При аллергических реакциях, как правило, происходит преимущественное увеличение в крови числа эозинофилов (аллерген обусловливает высвобождение из лимфоцитов стимуляторов эозинофильного лейкопоэза — ИЛ5, ИЛ17, фактора хемотаксиса эозинофилов ECF, эотаксина).
• При инфП, вызванных бактериями (в частности, стрептококками, стафилококками) стимулируются миелопоэз и выброс в кровь гранулоцитов, в основном нейтрофилов.
• При внедрении в организм многих вирусов (например, возбудителей коклюша, гепатита) и некоторых микробов (например, возбудителей туберкулёза, сифилиса, бруцеллёза) происходит преимущественная стимуляция лимфопоэза и увеличение числа лимфоцитов в периферической крови. Некоторые вирусы, бактерии и простейшие, вызывающие инфБ (например, инфекционный мононуклеоз, краснуху, бруцеллёз, малярию), активизируют также моноцитопоэз и мобилизацию моноцитов из костного мозга в кровь с развитием моноцитоза.
ИЗМЕНЕНИЯ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ ПРИ ЛЕЙКОЦИТОЗАХ
Истинные (регенераторные, абсолютные) лейкоцитозы, развивающиеся за счёт усиления пролиферации клеток миелоцитарного ряда, сопровождаются изменениями лейкоцитарной формулы.
Изменения лейкоцитарной формулы обусловлены увеличением или уменьшением в периферической крови числа молодых форм миелоцитарных клеток и появлением форм, в норме в ней отсутствующих. В таком случае говорят об изменении соотношения зрелых и незрелых форм лейкоцитов — о ядерном сдвиге гранулоцитов влево или вправо. Применение этих терминов связано с расположением названий молодых форм нейтрофилов (палочкоядерных, метамиелоцитов, миелоцитов, промиелоцитов) в левой части лабораторного бланка, а зрелых — в их правой части.
ЯДЕРНЫЕ СДВИГИ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ
Поскольку при микроскопии мазка крови основным критерием для идентификации разных форм зрелости зернистых лейкоцитов является характер ядра (форма, размер, интенсивность окраски), сдвиги лейкоцитарной формулы обозначают как «ядерные» (рис. 21–20).
Рис. 21–20. Виды ядерных сдвигов нейтрофилов в лейкоцитарной формуле.
Сдвиг влево характеризуется увеличением количества молодых и незрелых форм нейтрофилов.
Сдвиг вправо проявляется повышением числа сегментированных ядерных форм нейтрофилов.
• Сдвиг вправо
Нередко сочетается с увеличением признаков дегенерации лейкоцитов и уменьшением содержания палочкоядерных нейтрофилов.
• Сдвиг влево
Сдвиги лейкоцитарной формулы нейтрофилов влево определяются появлением незрелых форм нейтрофилов. Различают гипорегенераторный, регенераторный, гиперрегенераторный и регенераторнодегенераторный типы сдвига влево.
† Гипорегенераторный. О нём говорят при увеличении содержания палочкоядерных нейтрофилов выше нормы (более 6%), умеренном лейкоцитозе (обычно до 10–11×109/л).
† Регенераторный. Характеризуется увеличением выше нормы процентного содержания палочкоядерных нейтрофилов, появлением в периферической крови метамиелоцитов, лейкоцитозом до 13–18×109/л.
† Гиперрегенераторный (его иногда тоже обозначают как регенераторный). Проявляется значительным увеличением содержания палочкоядерных нейтрофилов, наличием в периферической крови большого числа метамиелоцитов и появлением миелоцитов, увеличением общего числа лейкоцитов до 20–25×109/л. Вместе с тем общее количество лейкоцитов может быть нормальным или даже сниженным. В отдельных случаях последнее наблюдается после длительного периода значительного лейкоцитоза и обусловлено истощением миелоидного ростка гемопоэтической ткани.
† Регенераторнодегенераторный. Наблюдается при некоторых инфБ, хронических гнойных процессах, протекающих со значительной интоксикацией. Характеризуется более или менее выраженным увеличением уровня палочкоядерных нейтрофилов, метамиелоцитов и миелоцитов, снижением числа сегментоядерных нейтрофилов (как правило), признаками дегенеративных изменений цитолеммы, цитоплазмы и ядра, увеличением общего числа лейкоцитов.
• Индекс ядерного сдвига
Указанные выше изменения соотношения зрелых и незрелых форм нейтрофилов могут быть оценены количественно — путём расчёта индекса ядерного сдвига. Он отражает отношение процентного содержания суммы всех молодых форм нейтрофилов (палочкоядерных, метамиелоцитов, миелоцитов, промиелоцитов) к их зрелым формам.
У здоровых взрослых людей индекс ядерного сдвига колеблется в диапазоне от 0,05 до 0,10. Увеличение его свидетельствует о ядерном сдвиге нейтрофилов влево, уменьшение — о сдвиге вправо.
Перераспределительные и гемоконцентрационные (ложные) лейкоцитозы не сопровождаются изменением лейкоцитарной формулы.
При значительных лейкоцитозах в пунктатах костного мозга и лимфатических узлов отмечаются признаки гиперплазии лимфопоэтической ткани в виде увеличения размеров лимфоидных фолликулов и их зародышевых центров.
ВИДЫ И ЗНАЧЕНИЕ ЛЕЙКОЦИТОЗОВ
Виды и значение лейкоцитозов приведены на рис. 21–21.
Рис. 21–21. Виды лейкоцитозов по их биологическому значению.
• Физиологические лейкоцитозы.
К ним относят большую часть лейкоцитозов. Они характеризуются адаптивным характером и адекватностью факторам, вызывающим их. Среди физиологических лейкоцитозов выделяют функциональные и защитно-приспособительные.
† Функциональный лейкоцитоз. Обусловлен выполнением организмом определённой функции (например, лейкоцитоз во время беременности, увеличение числа лейкоцитов в крови сосудов кишечника после приёма пищи или мышц после длительной физической работы).
† Защитноприспособительный. Развивается при воспалительных процессах, повреждении клеток и тканей (например, после инфарктов или инсультов, травмы мягких тканей), стрессреакции.
В названных и других подобных случаях лейкоцитоз сопровождается активацией функций лейкоцитов, в том числе — одной из важнейших среди них — фагоцитарной. Это способствует повышению резистентности организма к инфекционным и неинфекционным патогенным воздействиям.
• Патологический лейкоцитоз. Наблюдается при лейкозах. Такая разновидность лейкоцитоза, развивающаяся за счёт увеличения числа лейкоцитов опухолевой природы, не имеет адаптивного значения для организма. Лейкозные лейкоциты характеризуются нарушением функциональной активности лейкоцитов: снижена их способность синтезировать и высвобождать цитокины и низка их фагоцитарная активность. В связи с этим у пациентов с лейкозами снижена эффективность реакций иммунитета, нередко развиваются аллергические реакции и болезни иммунной аутоагрессии.
ТИПОВЫЕ ИЗМЕНЕНИЯ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ
Лейкоцитарная формула — численное описание соотношения различных видов циркулирующих в периферической крови лейкоцитов. Изменения лейкоцитарной формулы являются следствием увеличения или уменьшения содержания отдельных видов лейкоцитов и в связи с этим — изменения соотношения между ними.
• Увеличение сверх нормы числа отдельных видов лейкоцитов обозначают терминами нейтрофилия (нейтрофилёз), базофилия, эозинофилия (эозинофилёз), лимфоцитоз, моноцитоз.
• Уменьшение ниже нормального диапазона отдельных разновидностей лейкоцитов обозначают как нейтропения, эозинопения, лимфопения (лимфоцитопения), моноцитопения.
† Агранулоцитоз — отсутствие или значительное снижение абсолютного числа всех видов зернистых лейкоцитов: гранулоцитов (нейтрофилов, эозинофилов и базофилов). Это состояние сочетается, как правило, с лейкопенией.
† Термин «базопения» не употребляют, так как и в норме базофилы могут отсутствовать в периферической крови.
ОТНОСИТЕЛЬНЫЕ И АБСОЛЮТНЫЕ ИЗМЕНЕНИЯ В ЛЕЙКОЦИТАРНОЙ ФОРМУЛЕ
При изменениях относительного (относительно к 100 лейкоцитам, т.е. — процентного) содержания того или иного вида лейкоцитов в лейкоцитарной формуле говорят либо об относительной нейтропении, эозинопении, лимфопении, моноцитопении (при уменьшении процентного содержания лейкоцитов соответствующего вида), либо об относительной нейтрофилии, эозонофилии, относительном моноцитозе, лимфоцитозе (при увеличении их относительного содержания).
Изменения реального (абсолютного) содержания лейкоцитов в единице объёма крови обозначают как абсолютная нейтропения, эозинопения, лимфопения, моноцитопения (при уменьшении их абсолютного числа в единице объёма крови) или абсолютная нейтрофилия, эозинофилия, абсолютный моноцитоз или лимфоцитоз (в случае увеличения количества соответствующих разновидностей лейкоцитов).
При характеристике изменений состава лейкоцитов необходимо оценивать как относительное, так и (обязательно!) абсолютное их содержание.
Это определяется тем, что именно абсолютные величины отражают истинное содержание тех или иных видов лейкоцитов в крови, а относительные характеризуют только соотношение различных клеток между собой в единице объёма крови.
† Во многих случаях направленность изменений совпадает. Часто встречается, например, относительная и абсолютная нейтрофилия или нейтропения.
† Отклонение относительного (процентного) содержания клеток в единице объёма крови не всегда отражает изменение их истинного, абсолютного количества. Так, относительная нейтрофилия может сочетаться с абсолютной нейтропенией (подобная ситуация возникает, если относительная нейтрофилия наблюдается в условиях значительной лейкопении: например, содержание нейтрофилов равно 80%, а общее число лейкоцитов составляет лишь 1,0×109/л).
† Для определения абсолютного количества того или иного вида лейкоцитов в крови необходимо рассчитать эту величину исходя из знания общего числа лейкоцитов и процентного содержания соответствующих клеток (в приведённом примере 80% от 1,0×109/л составит 0,8×109/л. Это более чем в два раза меньше 2,0×109/л — нижней границы нормального абсолютного содержания нейтрофилов).
СДВИГИ ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ
При оценке сдвигов лейкоцитарной формулы исходят из того, что в периферической крови могут появляться нейтрофильные лейкоциты разной степени зрелости (метамиелоциты, миелоциты, промиелоциты, миелобласты). При этом определяют (см. выше «Индекс ядерного сдвига») наличие и степень изменения соотношения зрелых и молодых форм указанных гранулоцитов. Изменения обозначают как сдвиг лейкоцитарной формулы нейтрофилов вправо или влево.
Значение
Анализ лейкоцитарной формулы (выявление изменений абсолютного содержания нейтрофилов, эозинофилов и других лейкоцитов, оценка направленности и выраженности нейтрофильного сдвига) позволяет определить наличие и вид лейкоцитоза или лейкопении по клеточному составу, степень сдвигов в содержании и соотношении отдельных форм лейкоцитов, возможный механизм их возникновения.
Так, увеличение общего числа лейкоцитов в сочетании с абсолютной нейтрофилией свидетельствует о регенераторном (истинном) нейтрофильном лейкоцитозе. Если повышение общего числа лейкоцитов сопровождается абсолютной нейтро и эозинофилией, имеет место регенераторный смешанный — нейтрофильноэозинофильный лейкоцитоз. Снижение общего содержания лейкоцитов в сочетании с абсолютной лимфопенией — признак истинной лимфоцитарной лейкопении и т.д.
Наличие выраженного ядерного сдвига нейтрофилов влево при нейтрофильном лейкоцитозе обычно свидетельствует об истинной (регенераторной) природе этого лейкоцитоза, а отсутствие такого сдвига чаще наблюдается при перераспределительном механизме развития нейтрофильного лейкоцитоза или при нейтрофильной лейкопении.
ПАТОФИЗИОЛОГИЯ ТРОМБОЦИТОВ
Характеристики тромбоцитов и тромбоцитопоэза приведена в статьях «Тромбоциты» и «Гемопоэз» (см. приложение «Справочник терминов» на компакт диске).
Изменения в системе тромбоцитов, как правило, сопровождаются расстройством жизнедеятельности организма в целом и заключаются в увеличении их количества в единице объёма крови выше нормы (тромбоцитозы), либо уменьшении их числа в единице объёма крови ниже нормального уровня (тромбоцитопении), либо изменении функциональных свойств пластинок (тромбоцитопатии), либо, наконец, в сочетании указанных отклонений.
ТРОМБОЦИТОЗЫ
Тромбоцитозы — состояния, характеризующиеся увеличением числа тромбоцитов в единице объёма крови выше 320–340×109/л.
Виды тромбоцитозов. По механизму развития различают абсолютные и относительные тромбоцитозы, а среди последних выделяют перераспределительные и гемоконцентрационные.
АБСОЛЮТНЫЕ ТРОМБОЦИТОЗЫ
Абсолютные (истинные, пролиферативные) тромбоцитозы характеризуются возрастанием числа тромбоцитов в крови в результате их повышенного образования.
• Причины:
† Генные дефекты. Классический пример: миелопролиферативный идиопатический тромбоцитоз.
† Увеличение концентрации и/или активности стимуляторов тромбоцитопоэза: тромбоспондина, тромбопоэтина, FAT, ИЛ3, ИЛ6, ИЛ11.
† Опухолевая трансформация мегакариобластов под влиянием канцерогенов с последующей интенсификацией тромбоцитопоэза при гемобластозах. Это наблюдается, например, при мегакариобластных лейкозах. При этом возможно значительное (в 10–15 раз превышающее нормальный уровень) и длительное увеличение числа тромбоцитов в периферической крови.
ОТНОСИТЕЛЬНЫЕ ТРОМБОЦИТОЗЫ
Относительные (ложные, непролиферативные) тромбоцитозы не сопровождаются увеличением общего числа тромбоцитов в крови.
• Причины:
† Перераспределение тромбоцитов в различных регионах сосудистого русла. Так, число тромбоцитов увеличивается в участках микрососудов с повреждёнными стенками (например, при васкулитах), в первые часы после острой кровопотери, длительного стресса, ожогов, травмы (за счёт выброса крови из депо и выхода из костного мозга).
† Гемоконцентрация — увеличение относительной массы тромбоцитов при неизменном или сниженном объёме плазмы крови. Это может наблюдаться в результате плазморрагии (например, при обширных ожогах) или при значительной потере жидкости (например, у пациентов с длительной диареей, рвотой, при продолжительном интенсивном потоотделении).
ЗНАЧЕНИЕ ТРОМБОЦИТОЗОВ
• Адаптивное значение тромбоцитозов заключается в образовании тромбоцитарного сгустка и в дальнейшем — тромба (например, при нарушении целостности стенки сосуда) и в поддержании оптимального метаболизма в клетках эндотелия и их целостности за счёт выделения при контакте с ними ангиогенных факторов.
• Патогенное значение тромбоцитозов характеризуются избыточной активацией коагуляции белков крови и процесса тромбообразования с нарушением микроциркуляции в тканях (например, при тромбоцитозе у пациентов с мегакариобластным лейкозом).
ТРОМБОЦИТОПЕНИИ
Тромбоцитопении — состояния, характеризующиеся уменьшением количества тромбоцитов в единице объёма крови ниже нормы, как правило, менее 180–150×109/л. К тромбоцитопениям относятся также самостоятельные заболевания и некоторые синдромы, сопутствующие другим болезням.
ПРИЧИНЫ
Тромбоцитопении могут быть вызваны различными факторами физической, химической и биологической природы (см. раздел «Этиология и патогенез» в статье «Тромбоцитопении» приложения «Справочник терминов» на компакт диске).
МЕХАНИЗМ РАЗВИТИЯ
Механизм развития тромбоцитопений заключается в реализации одного или нескольких из следующих процессов (рис. 21–22):
Рис. 21–22. Основные механизмы развития тромбоцитопений.
• Подавление тромбоцитопоэза. Обусловливает абсолютную гипорегенераторную тромбоцитопению. Это может наблюдаться при гемобластозах; метастазах новообразований в костный мозг, лучевой болезни, применении некоторых ЛС (например, тиазидных диуретиков или химиотерапевтических препаратов), избирательно подавляющих созревание мегакариоцитов; дефиците витамина B12 или фолиевой кислоты, врождённом дефиците мегакариоцитарных колониеобразующих единиц в костном мозге (вследствие этого развивается амегакариоцитарная тромбоцитопения).
• Повышенное разрушение тромбоцитов (см. раздел «Этиология и патогенез» в статье «Тромбоцитопении» приложения «Справочник терминов» на компакт диске).
• Массированное «потребление» тромбоцитов. Выявляется при генерализованном тромбообразовании (например, при ДВС-синдроме на этапе образования большого числа тромбов).
• Избыточное депонирование тромбоцитов в селезёнке. Этот синдром обозначают как гиперспленизм. В норме в селезёнке содержится около 30% всего пула тромбоцитов. Увеличение размеров селезёнки (спленомегалия) обусловливает депонирование значительного числа тромбоцитов с исключением их из системы гемостаза. При значительном увеличении селезёнки возможно депонирование 90% всего пула тромбоцитов. Оставшиеся в кровотоке тромбоциты имеют нормальную продолжительность циркуляции. Гиперспленизм характеризуется умеренной тромбоцитопенией, нормальным количеством мегакариоцитов в костном мозге и значительным увеличением селезёнки.
ПРОЯВЛЕНИЯ ТРОМБОЦИТОПЕНИЙ
• Костный мозг.
† Гиперплазия костного мозга. Проявляется увеличением в нём числа мегакариобластов и мегакариоцитов. Наблюдается при повышенном разрушении или генерализованном «потреблении» тромбоцитов.
† Гипоплазия костного мозга. Выявляется у пациентов с гемобластозами (лейкозами), лучевой болезнью, метастазами опухолей (не относящихся к гемобластозам) в костный мозг.
† Снижение содержания гликогена и активности ряда ферментов (например, лактатдегидрогеназы, глюкозо–6фосфат дегидрогеназы) в мегакариобластах и мегакариоцитах, что уменьшает продолжительность жизни тромбоцитов.
• Периферическая кровь: уменьшение числа тромбоцитов и увеличение их размеров при обычно нормальном количестве эритроцитов, Hb, лейкоцитов. При выраженном геморрагическом синдроме возможно развитие анемии.
• Система гемостаза. Проявления тромбоцитопений в системе гемостаза представлены на рис. 21–23.
Рис. 21–23. Изменения в системе гемостаза при тромбоцитопениях.