Симптомы рецидива лимфомы ходжкина
Рецидив лимфомы | Запись на приём к онкологу
Рецидив лимфомы
Злокачественные новообразования могут возникать повторно даже после проведения оперативного вмешательства и комплексной терапии. Так, у пациентов нередко диагностируют рецидив лимфомы даже на фоне длительной ремиссии. Повторный рост опухоли часто обусловлен тем, что во время операции хирургу не удается полностью удалить злокачественные ткани. Кроме того, ни один метод лечения онкологии не гарантирует полного выздоровления. Консультация онколога поможет пациенту узнать больше о такой патологии, как лимфома: рецидив, лечение, осложнения, частота возникновения, рецидив лимфобластного лейкоза и возможности профилактики.
Информация о патологическом состоянии
В медицинской литературе лимфомой называют распространенный тип гематологического заболевания, при котором возникает злокачественное разрастание лимфоцитов. Болезнь характеризуется изменением морфологии клеток и распространением патологического очага в организме. Чаще всего на фоне лимфомы у пациента возникает увеличение одного или нескольких лимфатических узлов, однако опухоли лимфоцитарного происхождения также могут возникать в других органах. Частота встречаемости такой патологии зависит от возрастной категории. Так, например, у детей рецидив лимфомы или первичная опухоль входит в тройку самых распространенных онкологических заболеваний.
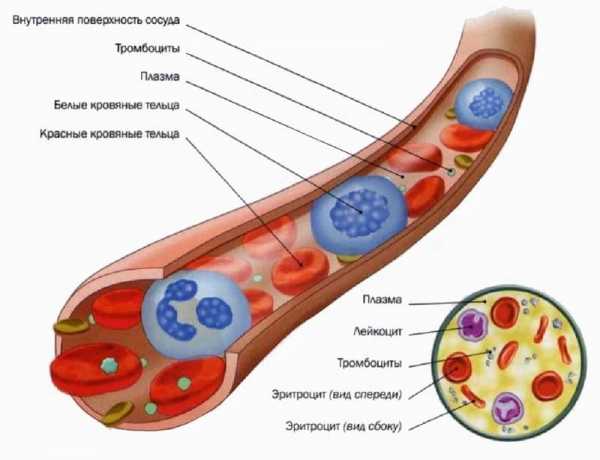
Лимфоциты – это клетки иммунной системы, являющиеся разновидностью белых кровяных телец (лейкоцитов). В зависимости от своего функционального типа лимфоциты выделяют антитела для уничтожения патогенных агентов или непосредственно избавляют организм от бактерий и других болезнетворных организмов. Эти клетки выделяются в красном костном мозге, после чего проникают в кровоток и инфильтруют ткани. Большое количество лимфоцитов можно обнаружить в лимфатических узлах, где происходит созревание иммунологических клеток. В свою очередь, функция лимфатических узлов связана с дренированием жидкости из органов и тканей с последующей задержкой болезнетворных клеток и веществ. Эти органы распространены во всех анатомических областях.
8 (495) 320-19-03
Круглосуточно без выходных
Ученым известные разные типы лимфом. Главным критерием классификации является гистологическая форма новообразования, поскольку от этого признака зависят особенности протекания болезни. Двумя основными категориями лимфоцитарных опухолей являются лимфомы Ходжкина и неходжкинские новообразования. Также Всемирная организация здравоохранения включает в классификацию множественные миеломы и иммунопролиферативные заболевания. Согласно эпидемиологическим данным, около 90% всех выявленных лимфоцитарных опухолей являются неходжкинскими лимфомами.
Отдельные виды:
- Новообразование Ходжкина или лимфогранулематоз – патология, для которой характерно массовое образование так называемых гигантских клеток Штернберга. Рецидив лимфомы Ходжкина может возникать достаточно часто.
- Неходжкинская лимфома, рецидивы которой также встречаются. Это разнообразная группа лимфоцитарных заболеваний, развивающихся из разных клеток.
- Лимфома Беркитта. Рецидив для этой патологии характерен в большей степени из-за агрессивного течения и быстрого распространения злокачественных клеток в другие анатомические области. При этом поражаются B-лимфоциты.
Как и в случае других онкологических заболеваний, актуальной проблемой является поздняя диагностика лимфоцитарных опухолей. Проведение регулярных обследований для пациентов из группы риска помогает решить такую проблему и даже предотвратить рецидив лимфомы после лечения.
Причины возникновения
Этиология опухолей лимфоцитарного происхождения до конца не изучена. Врачам лишь известны различные факторы предрасположенности болезни, которые связаны с индивидуальным анамнезом пациентов и наследственностью. Предполагается, что некоторые внутренние и внешние негативные факторы могут быть связаны с этиологией лимфом. При этом своевременное обнаружение у больного предрасположенности к онкологическому процессу важно для назначения профилактики и скрининговых обследований.
Рецидив лимфомы развивается несколько иначе, чем первичное новообразование, однако существуют общие патологические механизмы. Изначально из-за длительного воздействия факторов риска отдельные гематологические клетки изменяются. Потеря морфологических признаков и утрата регуляции клеточного цикла приводит к активному делению аномальных лимфоцитов. Постепенно в лимфатическом узле или другом органе формируется злокачественный процесс, быстро распространяющийся на другие ткани. Пусковым фактором патологии может быть экспрессия мутантного гена.
Известные факторы риска:
- Возраст пациента. Некоторые виды лимфоцитарных новообразований чаще встречаются у молодых людей, однако обычно подобные заболевания диагностируют у пациентов старше 55 лет. Стоит упомянуть и то, что рецидив после лимфомы Ходжкина может быть выявлен как в возрасте от 20 до 35, так и у больных после 55 лет.
- Половая принадлежность пациента. У мужчин такие заболевания встречаются чаще.
- Нарушение работы иммунной системы. Защитные системы организма могут предотвратить рост некоторых злокачественных новообразований, поэтому расстройство иммунитета нередко приводит к онкогенезу.
- Возникновение определенных инфекционных заболеваний. Это вирус Эпштейна-Барра, ВИЧ/СПИД (вирус поражает лимфоциты) и даже Helicobacter pylori.
- Воздействие некоторых иммунодепрессантов и пестицидов.
- Употребление большого количества красного мяса и курение.
- Рецидив лимфомы в анамнезе близких родственников пациента.
К сожалению, факторы риска лимфоцитарных опухолей изучены не так хорошо, как причины других онкологических заболеваний. Врачам известны лишь отдельные виды предрасположенности к болезни. Тем не менее проведение регулярной диагностики для пациентов из группы риска помогает вовремя обнаруживать заболевание и проводить эффективное лечение.
8 (495) 320-19-03
Круглосуточно без выходных
Стадии и рецидив лимфомы
Особенности прогрессирующего течения лимфоцитарного новообразования зависят от конкретного типа патологии. В целом, механизм развития болезни обусловлен увеличением размера злокачественных тканей и распространением аномальных лимфоцитов в организме. На определенном этапе у пациента обнаруживают вторичные опухоли. Наиболее эффективное лечение доступно при локализованной стадии, когда врач может провести оперативное вмешательство для иссечения злокачественных тканей.
Стадии неходжкинских лимфом:
- Первая стадия. Новообразование обнаружено в одном лимфатическом узле или в одном органе.
- Вторая стадия. Злокачественные ткани в одной или нескольких группах лимфатических узлов на одной стороне тела.
- Третья стадия. Пораженные лимфоузлы расположены по обе стороны диафрагмы.
- Четвертая стадия. Распространение лимфомы на разные органы, включая селезенку, печень и легкие. Возможен рецидив метастаз в лимфоузлах после терапии.
Рецидив рака лимфоузлов может возникать и при достаточном лечении. Дело в том, что отдельные злокачественные клетки могут сохраняться в лимфатических узлах даже после облучения или химиотерапии, поэтому повторный рост опухоли невозможно гарантированно предотвратить. Онкологическим пациентам следует проходить обследования 1-2 раза в год после терапии для исключения возвращения болезни.
Симптомы
Симптоматическая картина может быть разнообразной. Большинство признаков, появляющихся даже на 2-3 стадии, не являются специфическими, поэтому при появлении любых симптомов со стороны иммунной системы следует обратиться к врачу.
Возможные проявления болезни:
- Постоянная усталость.
- Повышение температуры тела (лихорадка).
- Обильное потоотделение в ночное время суток.
- Нарушение дыхания.
- Необъяснимая потеря веса.
- Снижение настроения и апатия.
На поздних стадиях могут появляться признаки поражения других органов метастазами.
Диагностика и лечение
При обнаружении опухших лимфатических узлов или других признаков заболевания необходимо обратиться к онкологу. Во время приема специалист спросит о жалобах, изучит анамнестические данные для выявления предрасположенности к болезни и проведет физикальное обследование. С помощью пальпации можно легко обнаружить увеличенные лимфатические узлы. Следующим этапом диагностики будет проведение инструментальных и лабораторных исследований для уточнения типа и стадии заболевания.
Назначаемые диагностические процедуры:
- Анализ крови для подсчета форменных компонентов и уточнения биохимических показателей.
- Удаление пораженного лимфатического узла для микроскопирования тканей. Биопсия помогает определить гистологический тип опухоли, что очень важно для проведения лечения.
- Биопсия красного костного мозга. С помощью иглы врач получает образец кроветворной ткани и направляет материал в лабораторию. Результаты помогают выявить причину и точную форму лимфомы.
- Визуальная диагностика анатомических областей для выявления опухоли. Это компьютерная и магнитно-резонансная томография.
Предполагаемое лечение:
- Хирургическое удаление опухоли.
- Химиотерапия.
- Лучевая терапия.
- Таргетная терапия.
- Костномозговая трансплантация.
Важно своевременно обратиться к онкологу при появлении первых симптомов, поскольку на ранних стадиях доступны более эффективные методы лечения, включая оперативное вмешательство.
8 (495) 320-19-03
Круглосуточно без выходных
Рецидив лимфомы ходжкина симптомы — ooncologiya
Лимфома Ходжкина (ЛХ) была впервые описана Т. Ходжкиным в 1832 г. у 7 больных как заболевание, при котором имелась генерализованная лимфоаденопатия и поражение селезенки, не связанное с инфекцией, метастазами опухолей или другими заболеваниями.
В дальнейшем С. Березовский, К. Штернберг и Д. Рид описали крупные многоядерные клетки в опухолевом лимфоузле и предположили, что они являются морфологическим субстратом болезни.
На протяжении более чем столетия эта болезнь рассматривалась как хроническое воспалительное заболевание, что отражает старое название-лимфогранулематоз.
Однако, поскольку в клетках Березовского-Штернберга (кБ-Ш) была выявлена анеуплоидия и моноклональность, болезнь Ходжкина, или, по классификации ВОЗ, лимфома Ходжкина, рассматривается как злокачественная опухоль. Заболеваемость ЛХ составляет 1,5-4,5 на 100000 населения в год с некоторым преобладанием мужчин, хотя среди молодых больных преобладают женщины; распределение по возрасту — бимодальное.
Первый пик заболеваемости наблюдается в возрасте 15-30 лет, второй — после 50 лет, хотя первый пик заболеваемости у лиц желтой расы отсутствует. Одним из факторов риска является высокий социально-экономический статус.
Этиология и патогенез ЛХ
Комбинация признаков воспалительной реакции и признаков злокачественного заболевания при лимфоме Ходжкина привело к дебатам о том, какие из признаков имеют опухолевое, а какие — инфекционное происхождение.
Считается, что вирусная инфекция в подростковом возрасте может запустить пролиферацию предопухолевых лимфоидных клеток. В США в 50% случаев ЛХ была выявлена интеграция EBV в геном клеток опухоли. Однако, поскольку не во всех случаях ЛХ положительна на EBV, похоже, что он является только кофактором для пока неизвестного причинного фактора.
Клиническая картина у пациентов с ЛХ, положительных по EBV, не отличается от таковой у пациентов, отрицательных по EBV. Это позволило предположить, что EBV вызывает генетическую нестабильность у предрасположенных пациентов.
В ряде исследований было показано, что патогномоничные для лимфомы Ходжкина кБ-Ш в 80% случаев происходят из зрелых медленно пролиферирующих В-клеток зародышевых центров фолликулов лимфоузла, в 20% они являются дериватами цитотоксических Т-лимфоцитов.
В-клеточное происхождение клеток Ходжкина и кБ-Ш подтверждено клональной реаранжировкой генов Ig с отсутствием экспрессии поверхностного Ig. Соматические мутации с реаранжировкой генов Ig определяются в В-клетках зародышевых или постзародышевых центров в предшественниках кБ-Ш, хотя могут происходить и на других ступенях развития В-лимфоцитов.
Можно предположить, что клетки Ходжкина и кБ-Ш, утратив способность экспрессировать Ig и, избежав апоптоза, получили возможность неконтролируемой пролиферации. Так как эти клетки с нежелательными мутациями не подвергаются апоптозу, можно думать о дисфункции генов, контролирующих апоптоз, а именно, генов р53, BCL-2, MYC или о блокаде передачи «сигнала смерти» через рецепторы CD30 на поверхности кБ-Ш.
Поскольку кБ-Ш в большинстве случаев относятся к линии В-лимфоцитов, они имеют фенотип CD30+, часто CD15+, CD25+, в большинстве случаев CD45-, CD20-. Дополнительно эти клетки имеют маркеры дендритических клеток. Реакция с aнти-CD30-антителами типична для ЛХ, но не специфична, т.к. она положительна с активированными лимфоидными клетками и клетками анапластической крупноклеточной лимфомы.
Клиническая картина
Типичным для начальной стадии ЛХ является постепенное увеличение одного или нескольких лимфоузлов, чаще шейных, менее часто — подмышечных. Поражение паховых или бедренных лимфоузлов в начале заболевания выявляется менее чем в 10% случаев.
Лимфоузлы имеют плотноэластическую консистенцию, не спаяны с кожей, безболезненные. В 2-5% случаев отмечаются боли в пораженных лимфоузлах после приема алкоголя; у 10% пациентов появляется неспецифический зуд кожи. В ранней стадии болезни лимфоузлы могут самопроизвольно регрессировать.
Довольно типичной манифестацией заболевания является увеличение медиастинальных лимфоузлов, что часто выявляется при случайном рентгенисследовании органов грудной клетки, с одышкой или без нее.
Увеличение абдоминальных лимфоузлов или селезенки может проявляться абдоминальным дискомфортом, болями в поясничной области или протекать бессимптомно. Легкие могут вовлекаться в процесс при диссеминации заболевания или инфильтративно при распространении опухоли «per contuitatem».
Поражение легких носит как очаговый, так и инфильтративный характер, иногда с распадом и образованием полостей, в мокроте кБ-Ш обнаруживаются крайне редко. Аускультативная картина крайне скудная. Патогномоничных признаков при поражении печени нет, и достоверно установить диагноз можно только при гистологическом исследовании биоптата печеночной ткани. Поражение костного мозга бывает менее чем у 5% больных.
Его можно предположить при наличии стойкой тенденции к анемии, тромбоцитопении и лейкопении, однако при отсутствии данных симптомов поражение костного мозга устанавливают только при трепанобиопсии; стернальная пункция в большинстве случаев неинформативна. Примерно у 1/3 больных выявляется волнообразная лихорадка с повтором волн через различные промежутки времени.
Считается, что интоксикационный синдром обусловлен цитокинами, секретируемыми в основном кБ-Ш: IL-1, вызывающий лихора
Лимфома Ходжкина - этиология, клиника, диагноз, лечение
Лимфома Ходжкина (ЛХ) была впервые описана Т. Ходжкиным в 1832 г. у 7 больных как заболевание, при котором имелась генерализованная лимфоаденопатия и поражение селезенки, не связанное с инфекцией, метастазами опухолей или другими заболеваниями.В дальнейшем С. Березовский, К. Штернберг и Д. Рид описали крупные многоядерные клетки в опухолевом лимфоузле и предположили, что они являются морфологическим субстратом болезни.
На протяжении более чем столетия эта болезнь рассматривалась как хроническое воспалительное заболевание, что отражает старое название-лимфогранулематоз.
Однако, поскольку в клетках Березовского-Штернберга (кБ-Ш) была выявлена анеуплоидия и моноклональность, болезнь Ходжкина, или, по классификации ВОЗ, лимфома Ходжкина, рассматривается как злокачественная опухоль. Заболеваемость ЛХ составляет 1,5-4,5 на 100000 населения в год с некоторым преобладанием мужчин, хотя среди молодых больных преобладают женщины; распределение по возрасту - бимодальное.
Первый пик заболеваемости наблюдается в возрасте 15-30 лет, второй - после 50 лет, хотя первый пик заболеваемости у лиц желтой расы отсутствует. Одним из факторов риска является высокий социально-экономический статус.
Этиология и патогенез ЛХ
Комбинация признаков воспалительной реакции и признаков злокачественного заболевания при лимфоме Ходжкина привело к дебатам о том, какие из признаков имеют опухолевое, а какие - инфекционное происхождение.Считается, что вирусная инфекция в подростковом возрасте может запустить пролиферацию предопухолевых лимфоидных клеток. В США в 50% случаев ЛХ была выявлена интеграция EBV в геном клеток опухоли. Однако, поскольку не во всех случаях ЛХ положительна на EBV, похоже, что он является только кофактором для пока неизвестного причинного фактора.
Клиническая картина у пациентов с ЛХ, положительных по EBV, не отличается от таковой у пациентов, отрицательных по EBV. Это позволило предположить, что EBV вызывает генетическую нестабильность у предрасположенных пациентов.
В ряде исследований было показано, что патогномоничные для лимфомы Ходжкина кБ-Ш в 80% случаев происходят из зрелых медленно пролиферирующих В-клеток зародышевых центров фолликулов лимфоузла, в 20% они являются дериватами цитотоксических Т-лимфоцитов.
В-клеточное происхождение клеток Ходжкина и кБ-Ш подтверждено клональной реаранжировкой генов Ig с отсутствием экспрессии поверхностного Ig. Соматические мутации с реаранжировкой генов Ig определяются в В-клетках зародышевых или постзародышевых центров в предшественниках кБ-Ш, хотя могут происходить и на других ступенях развития В-лимфоцитов.
Можно предположить, что клетки Ходжкина и кБ-Ш, утратив способность экспрессировать Ig и, избежав апоптоза, получили возможность неконтролируемой пролиферации. Так как эти клетки с нежелательными мутациями не подвергаются апоптозу, можно думать о дисфункции генов, контролирующих апоптоз, а именно, генов р53, BCL-2, MYC или о блокаде передачи «сигнала смерти» через рецепторы CD30 на поверхности кБ-Ш.
Поскольку кБ-Ш в большинстве случаев относятся к линии В-лимфоцитов, они имеют фенотип CD30+, часто CD15+, CD25+, в большинстве случаев CD45-, CD20-. Дополнительно эти клетки имеют маркеры дендритических клеток. Реакция с aнти-CD30-антителами типична для ЛХ, но не специфична, т.к. она положительна с активированными лимфоидными клетками и клетками анапластической крупноклеточной лимфомы.
Клиническая картина
Типичным для начальной стадии ЛХ является постепенное увеличение одного или нескольких лимфоузлов, чаще шейных, менее часто - подмышечных. Поражение паховых или бедренных лимфоузлов в начале заболевания выявляется менее чем в 10% случаев.Лимфоузлы имеют плотноэластическую консистенцию, не спаяны с кожей, безболезненные. В 2-5% случаев отмечаются боли в пораженных лимфоузлах после приема алкоголя; у 10% пациентов появляется неспецифический зуд кожи. В ранней стадии болезни лимфоузлы могут самопроизвольно регрессировать.
Довольно типичной манифестацией заболевания является увеличение медиастинальных лимфоузлов, что часто выявляется при случайном рентгенисследовании органов грудной клетки, с одышкой или без нее.
Увеличение абдоминальных лимфоузлов или селезенки может проявляться абдоминальным дискомфортом, болями в поясничной области или протекать бессимптомно. Легкие могут вовлекаться в процесс при диссеминации заболевания или инфильтративно при распространении опухоли «per contuitatem».
Поражение легких носит как очаговый, так и инфильтративный характер, иногда с распадом и образованием полостей, в мокроте кБ-Ш обнаруживаются крайне редко. Аускультативная картина крайне скудная. Патогномоничных признаков при поражении печени нет, и достоверно установить диагноз можно только при гистологическом исследовании биоптата печеночной ткани. Поражение костного мозга бывает менее чем у 5% больных.
Его можно предположить при наличии стойкой тенденции к анемии, тромбоцитопении и лейкопении, однако при отсутствии данных симптомов поражение костного мозга устанавливают только при трепанобиопсии; стернальная пункция в большинстве случаев неинформативна. Примерно у 1/3 больных выявляется волнообразная лихорадка с повтором волн через различные промежутки времени.
Считается, что интоксикационный синдром обусловлен цитокинами, секретируемыми в основном кБ-Ш: IL-1, вызывающий лихорадку и профузную ночную потливость при ЛХ; фактор некроза опухоли (ФНО)-а и ФНО-в, продуцируемые клетками этой же линии, а также повышение активности простагландина Е2, могут быть причиной интоксикационного синдрома. Дефицит клеточного иммунитета при лимфоме Ходжкина может быть результатом иммуносупрессивного действия в-трансформирующего фактора роста (TGF).
Поражение ЦНС во время установления диагноза выявляется крайне редко и наблюдается обычно при прогрессировании в поздних стадиях болезни (врастание опухоли из лимфоузлов по миелиновым оболочкам).
Характерных изменений в периферической крови нет. У части больных отмечается повышение скорости оседания эритроцитов (СОЭ), иногда тенденция к нейтрофильному лейкоцитозу или лимфоцитопении. При биохимическом исследовании выявляется дисглобулинемия, повышение уровня фибриногена, гаптоглобина, церулоплазмина, острофазовых белков, которые не являются специфическими, но отражают активность процесса. Уровень лактатдегидрогеназы (ЛДГ) повышается редко.
Диагноз и дифференциальный диагноз
При наличии увеличенного лимфоузла более 2,0 см в диаметре или при наличии более мелких лимфоузлов в течение более 6 недель, при наличии интоксикационного синдрома или других признаков злокачественной лимфомы показана биопсия лимфоузла. Дифференциальную диагностику проводят с другими опухолями, НХЛ, реактивными процессами. При подтверждении диагноза ЛХ необходимо определить стадию заболевания.С этой целью проводится обследование, включающее:
- клиническое физикальное обследование,
- лабораторное обследование: общий анализ крови, СОЭ,
- рентгенисследование органов грудной клетки,
- компьютерную томографию шеи, органов грудной клетки и брюшной полости,
- фиброларингоскопию для исключения поражения Вальдейерова кольца,
- трепанобиопсию,
- позитронную эмиссионную томографию для дифференциальной диагностики опухолевых и фибронекротических очагов,
- биопсию печени при подозрении на ее поражение.
Применение лапароскопии с целью уточнения стадии заболевания выполняется крайне редко при отсутствии увеличенных периферических или медиастинальных лимфоузлов, поскольку ее выполнение позволяет изменить стадию только в 20% случаев.
В настоящее время для определения стадий ЛХ используется принятая в Ann-Arbor (1971 г.) классификация в модификации Costwold (1990 г.):
стадия I поражение одной лимфатической зоны или структуры (IE) или локализованное поражение одного экстралимфатического органа или ткани в пределах одного сегмента;
стадия II поражение двух или более лимфатических областей по одну сторону диафрагмы либо локализованное поражение одного экстралимфатического органа или ткани и их регионарных лимфоузлов с поражением других лимфатических областей по ту же сторону диафрагмы или без него (IIE). Указывается число пораженных лимфатических зон;
стадия III поражение лимфоузлов или структур по обе стороны диафрагмы, которое может сочетаться с локализованным поражением одного экстралимфатического органа или ткани (IIIE) либо с поражением селезенки (IIIS) или поражением того и другого (IIIE+S). Рекомендуется выделять верхние абдоминальные лимфоузлы (ворота печени, селезенки) - стадия и нижние (парааортальные, мезентериальные) - стадия III2;
стадия IV диссеминированное (многофокусное) поражение одного или нескольких экстралимфатических органов с поражением лимфоузлов или без него, либо изолированное поражение экстралимфатического органа с поражением отдаленных (не региональных) лимфоузлов. Метастазы в печень и КМ - всегда IV стадия.
Поражение селезенки обозначается символом «S». Символом «Е» обозначается локализованное в пределах одного сегмента экстранодальное поражение. Символ «X» обозначает массивное поражение лимфоузлов. Массивными («bulky disease») предложено считать медиастинальные лимфоузлы при медиастинально-торакальном индексе (МТИ) выше 1/3 или любые другие опухолевые массы диаметром более 10 см.
Отдельно обозначают симптомы интоксикации: символом «В» - наличие одного или более клинических симптомов: профузный ночной пот, температура тела выше 38°С не менее трех дней подряд без признаков воспалительного процесса, снижение массы тела на 10% за последние 6 месяцев; символом «А» - отсутствие указанных выше симптомов.
На симпозиуме в Costwold введен еще один индекс - неуверенная полная ремиссия для обозначения сомнительной полной ремиссии, когда после окончания лечения остаются увеличенные лимфоузлы диаметром не более 1,5 см.
Согласно классификации ВОЗ (2002 г.), гистологически различают 2 группы лимфомы Ходжкина:
- нодулярную форму ЛХ с преобладанием лимфоцитов (5% от всех ЛХ),
- классическую ЛХ.
Последнюю группу подразделяют на 4 варианта:
- лимфоидное преобладание 5-8%,
- нодулярный склероз 35-55%,
- смешанно-клеточный 20-35%,
- лимфоидное истощение 3-4%.
Выделение вариантов имеет большое прогностическое значение. Благоприятными являются варианты лимфоидного преобладания и нодулярного склероза, а смешанно-клеточный и вариант лимфоидного истощения относятся к неблагоприятным вариантам.
Частота вариантов различна в различных странах мира. Нодулярный склероз чаще встречается у молодых женщин, для него характерна большая опухолевая масса лимфоузлов средостения. Вариант лимфоидного преобладания напоминает клинически В-клеточную лимфому низкой степени злокачественности.
Гистологические данные при лимфоме Ходжкина разнообразны и различаются в зависимости от варианта:
- нодулярная форма ЛХ с преобладанием лимфоцитов. Среди реактивных клеток преобладают малые лимфоциты, а типичные кБ-Ш и кХ немногочисленны. Иммунофенотипически этот вариант идентичен смешанно-клеточному и нодулярному склерозу;
- лимфоидное преобладание. Чаще наблюдается нодуляр-ный с реактивной фолликулярной гиперплазией и формированием центров размножения, реже - диффузный характер роста; возможно их сочетание. Превалируют малые лимфоциты с наличием некоторого количества эпителиоидных гистиоцитов. Редко могут встречаться кБ-Ш, но они не экспрессируют CD15. Диагностическими являются крупные лимфоцитарные и гистиоцитарные клетки. Некрозы и фиброз в опухолевой ткани отсутствуют;
- нодулярный склероз. В опухолевой ткани тяжи коллагенизированной бедной фибробластами соединительной ткани кольцевидно окружают опухолевые полиморфноклеточные инфильтраты. Другой особенностью этого варианта является наличие своеобразных «лакунарных» кБ-Ш. Клеточный состав инфильтратов может быть с лимфоидным преобладанием, смешанно-клеточным и с лимфоидным истощением;
- смешанно-клеточный вариант. Характерна диффузная инфильтрация полиморфного состава. Среди реактивных клеток присутствуют лимфоциты, гранулоциты, гистиоциты, эозинофилы, плазматические клетки, фибробласты («рандеву клеток»). Могут встречаться очажки коллагенового фиброза;
- лимфоидное истощение может иметь форму диффузного фиброза или «ретикулярного» подварианта. При диффузном фиброзе бедная фибробластами соединительная ткань вытесняет клеточный инфильтрат. Имеются небольшие скопления лимфоцитов, кБ-Ш и клеток Ходжкина. Реактивные клеточные элементы отсутствуют, но встречаются очаги некрозов.
При «ретикулярном» подварианте в инфильтрате преобладают опухолевые клетки. В разных соотношениях могут присутствовать классические и атипичные кБ-Ш и клетки Ходжкина, а также фибробластоподобные клетки. Отсутствуют переходные формы между мелкими лимфоидными клетками и крупными атипичными. В таких случаях трудно исключить диффузную В-крупноклеточную лимфому (ДВККЛ).
Терапия лимфомы Ходжкина
В последние два десятилетия в терапии всех стадий ЛХ применяется комбинированная химиолучевая терапия. Выбор тактики и объема лечения проводится с учетом группы факторов неблагоприятного прогноза (ФНП) - («факторов риска»), что в определенной степени определяет прогноз заболевания.К ним относятся:
- экстранодальное поражение в пределах, обозначаемых символом «Е»,
- наличие медиастинально-торакального индекса более 1/3,
- массивное поражение селезенки (диффузное поражение или наличие более 5 очагов),
- поражение 3 или более зон лимфоузлов,
- ускорение СОЭ выше 30 мм/час в стадии «В» и выше 50 мм/час в стадии «А»,
- возраст старше 45 лет; мужской пол,
- наличие «bulky disease» - лимфоузлы более 10 см в диаметре,
- анемия, лейкоцитоз, лимфоцитопения,
- низкий уровень альбумина сыворотки - ниже 30 г/л,
- стадия IV лимфомы Ходжкина.
Терапия I-IIA стадий ЛХ
Интерес к лечению ранних стадий ЛХ объясняется тем, что 2/3 больных обращаются за медицинской помощью в стадиях заболевания. В тактике лечения четко прослеживается тенденция к сокращению объема интенсивности терапии у больных с благоприятным прогнозом и интенсификации лечения больных с ФНП.Для больных лимфомой Ходжкина без ФНП ВОНЦ предложена следующая схема терапии: два цикла ABVD + облучение зон исходного поражения в суммарной очаговой дозе (СОД) 30 Гр + два цикла ABVD, поскольку при оценке отдаленных результатов отмечено достоверное преимущество схемы ABVD перед МОРР.
При наличии хотя бы одного ФНП проводится больший объем полихимиотерапии (ПХТ): три цикла ABVD или CVPP + облучение всех лимфатических коллекторов выше диафрагмы в СОД 40 Гр + три цикла по той же схеме. Однако, поскольку у 5% пациентов отмечается прогрессирование процесса, а у 15% - ранние рецидивы, изучается применение более интенсивных режимов: BEACOPP, Stanford V в комбинации с облучением пораженных зон.
Терапия генерализованных (IIB-IV) стадий
Данные стадии предполагают вовлечение в процесс лимфоузлов по обе стороны диафрагмы, а в стадии IV - дополнительное поражение экстралимфатических органов (легкие, печень, костный мозг). После стандартной ПХТ (МОРР, ABVD) отмечаются прогрессирование или рецидивы в 30—Ю% случаев.Поэтому рекомендуется применение одного из протоколов: COPP-ABVD, BEACOPP в стандартных дозах, эскалированный BEACOPP или Stanford V. Обычно первые три протокола предполагают проведение восьми циклов, причем при проведении двух последних протоколов необходимо применение гранулоцитарного колониестимулирующего фактора (Г-КСФ) с 8-го дня каждого цикла до нормализации уровня гранулоцитов.
Уточнение стадии проводилось после четвертого и восьмого циклов ПХТ. После окончания ПХТ места первоначальной «bulky diseases» ( более 5 см в диаметре) облучались в СОД 30 Гр, и остаточная опухоль облучалась в СОД 40 Гр.
Ниже приводится дизайн выполняемых протоколов.
Таблица 1. Дизайн выполняемых протоколов
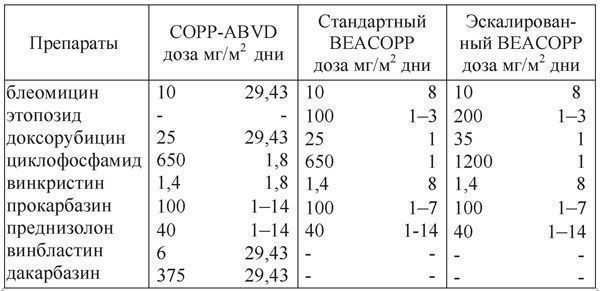
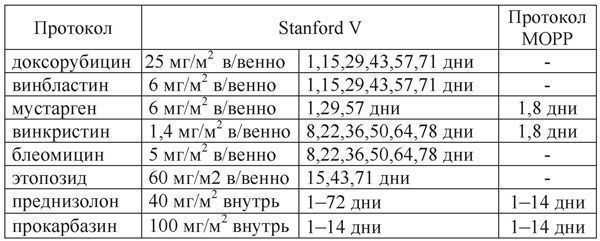
Протоколы МОРР и СОРР повторяются каждые 28 дней; протокол COPP-ABVD повторяется через 57 дней; протоколы BEACOPP (стандартный и эскалированный) повторяются через 22 дня от первого дня предыдущего цикла.
При нодулярной форме ЛХ с преобладанием лимфоцитов наблюдается увеличение периферических лимфоузлов, внутренние органы поражаются редко. Пациенты в IA стадии выявляются в 75% случаев. Клиническое течение медленное, но с частыми рецидивами. В I-IIA стадии заболевания проводится облучение пораженных зон в СОД 30 Гр. Пациенты в IIB-IV стадиях должны лечиться по более агрессивным схемам с включением ритук-симаба в дозе 375 мг/кв.м. в/венно в первый день цикла (протокол R-COPP).
Терапия ЛХ у больных подросткового возраста проводится по схемам ОЕРА и ОРРА.
Таблица 2. Схемы ОЕРА и ОРРА
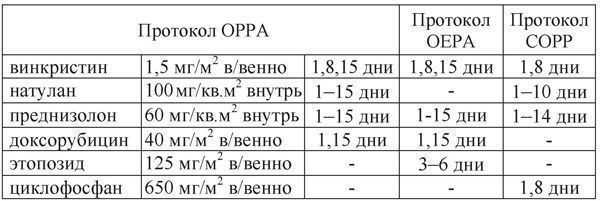
У пациентов в I-IIA стадиях (юноши) проводятся 2 курса ОЕРА, у девушек - 2 курса ОРРА.
Во IIB, IIIA, IE, IIE стадиях (юноши) проводятся 2 курса ОЕРА и 2 курса СОРР-терапии; у девушек - 2 курса ОРРА и 2 курса СОРР-терапии. В стадиях IIIB-IV, IIEB, IIIEA, IIIEB (юноши) проводятся 2 курса ОЕРА и 4 курса СОРР-терапии, у девушек в этих стадиях - 2 курса ОРРА и четыре курса СОРР-терапии.
Терапия рецидивов лимфомы Ходжкина
Клинический диагноз рецидива должен быть подтвержден данными биопсии. При рецидиве в течение первого года или прогрессировании заболевания показана высокодозная терапия с аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК).Высокодозная терапия включает четыре цикла сальваж-терапии (ICE, MIME, Dexa-BEAM с интервалами в 21 день), ESHAP, DHAP. Если рецидив наблюдается после ПХТ, длительная ремиссия может быть после дополнительной лучевой терапии плюс дальнейшая ПХТ; при рецидиве после лучевой терапии показана ПХТ плюс дополнительная лучевая терапия на область рецидива.
Результаты ауто-ТГСК при рецидиве более эффективны, чем при выполнении алло-ТГСК (хотя у молодых больных при наличии HLA-совместимого донора предпочтительнее выполнение алло-ТГСК).
Среди осложнений лечения ЛХ наиболее часто встречаются дисфункция щитовидой железы (гипопаратиреодизм в 6-25%), риск возникновения рака железы составляет 2,4-6,8%.
Бессимптомные перикардиты и миокардиты отмечаются у 50% больных, подвергшихся лучевой терапии (облучение средостения), острые перикардиты - в 2-13% случаев. У 20% больных развивается острый лучевой пульмонит и хронический рестриктивный фиброз. При сочетании программы ABVD с облучением средостения изменения в легочной ткани возникают у 49% больных.
Нарушения сперматогенеза при наличии интоксикационного синдрома выявляются у 60% мужчин, причем программа ABVD вызывает транзиторную азооспермию с восстановлением через 2 года. Транзиторная аменорея наступает у 60% женщин. Herpes zoster развивается после комбинированной химиолучевой терапии у 25% больных.
А.Т. Фиясь
Опубликовал Константин Моканов
Онко портал » Рецидив лимфомы – как заставить болезнь вновь отступить?
27.05.2015

Возвращения заболевания или рецидива опасается каждый человек, столкнувшийся с онкологическим диагнозом. Но как свидетельствует медицинская практика, рецидив не означает приговор. И второй бой с болезнью может быть достаточно успешным. Что может предложить современная медицина для пациентов с рецидивом диффузной В-крупноклеточной лимфомы? Об этом – научный сотрудник Национального института рака, Евгений Кущевой.
Если у пациента случился рецидив лимфомы, что он должен предпринять?
Лимфомы – это очень разнородная группа заболеваний, которые отличаются по своему течению, лечатся разными схемами терапии. И в случае рецидивов подход тоже различный. Давайте рассмотрим проблему на примере самой распространенной лимфомы – диффузной В-крупноклеточной. Но вначале определимся с терминологией. Рецидив – это возобновление заболевания после того, как его считали излеченным. Это означает, что заболевание вернулось через некоторое время после того, как у пациента после первоначального лечения была достигнута полная ремиссия.
Какие признаки и симптомы могут свидетельствовать о том, что болезнь вернулась?
У пациента могут увеличиться наружные лимфоузлы, повыситься температура тела, появиться какие-то другие симптомы (например, длительный кашель). Скажем так: если у человека что-то не так, это не банальная ОРВИ, лучше проконсультироваться у специалиста. Если при проведении обследования у пациента выявлено увеличение лимфоузлов или какие-то другие изменения, свидетельствующие о возврате болезни, говорят о рецидиве. Хочу особенно акцентировать на том, что очень важным при диагностировании рецидива является проведение повторной биопсии лимфоузла и иммуногистохимическое исследование материала. Это позволяет исключить неопухолевое поражение лимфатических узлов, отличить остаточную опухолевую массу без жизнеспособной опухоли от истинного опухолевого роста, уточнить тип лимфомы. Существенную роль при этом может сыграть позитронно-эмиссионная томография всего тела. Говоря о диагностике лимфом, хочу отметить, что у нас в Национальном институте рака работает международная программа «iPath». Это международный ресурс телемедицины и в сложных диагностических случаях сотрудники Института рака могут обсудить информацию о пациенте с ведущими специалистами из разных стран. Це міжнародний ресурс телемедицини і в складних діагностичних випадках співробітники Інституту раку можуть обговорити інформацію про пацієнта з провідними фахівцями з різних країн.
И если в результате диагностики было подтверждено, что это – все-таки рецидив, какой следующий шаг?
Пациент и врач должны принять решение о том, будет ли предпринята вторая попытка вылечить лимфому, проведя радикальную терапию, или начнется паллиативная терапия. Этот выбор должен быть сделан вместе с пациентом с учетом всех возможных рисков такой терапии и сопоставления их с ожидаемой пользой.
Радикальная терапия рецидивов так опасна?
Нет, ее токсичность сопоставима с терапией первой линии, т.е. тем лечением, с которого начинали. Опыт показал, что проведение терапии второй линии или сальвадж-терапии, возможно в условиях обычного стационара при соблюдении правил и принципов сопроводительной терапии. Но выбор должен быть сделан пациентом осознанно. После подтверждения того, что у пациента случился рецидив лимфомы, проводят обследования для оценки общего состояния здоровья и распространения лимфомы в организме при рецидиве. Затем начинается лечение (полихимиотерапия) по одной из схем терапии второй линии. Это схемы, которые содержат препараты других лекарственных групп в сравнении с первичной терапией. Дело в том, что если первичная терапия не дала стабильного эффекта, повторять те же препараты не имеет смысла. Как правило, проводится лечение по схемам, основанным на препаратах платины или гемцитабина (DHAP, ESHAP, ICE, IGEV). При достижении положительного ответа на терапию крайне желательно проведение высокодозовой химиотерапии как завершающего этапа. Его цель – подавление минимальной остаточной болезни. Это мировой стандарт лечения рецидивов многих лимфом, в том числе и диффузной В-крупноклеточной. Такая терапия позволяет добиться выздоровления у существенной части пациентов даже после рецидива лимфомы.
У некоторых пациентов первичная терапия не дает существенного эффекта. Что делать в этой ситуации?
Это так называемое первично-рефрактерное течение, под которым подразумевается нечувствительность к стартовой терапии. На фоне лечения такая лимфома недостаточно уменьшается или даже увеличивается. В этом случае очень важно немедленно прекратить терапию І линии как неэффективную. Дальнейшая тактика будет схожей с рецидивом: лечение радикально меняется и планируется высокодозовая терапия. Продолжать первичную терапию в этой ситуации бесполезно и даже вредно – токсичность она имеет, а пользы не принесет.
А есть ли какие-то меры профилактики рецидива?
Вероятность рецидива меньше у тех пациентов, у которых, прежде всего, была проведена правильная диагностика, а также лечение соответствовало современным стандартам. Примером может послужить схема R-CHOP. Долгое время стандартом терапии диффузной В-крупноклеточной лифомы являлась схема CHOP как наиболее эффективная и наименее токсичная. После того как было синтезировано моноклональное антитело ритуксимаб, исследования показали существенное преимущество комбинации CHOP с ритуксимабом над схемой CHOP. Это улучшило результаты лечения, в том числе способствовало снижению частоты рецидива. Таким образом, точная диагностика типа лимфомы и возможность проведения самого современного лечения позволяет снизить риск рецидива лимфомы. А если все-таки рецидив возник, с ним можно и нужно бороться.
Візитів: 3 762 всього, 1 в день
Все статьи раздела: "Публикации"
сколько живут при успешном лечении
Лимфома Ходжкина является одним из распространенных проявлений рака. Он диагностируется как у взрослых, так и у детей. Данная разновидность лимфомы считается одной из самых излечимых. Даже на последней стадии заболевания, выживаемость составляет почти 65%.
Определение
Лимфома Ходжкина представляет собой поражение лимфоситемы раковыми клетками, которое приводит к патологическому изменению состава крови. Чаще всего, патология диагностируется у мужчин.
В группу риска при этом входят люди возрастом от 14 до 40 лет. Заболевание характеризуется постепенным поражением региональных узлов системы, которое затем распространяется в кровь и на удаленные участки тела.
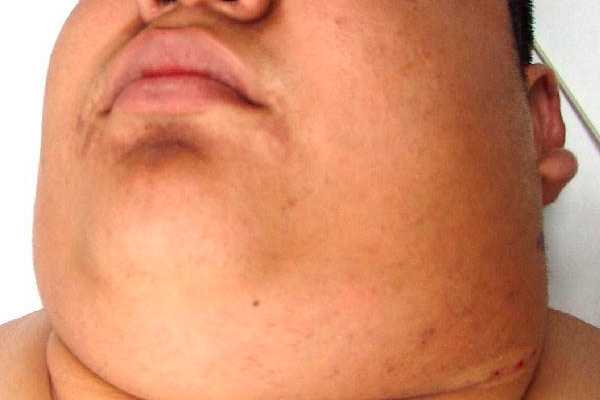
История
Данный вид лимфомы был выделен после многочисленных наблюдений ученым-медиком Томасом Ходжкином. Сначала он начал изучать патологию, как одно из общих заболеваний с отягощенной клинической картиной. Патологии было присвоено название – болезнь Ходжкина. Она диагностировалась по следующим симптомам:
- аномальная слабость;
- чрезмерное разрастание узлов;
- увеличение и видоизменение селезенки.
Но, глубоко изучив механизм развития заболевания и его причину, ученый пришел к выводу, что данная патология носит раковый характер, в результате чего она была переименована в лимфому Ходжкина.
Причины
Учеными было выделено несколько причин, которые, по их мнению, могут провоцировать развитие лимфомы:
- вирус Эпштейн-Барра;
- постоянное проживание в неблагополучных экологических условиях;
- облучение радиацией;
- наследственный фактор;
- работа на вредном производстве с использованием канцерогенных и химических веществ.
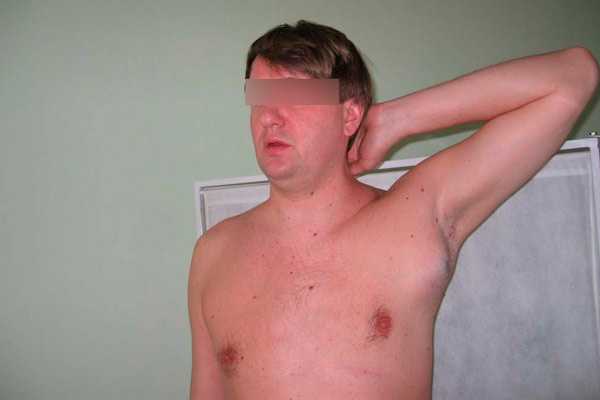
Стадии
Для лимфомы Ходжкина характерно 4 стадии развития:
1 стадия. Характеризуется поражением лимфоузлов одной группы. На первой стадии выделяют две фазы развития: IА и IЕ. На IА поражаются только лимфоузлы, а на IЕ в патологический процесс вовлекаются прилегающие ткани.
На данной стадии, как правило, требуется минимальный объем лечения, при котором количество выживших на протяжении 10 и более лет достигает почти 100%. Полные ремиссии наблюдаются у 96% пациентов. Безрецидивный период до 15 лет отмечается у 82%.
2 стадия. Раковые клетки распространяются на другую группу лимфосистемы, расположенную на той же стороне, что и первоначальный очаг. Для второй стадии определяется очень благоприятный прогноз лечения. Выживаемость за 5 лет составила 85%.
Полная ремиссия наблюдается у 76% заболевших. Рецидивы возникают лишь у 35% пациентов, причем только у одной трети из них наблюдается негативный прогноз.
3 стадия. Для данной стадии характерно два варианта развития: III1 и III2. При первом варианте поражается верхний отдел брюшной полости. При втором варианте наблюдается поражение нижнего отдела. Эффективность лечения при этой стадии находится в пределах 85%.
При этом выживаемость в течение 10 лет составляет 60% от общего числа заболевших. В зависимости от степени осложнений, рецидивы могут возникать в 10 или 40% случаев в первый год после лечения, и 25% в последующие годы.
- 4 стадия. Отличается распространением патологии на удаленные органы и ткани. Вероятность излечения при запущенной стадии достаточно высока и держится на уровне 75%, с полной ремиссией у 45% пациентов. Однако при этом рецидивы в первые годы после терапии, составляет почти 50%, из них только 10% проживает более 10 лет.
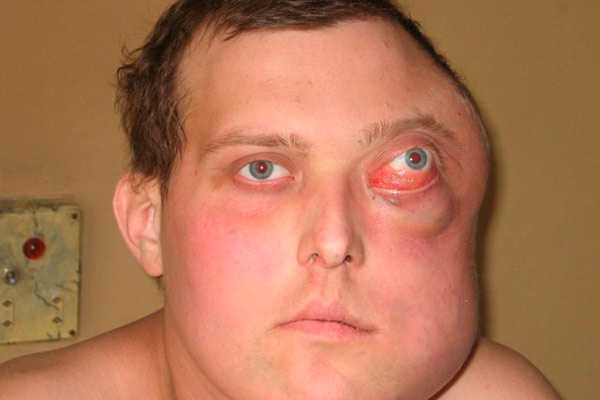
Виды
Для лимфомы Ходжкина характера вариативность, которая определяется типом тканевых изменений в узлах системы. По данному признаку выделяют несколько видов патологии:
- Классическая. Характеризуется появлением стандартных симптомов заболевания с увеличением лимфоузлов и медленным типом развития. За счет этого, данный вид патологии диагностируется на ранних этапах, что влияет на прогноз лечения. На начальных стадиях заболевания классического типа выживаемость составляет 96–98%.
- С нодулярным склерозом. Характеризуется образованием в лимфоидной ткани многочисленных фиброзных прослоек. На первых порах развития рака такого типа, патологию путают с вирусной инфекцией, что затрудняет раннее диагностирование. Но даже при этом, лечение имеет положительный прогноз в 96% случаев.
- С лимфопенией. Отличается небольшим разрастанием фиброзной ткани и ограниченным количеством раковых клеток. Данный вид заболевания характеризуется полным излечением даже на последних стадиях.
- Смешанноклеточная. Является редким видом патологии, при которой практически отсутствует распространения на органы и ткани. Она отличается пассивным типом развития, что дает гарантированный положительный результат даже при небольших объемах лечения.
- Классическая с преобладанием лимфоцитов. Является патологией с наименьшей степенью злокачественности. Обладает хорошим прогнозом, даже при поддерживающем лечении. Ремиссия в этом случае наблюдается в 99% случаев.
- Нодулярная с преобладанием лимфоцитов. Имеет низкий процент злокачественности, но лечение осложняется регулярным присоединением дополнительных инфекций.
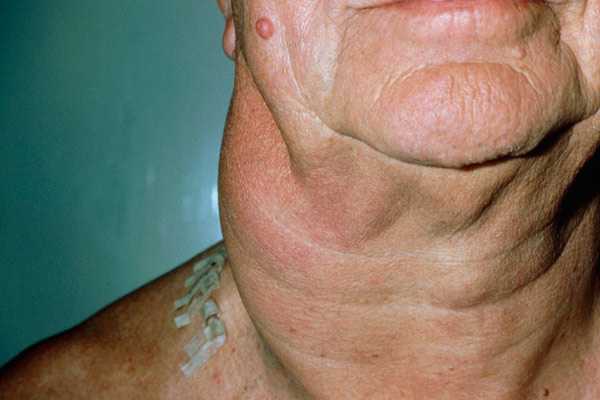
Признаки
Данное заболевание можно распознать по следующим признакам:
- увеличение и болезненность лимфоузлов, которые по мере развития патологии разрастаются и сливаются друг с другом;
- появление отдышки;
- затруднение дыхания;
- ноющие тупые боли спонтанного характера, возникающие за грудиной;
- увеличение температуры;
- интоксикация организма: тошнота, головная боль;
- быстрое уменьшение массы тела;
- частое присоединение инфекций в результате снижения иммунитета.
Прогноз
Несмотря на то, что общая цифра выживаемости составляет 98%, в каждом отдельном случае этот показатель может изменяться. На это в первую очередь, влияет возраст пациента.
Люди среднего возраста
Для людей среднего возраста характерен высокий показатель выживаемости при первой стадии заболевания, который находится около 96%. Из них, у 95% наблюдается полная ремиссия. Остальное число пациентов включает всего 18% рецидивов и 93% выживаемости в течение 15 лет.
После лечения 2 стадии, положительный эффект наблюдается у 88% пациентов, с ремиссией в течение 5 лет и более и 80% из них. Рецидивы при этом встречаются у 35% заболевших.
Для 3 и 4 стадии, также характерен высокий показатель выживаемости в течение 5 лет, который может достигать 75%. Но в данном случае возникает высокий риск первичных и вторичных рецидивов. И если после первичного рецидива остаются в живых около 60% пациентов, то при вторичном рецидиве, этот показатель снижается до 10%. Хотя и в этом случае срок жизни может быть около 10 лет.
Мужчины и женщины
Если рассматривать прогноз жизни среди мужчин и женщин, то стоит отметить, что при равном количестве заболевших выживает 53% женщин и всего 45% мужчин. При этом большая часть мужчин принадлежит к старшей возрастной группе.
По статистике, и мужчины и женщины имеют примерно одинаковый положительный прогноз лечения. Но у мужчин отмечается большее количество рецидивов, которые чаще всего провоцируются тяжелыми условиями труда или вредными привычками.
У женщин только в 12% случаев, первичные рецидивы ведут к летальному исходу. У мужчин эта цифра составляет 37%.
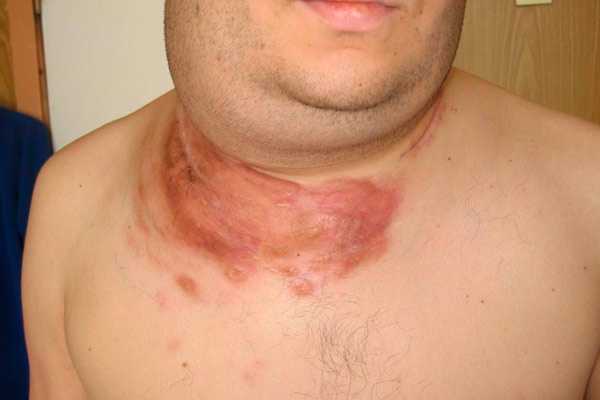
Старики
Пожилой возраст считается самым неблагоприятным для любой стадии лимфомы, так как ослабленный организм не всегда способен справиться с негативным влиянием методов, применяемых для лечения.
Но даже после всех неблагоприятных последствий, ремиссия наступает у 60% пожилых пациентов. Данный показатель сохраняется на протяжении 10 лет, но не более. У 40% заболевших наблюдаются рецидивы в течение этого периода, что приводит у 25% к летальному исходу в течение 3 лет.
При беременности
Разработка новейших методов лечения, позволила восстановить детородные функции и нормальное родоразрешение у пациенток, которые обнаружили лимфому уже в период беременности, либо находящиеся в стадии ремиссии.
Последние многочисленные исследования доказали, что при назначении грамотного современного лечения, риск негативного воздействия на плод сводится к нулю.
Если пациентка находится в стадии ремиссии, то на протяжении всей беременности, врач осуществляет регулярный контроль за состоянием матери и развитием плода, используя для этого разнообразные методы диагностики. При этом пациентке не обязательно находиться в стационаре.
Если же, лимфома была обнаружена в период беременности, и она имеет агрессивный характер, то проводится щадящая химиотерапия, которая не оказывает на плод ни какого влияния. В ситуации, когда требуется объемное лечение с применением мощных противораковых препаратов, ставится вопрос о прерывании беременности в соотношении со степенью потенциальной угрозы плоду.
Но к агрессивным методам лечения во время беременности прибегают реже всего, так как гормональная перестройка организма женщины сдерживает рост и распространение рака.
Клинические данные показывают, что и при наличии ремиссии, и после проведения лечения 1–3 стадии, из 100% детей, все родились здоровыми и не имели отклонений в своем психологическом и физическом развитии.
Дети
В случае лечения лимфомы у детей, отмечается наиболее благополучный прогноз лечения. В отличие от взрослых, на первичных стадиях, выживаемость детей составляет за 15 лет 99%.
Для третьей стадии, этот показатель уменьшается лишь до 95%. Только у 11% пациентов в течение этого времени наблюдается рецидив, который чаще всего приходится на возраст около 18 лет. При этом степень вероятности выживания будет зависеть от времени рецидива. Чем позднее он произошел, тем выше риск неблагополучного исхода лечения.
Что способствует исцелению?
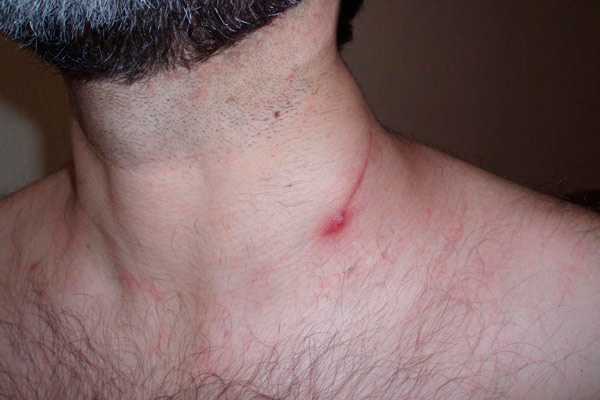
Шрам после удаления опухоли
На результат лечения влияет не только своевременность его проведения, но и эмоциональный настрой, который в первую очередь зависит от окружающих людей.
Для пациента нет необходимости в сопереживании или сочувствии. Ему нужна поддержка, которая повысит уверенность в благополучном лечении и простимулирует внутренние защитные силы.
Кроме того, необходимо уделять особое внимание питанию и правильному образу жизни. Благодаря правильному сочетанию данных факторов, у пациента нормализуются обменные процессы, и повышается иммунитет, что в значительной степени влияет на выздоровление именно при данном виде рака.
Несмотря на то, что при злокачественных поражениях ощущается постоянная слабость, необходимо постоянно поддерживать физическую форму. Благодаря этому повышается общий тонус организма и нормализуется кровоток, улучшающий трофику и питание тканей.
Истории успешного излечения
Положительный результат лечения лимфомы Ходжкина можно доказать многочисленными историями выздоровления:
Женщина, 18 лет. Обратилась к врачу для обследования из-за постоянной слабости, увеличения лимфатических узлов и резкой потери веса. После диагностики был поставлен диагноз – смешанноклеточная лимфома Ходжкина 4 стадии.
Назначено 10 курсов химиотерапии и облучения, с положительным результатом. Через несколько лет случился рецидив с разрастанием до 4 стадии, после чего пришлось пройти высокодозную химиотерапию и трансплантацию костного мозга. Несмотря на неблагоприятный прогноз, уже после 2 курсов, наблюдалась активная ремиссия.
После пересадки костного мозга, организм начал быстро восстанавливаться. На сегодняшний день пациентка находится в стадии стойкой ремиссии в течение 6 лет.
Мужчина 25 лет. Обратился к врачу с симптомами длительного кашля и отдышки. При детальном обследовании выявили рак Ходжкина классического типа 2 стадии. Было назначено 6 курсов высокодозной химиотерапии с перерывами в месяц.
Лечение проходило с минимальным проявлением побочных эффектов и с активной положительной динамикой. Уже после второй химиотерапии наблюдалось троекратное уменьшение патологических тканей. Спустя 5 лет после лечения отмечается стойкая ремиссия.
Рекомендуем к просмотру видео о лечении данного заболевания:
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Лимфома Ходжкина - причины, симптомы, диагностика, стадии, методы лечения и прогнозы | Полезно знать
добавлено: 02.01.2017
Лимфома Ходжкина — излечимое заболевание лимфатической системы
Лейкоциты – главная защита человека от окружающего мира. Но при поломке в механизме саморегуляции клеток развиваются разные проблемы. Самые опасные из них – злокачественные опухоли, к которым относится лимфома ходжкина (лимфогранулематоз). Возникает из лимфоцитов – разновидность защитных белых кровяных телец.
Лимфома — стадии, диагностика, лечение
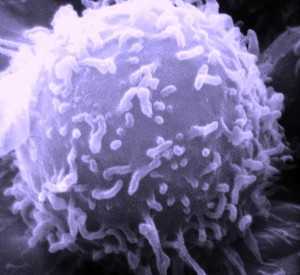
Лимфома – это группа онкологических заболеваний, которая характеризуется поражением клеток, играющих важную роль в работе иммунной системы, а также клеток, образующих лимфатическую систему организма. Лимфатическая система – это сеть ветвящихся сосудов, по которым циркулирует жидкость, называемая лимфой. Клетки лимфы – лимфоциты, выполняют важнейшую функцию в борьбе с инфекциями. Лимфатическая система имеет множество лимфоузлов. Их задача – фильтрация лимфы, которая может содержать бактерии или вирусы.
Рак возникает тогда, когда нормальные лимфоциты трансформируются в клетки, начинающие бесконтрольно расти и размножаться. Такие клетки могут собираться в одном или нескольких лимфоузлах или других тканях, образуя массы неправильно развивающихся клеток, или опухоль. В дальнейшем они вторгаются в соседние ткани и отдаленные органы, образуя метастазы. Например, если поражена центральная нервная система, то развивается лимфома мозга.
Классификация болезни производится по двум группам:
- болезнь Ходжкина, или HL;
- остальные виды опухолей, которые носят название “неходжкинская лимфома”.
Обе категории рака имеют схожие симптомы, но с помощью анализа крови и исследования образцов ткани под микроскопом специалисты Центра Лечения Рака Крови диагностируют определенный тип лимфомы. При своевременном принятии мер для лечения лимфомы прогноз достаточно оптимистичный.
Болезнь Ходжкина возникает из-за неправильного развития В-лимфоцитов, продуцирующих специальные белки, которые крепятся к инфицированным и чужеродным клеткам для того, чтобы иммунная система могла распознать и уничтожить их.
Неходжкинская лимфома возникает при аномальном функционировании Т-клеток, которые уничтожают зараженные клетки и принимают участие в регуляции иммунитета. Существует множество подтипов рака, которые по-разному реагируют на терапию. Одним из вариантов неходжскинской лимфомы является первичная лимфома мозга, которая составляет 2% от всех онкологических поражений ЦНС.
Болезнь Ходжкина является распространенной формой опухоли среди молодежи в возрасте от 16 до 35 лет и у пожилых людей от 55 лет. Неходжкинские типы недуга развиваются в основном у пожилых людей. Изучение причин, которые приводят к подобным нарушениям генетической составляющей клеток лимфы, является одним из основных направлений исследований медицинских онкологических центров.
Ученые не знают точных причин возникновения лимфомы мозга и других типов заболевания. Большинство людей, которым поставили такой диагноз, старше 60 лет. В группу риска попадают люди, инфицированные ВИЧ/СПИД, вирусом Эпштейна-Барра и гепатита C. Иммунная система таких пациентов крайне ослаблена, а поэтому и более восприимчива к лимфоме. Воздействие высоких уровней радиационного излучения повышает риск развития неходжкинской лимфомы.
Симптомы лимфомы
Ранние симптомы лимфомы могут проявляться незначительно и имитировать менее опасные распространенные заболевания. Один из первых симптомов лимфомы – безболезненный отек шеи, подмышечных впадин или паха из-за увеличения соответствующих лимфоузлов. Растущие лимфатические узлы сдавливают близко расположенные нервные волокна или вены. Как следствие, возникает онемение, покалывание и/или боль в пораженном месте или отек конечностей.
Если увеличение узлов происходит в области желудка, то пациент ощущает раннее чувство сытости при употреблении пищи. Другие симптомы проявляются в виде лихорадки, необъяснимой потери веса, озноба, ночной потливости, болей в груди или пояснице, упадка сил, а также появления кожной сыпи и зуда.
Диагностика лимфомы
Чтобы выбрать оптимальный вариант лечения, специалисты Центра Лечения Рака Крови исследуют лимфатические узлы. Для определения типа опухоли проводится процедура биопсии, предполагающая взятие небольшого образца увеличенного лимфатического узла и изучение его под микроскопом. Биопсию проводят опытные специалисты с применением специализированной техники.
Тип лимфомы можно определить по внешнему виду раковых клеток под микроскопом и с помощью маркеров, которые распознают особые молекулы на лимфоидных клетках. Такие дополнительные анализы, как анализ крови, рентген грудной клетки или исследование клеток костного мозга помогают врачам увидеть, насколько далеко распространилась болезнь и какие органы поражены.
Стадии лимфомы
Чтобы определить, на какой стадии находится заболевание, используется комплексная диагностика. Это необходимо для выбора правильного лечения. Большинство лимфом имеют 4 стадии, каждой из которых соответствует определенный размер опухоли и дальность распространения рака.
I стадия лимфомы. Область развития опухоли ограничена одной группой лимфатических узлов и, в более редких случаях, одним близкорасположенным органом, не относящимся к лимфатической системе организма.
II стадия болезни. Рак обнаружен в двух и более группах лимфатических узлов, по одну сторону диафрагмы, также может быть поражен орган другой системы организма, расположенный рядом с пораженными узлами лимфатической системы.
III стадия. Поражение присутствует в группе лимфатических узлов по обе стороны диафрагмы, иногда с привлечением других соседних органов. На этой стадии нередко поражена селезенка.
IV стадия лимфомы. Рак распространился на кости, ткани костного мозга, легкие и другие органы, расположенные далеко от первоначального очага развития лимфомы – пораженных лимфатических узлов.
Лечение лимфомы
Если у пациента подтвержден диагноз лимфома, прогноз развития болезни может носить различный характер, и зависит от многих факторов, включая стадию болезни, возраст человека и многое другое. После изучения результатов лабораторных исследований и уточнения стадии разрабатывается индивидуальная программа лечения. Существует четыре вида лечения, которые используются самостоятельно или в сочетании друг с другом:
- химиотерапия;
- биологическая терапия;
- лучевая терапия;
- трансплантация стволовых клеток.
Болезнь Ходжкина обычно лечится с помощью лучевой терапии и химиотерапии. Лечение неходжкинской лимфомы зависит от конкретного вида рака. Химиотерапия – основной метод лечения, а лучевая и биологическая терапия добавляются при необходимости как дополнительный способ лечения.
Лечение лимфомы на разных стадиях может иметь затяжные побочные эффекты, такие, как боль в костях и суставах, онемение рук и ног, снижение способности концентрировать внимание, потливость. Такие явления могут длиться более года после достижения ремиссии. Женщины могут ощущать симптомы менопаузы. Организму требуется время для того, чтобы восстановиться после интенсивной терапии. Лечащий врач поможет пациенту преодолеть реабилитационный период.
Лимфомы Ходжкина — почему она появляется
Как и при большинстве онкологических болезней, связать появление лимфомы Ходжкина с чем-то одним невозможно. Есть предрасполагающие факторы, увеличивающие риск патологии:
- Когда-то человек перенес болезнь, вызванную вирусом Эпштейн-Барра (например, инфекционный мононуклеоз). Частички генетической информации вируса остались в лимфоцитах, это привело к мутациям в них
- Подавление клеточной части иммунитета – при ВИЧ-инфекции, после пересадки органов и приема специальных препаратов против отторжения
- Генетическая предрасположенность. Лимфомой Ходжкина практически не болеют представители монголоидной и негроидной рас. Крайне редко болезнь встречается у разных членов одной семьи. Правда, в случае однояйцевых близнецов обнаружение этой патологии у одного автоматически повышает шансы второго заболеть почти до 100%
Симптомы лимфомы Ходжкина
Главные признаки развития лимфогранулематоза разделяются на 2 большие группы:
Общие симптомы, говорящие об активности опухолевых клеток
- Стойкое повышение температуры выше 38 градусов. Лечение антибиотиками, противовоспалительными препаратами не помогает совсем или снимает проявления ненадолго
- Проливные поты, особенно вечером и ночью, связаны с лихорадкой
- Снижение веса за последние полгода, особенно если нет других причин для похудания
- Слабость, невозможность выполнять работу, с которой раньше легко справлялись
- Зуд кожи – от незначительного на определенных участках кожи (над пораженными лимфоузлами) до резко выраженного, мучительного, лишающего покоя и сна
Специфические симптомы – разрастание в органах опухолевой ткани, состоящей из нормальных и патологических лимфоцитов
- Увеличение лимфоузлов. Самые частые места скопления опухоли – шейные и надключичные лимфоузлы, больше слева. Нередко увеличиваются и другие группы на периферии (подмышечные, паховые) или внутри полостей тела (внутригрудные, в брюшной полости, вдоль аорты). Разрастание лимфоузлов на поверхности причиняет больному эстетические проблемы, мешают при движениях. Значительное прибавление опухолевой ткани внутри тела сдавливает внутренние органы. Внутри грудной клетки компрессия бронхов приводит к кашлю, одышке, полых вен – к отеку и синюшности лица. Лимфоузлы внутри брюшной полости иногда становятся причиной проблем с кишечником
- Увеличение селезенки, а на поздних стадиях – печени. Печеночные проблемы проявляются болью, усилившимся зудом и желтушностью кожи
- Появление симптомов поражения других органов – кашель, одышка при легочных очагах, резкая боль при повреждении плевры, накоплении опухолевой ткани в позвонках
Дополнительные признаки — проникновение раковых клеток в костный мозг и нарушение формирования нормальных кровяных клеток — это анемия, значительно сниженная сопротивляемость инфекциям.
Симптомы рака груди
Разновидности лимфомы Ходжкина
Существует много видов злокачественного перерождения лимфоцитов, лимфома Ходжкина выявляется в 10-20% всех зарегистрированных заболеваний. Все лимфоциты образуются в одном месте, но после выхода из костного мозга проходят «обучение» в разных местах и обзаводятся буквой-приставкой – Т или В. С этого момента они сильно отличаются друг от друга.
Главный критерий отнесения лимфомы к ходжкинской – обнаружение специфических клеток – Рид-Березовского-Штернберга и двух видов клеток Ходжкина (больших и маленьких). Они отличаются особым строением и имеют принципиальную особенность – смешанные антигенные и иммунологические факторы, их невозможно отнести ни к Т, ни к В. Существует редкая форма лимфомы Ходжкина, где источник развития – мутировавшая В-клетка.
Классические варианты лимфомы Ходжкина
По мнению некоторых исследователей – это стадии прогрессирования болезни
- Лимфоидное обогащение. Патологические клетки обнаруживаются в небольшом количестве – около 1% объема опухоли. Благодаря большому количеству биологически активных веществ, мутанты окружают себя нормальными лимфоцитами, эозинофилами, плазматическими клетками. Эозинофилы отвечают за интересный эффект при лимфоме – болезненность в лимфоузлах под действием алкоголя. Этиловый спирт приводит к разрушению этих клеток, выделившиеся вещества воздействуют на окружающие ткани. Форма благоприятная, хорошо лечится, но выявляется редко
- Лимфома Ходжкина нодулярный склероз. У 70% пациентов патология выявлена именно на этой стадии. В лимфоузле (нодулюс) разрастается соединительная ткань (склероз). Утолщается капсула, внутри появляются заметные перегородки, между которыми обнаруживаются нормальные и патологические клетки. Хорошо отвечает на лечение, считается благоприятной
- Смешанно-клеточная форма лимфогранулематоза. Зрелых лимфоцитов становится меньше, характерные элементы лимфомы ходжкина легко обнаруживаются в препарате под микроскопом. Встречается у людей с недостаточным иммунитетом – ВИЧ-инфицированных, детей, людей в возрасте. Требует более интенсивного лечения из-за большого распространения опухолевых клеток в организме
- Лимфоидное истощение. Заключительная, самая злокачественная форма. Полноценных защитных клеток практически нет, в материале из лимфоузлов обнаруживаются только склеротические изменения и клетки Березовского-Штернберга
Особый вариант лимфогранулематоза
Нодулярная форма с лимфоидным преобладанием. Отличается от похожего по названию классического подвида четкими характеристиками В-звена лимфоцитов.
Стадии течения лимфомы Ходжкина
Запущенность и распространенность лимфогранулематоза оценивается по количеству пораженных лимфоузлов, вовлеченности соседних к ним и отдаленных органов.
I стадия
Ограниченное разрастание опухолевых клеток в одной группе лимфоузлов.
II стадия
Злокачественные клетки обнаруживаются в разных местах: несколько групп лимфоузлов недалеко друг от друга (не разделены диафрагмой) или лимфоузлы плюс соседний орган (IIE).
III стадия
Процесс распространен по обе стороны от диафрагмы. Преимущественная локализация в верхней части живота – III-1, скопление пораженных лимфоузлов в нижней части брюшной полости – III-2.
IV стадия
Запущенный лимфогранулематоз с вовлечением разных органов. Проявляется симптомами повреждения печени, позвоночника, легких.
Дополнительно к номеру стадии добавляются или нет определенные группы:
- A – нет общих симптомов (лихорадка, потливость, похудание)
- B – есть общие симптомы болезни
- E – злокачественные клетки образуют опухолевые скопления во внутренних органах
- S – поражена селезенка. Для этого органа выделена специальная буква, потому что наличие опухоли в ней означает переход болезни на новый уровень – патологические клетки попадают в кровь и к лимфатическому пути распространению добавляется гематогенный
- X – большой размер образования
Любая из этих букв (кроме А) отягощает болезнь, требует более агрессивного и длительного лечения.
Лимфогранулематоз – осложнения болезни
Симптомы развившихся осложнений появляются из-за нескольких причин:
- Опухолевые ткани распространяются в разные органы – кости, нервную систему, плевру. Разрастание клеток в железах внутренней секреции (щитовидную, поджелудочную, яичники) приводит к нарушению их работы с характерными проявлениями. На поздних стадиях возможно поражение спинного мозга и проблемы с чувствительностью и движением вплоть до параличей
- Опосредованная связь с некоторыми характерными признаками лимфомы ходжкина. Больные с лимфогранулематозом страдают от длительного кожного зуда. Это приводит к частым расчесам и инфицированию кожи, дискомфорт вызывает хроническую бессонницу, психоэмоциональное возбуждение. Со временем развиваются невроз и депрессия
- Неполноценность лимфоцитарного звена лейкоцитов аукается частыми вирусными, бактериальными и грибковыми инфекциями
- Осложнение после лечения лимфомы – постлучевые повреждения внутренних органов и кожи, бесплодие, инфекционные болезни. В отдаленном периоде – развитие вторичных опухолей, в том числе и лейкоза
Симптомы рака горла — формы, стадии, причины
Ключевые моменты диагностики лимфомы Ходжкина
Для правильного и своевременного выявления лимфогранулематоза необходимо оценить выраженность и частоту проявления характерных симптомов. Необходимо выяснить все симптомы, дающие право добавить букву В к стадии болезни.
После этого обязательно осматривают пациента, прощупывают все доступные для пальпации лимфоузлы, определяют размеры печени и селезенки. Обращают внимание на кожу – цвет, сухость, наличие следов расчесов.
Лабораторные исследования
Общий анализ крови – при повреждении костного мозга – анемия. Обнаруживают изменение числа лейкоцитов с уменьшением лимфоцитов, чем запущенней болезнь – тем меньше лимфоцитов в периферической крови. Особое внимание обращают на СОЭ – скорость оседания эритроцитов. Ускорение выше 30, а тем более, выше 50 – свидетельство выраженной активности опухоли.
Биохимия крови. Главный показатель – уровень лактатдегидрогеназы (ЛДГ), количество белков в плазме, проба Кумбса. При распространении опухоли на печень – печеночные пробы
Инструментальные методы
Необходимы для визуализации увеличенных лимфоузлов, размеров опухолей в легких, костях, печени и других органов.
- УЗИ лимфоузлов, грудной, брюшной полости
- Рентгенография грудной клетки – как минимум, в двух проекциях – прямой и боковой
- Компьютерная томография, магнитно-резонансная томография
- По возможности – ПЭТ/КТ. Обнаруживает участки распространения активно размножающихся опухолевых клеток. Это необходимо как для выявления новых метастазов в лимфоузлах и других органах и тканях, так и для контроля эффективности лечения. Сколько раз и как часто проводится ПЭТ определяет лечащий врач
- Лимфома Ходжкина образует злокачественные очаги в костях, для их обнаружения проводится сцинтиграфия с галлием.
Специальные методы, без которых невозможно говорить о лимфогранулематозе
- Биопсия и гистология. Для точного диагноза недостаточно исследовать пунктат (вытяжка шприцом), обязательно нужен кусочек ткани или удаленный лимфоузел. Материал заливается парафином, очень тонко нарезается, помещается на стекло и особым образом окрашивается. Потом врач смотрит препарат под микроскопом. Обнаружение клеток Березовского-Штернберга и других характерных изменений позволяет поставить диагноз и отличить лимфогранулематоз от других лимфом.
- Трепанобиопсия и исследование костного мозга.
- Определение антигенной структуры клеток опухоли.
Лечение лимфомы Ходжкина
Как и при других злокачественных заболеваниях, при лимфогранулематозе используют химиотерапию и облучение. Эти методы убивают быстроразмножающиеся клетки опухоли, в меньшей степени затрагивая здоровые. В зависимости от стадии и выраженности проявлений способы лечения назначают изолированно или в комбинации.
- Химиотерапия. Существуют разные протоколы проведения с одновременным введением 4-8 высокотоксичных препаратов. На разных стадиях болезни, в зависимости от преобладающих симптомов меняется количество наименований лекарств, их доза. Решается, сколько раз будут проводиться курсы лечения (2-4-6) и определяется промежуток между ними
- Лучевая терапия. Назначается при увеличении периферических лимфоузлов. При лимфоме Ходжкина изолированное воздействие рентгеновских лучей применяется при менее запущенных формах с ограниченным поражением. Окружающие ткани защищаются свинцовыми экранами
- Комбинация лучевой и химиотерапии – наиболее распространенный сейчас метод лечения. Двойное воздействие на опухоли вызывает более длительную ремиссию, меньший риск осложнений терапии
- При самых запущенных формах лимфом и ранних рецидивах рекомендовано интенсивное воздействие. У пациента заранее берут костный мозг, при необходимости очищают его от опухолевых элементов, выделяют стволовые клетки. Далее очень высокой дозой химиопрепаратов и мощным облучением полностью убивают оставшиеся лимфоидные ткани по всему организму. Больной в этот момент полностью беззащитен перед инфекцией, поэтому находится в стерильном боксе. В дальнейшем идет пересадка костного мозга – собственного, забранного перед терапией. При невозможности подсадить собственные клетки, используют донорский – родственный или не родственный.
Симптомы рака легких — причины, виды, стадии
Прогноз выживания при лимфоме Ходжкина (лимфогранулематозе)
Лимфома Ходжкина – достаточно благоприятный сейчас диагноз. 90% больных достигают полной и длительной ремиссии, срок жизни не отличается от людей, никогда не страдавших лимфомами. Некоторые пациенты даже сохраняют фертильность, но для этого в большинстве случаев необходимо собрать и заморозить яйцеклетки или сперму.
Для оценки эффективности лечения используются следующие критерии:
- Уменьшение размера лимфоузла или опухоли после окончания химиотерапии наполовину
- Оставшиеся клетки не активны, мертвы (проверяется с помощью ПЭТ)
- Отсутствие рецидивов
Неблагоприятные результаты терапии:
- Отсутствие или слабый ответ на лечение – опухоль уменьшается незначительно, в некоторых случаях даже продолжает расти или сохраняет прежние размеры
- Появление признаков распространения процесса – вовлечение новых лимфоузлов очагов активности в других тканях и органах
- Ранние рецидивы (до 12 месяца после конца лечения)
Но даже в запущенных случаях с неблагоприятным ответом на стандартную терапию при лимфоме Ходжкина есть шансы добиться ремиссии более интенсивными методами, поэтому главное – настроиться на выздоровление и верить врачу. Несмотря на плохое самочувствие лечение должно продолжаться.
Профилактика лимфомы Ходжкина
Поскольку точной причины развития болезни до сих пор не знает ни один человек в мире, способов профилактики лимфомы просто не существует. Но в силах пациента сделать все для возможно более раннего выявления патологии:
- Регулярные профосмотры
- При длительной лихорадке, похудании попросите врача провести специальные обследования на онкологию, в том числе и на лимфому Ходжкина
Рейтинг статьи:
Лимфома Ходжкина — излечимое заболевание лимфатической системы
Причины возникновения
К основным причинам возникновения такого заболевания как рак лимфатических узлов относят:
- Воздействие на организм человека вредных веществ, например, работа на вредном производстве или частое взаимодействие с канцерогенами, пестицидами и гербицидами
- Частое нахождение под прямыми лучами солнца
- Заражение такими инфекциями как ВПЧ (Вирус папилломы человека), СПИД, ВИЧ и вирус Эпштейна-Барра
- Вредные привычки, например, курение. Чем больше стаж, тем больше вероятность развития опухоли лимфатических узлов
Также существуют некоторые факторы риска, которые способствуют поражению лимфоузлов:
- Поздние первые роды
- Возраст либо слишком молодой (до 25 лет), либо преклонный
- Наследственная склонность к раку
Симптомы лимфомы
Признаки рака лимфоузлов разделяют на местные (локальные) и общие.
К локальным признакам относят:
- Видимый рост лимфатических узлов в размерах
- Дискомфорт во время надавливания на область поражения
- Зуд кожного покрова и образование язв
- Субфебрильная температура тела (до тридцати восьми градусов) и повышенное потоотделение
Симптоматика проявления общих признаков выглядит следующим образом:
- Отсутствие аппетита и резкая потеря веса
- Слабость
- Затрудненность дыхания
- Анемия
- Нарушение работы пищеварительной системы
Диагностика рака лимфоузлов
Диагностировать поражение лимфоузлов, помимо стандартной пальпации, возможно следующими методами современной медицины:
- Ультразвуковое исследование, с помощью которого возможно установить место и структуру опухоли
- Магнитно-резонансная томография, которая проводится перед операцией, чтобы установить точное местоположение образования и распространение на близлежащие ткани
- Биохимический анализ крови
- Биопсия, которая подразумевает под собой исследование ткани на наличие онкологии и позволяет установить стадию заболевания
Стадии заболевания
Рак лимфоузлов разделяется на несколько стадий, среди которых выделяются:
Первая стадия:При обнаружении первой стадии рака выделяют поражение узлов одного участка лимфатической системы, выявить которое возможно благодаря полному обследованию. На данной стадии высока вероятность успешного излечения.
Вторая стадия:Вторая стадия отличается распространением поражения на два и более участка, а также возможен захват другого органа вне системы.
Третья стадия:На третьей стадии болезнь распространяется почти на все участки нахождения лимфоузлов, с захватом других органов. Наблюдается полное поражение диафрагмы и селезенки. Быстрый переход на 4 стадию онкологии.
Четвертая стадия:На последней стадии шанс на выздоровление очень мал, увеличивается вероятность летального исхода. Лечение уже не приносит облегчения, а опухоль поражает все больше органов: головной мозг, легкие, печень, поджелудочную железу.
Как лечить рак лимфоузлов
Назначение лечения рака лимфоузлов зависит от многих факторов, например: локализация опухоли, степень ее распространения на окружающие ткани, стадия, размер.
В основном используют следующие методы лечения:
- Лимфоузлы при раке наиболее эффективно поддаются лечению с помощью хирургического вмешательства. Суть в том, что зараженные ткани удаляются вместе с узлами. Для профилактики подлежат иссечению также и близлежащие узлы.
- После удаления, или как самостоятельное лечение рака лимфоузлов, назначают лучевую терапию. Продолжительность курса может составлять три-четыре недели.
- Универсальным средством для того, чтобы лечить рак является интенсивная терапия химическими препаратами, направленная на уменьшение размеров и рост образования, а также остановку распространения новообразований.
- Новейшие разработки в области медицины – пересадка костного мозга от донора или самого пациента. Подразумевает под собой переливание стволовых клеток с целью восстановить нормальное кроветворение.Здесь можно выделить фотодинамическую терапию. Пациенту вводят специальный препарат, который реагирует на опухоль под влиянием света, убивая зараженные клетки, при этом не затрагивая здоровые.В любом случае, схема лечения зависит от состояния пациента и может включать в себя как один способ из вышеперечисленных, так и несколько в совокупности.
Прогнозы
Рак лимфатических узлов разделяется на первичный и вторичный. Лимфома относится к первичному типу. Почти всегда ей заболевают люди, которые подвергаются основным причинам возникновения (нахождение на солнце, контакт с вредными веществами, вредные привычки, инфекции). Первостепенно лимфоузлы увеличиваются в той области, где изначально был очаг заболевания.
Прогноз поражения разных областей тела выглядит так:
- Паховая зона – 35%
- Шея – 31%
- Подмышки – 28%
- Прочие области – 6%
Для составления прогноза больного существует универсальный индекс.
Главными факторами для прогноза выживаемости являются:
- Стадия. 1 и 2 стадии отличаются 80% выживаемостью, по сравнению с 3 и 4 стадией
- Возраст. Самые лучшие показатели выживаемости у людей в возрасте от 15 до 39 лет
- Операционное вмешательство. При своевременном удалении зараженных тканей срок жизни может увеличиться в 5 раз
- Состояние человека. При отсутствии серьезных патологий шансы к выздоровлению больше, чем у больных людей
- Уровень ЛДГНаличие метастаз и их локализации. Менее всего опасны метастазы в районе рта, более – во внутренних органах
- Вид рака лимфоузлов
Соответственно, чем идеальнее показатели, тем благоприятнее прогноз для больного.
Профилактика заболевания
Специфической профилактики рака лимфатических узлов не существует. Но, учитывая вероятные причины его возникновения, такие как радиация и вредные вещества, можно уменьшить риск онкологии.
К общим рекомендациям относится:
- Употребление продуктов, которые богаты антиоксидантами (грецкие орехи, бобы, капуста, зелень)
- Хорошее питание с содержанием витаминов
- Избегание нахождения под прямыми лучами солнца
Рак лимфатических узлов, бесспорно, неприятное заболевание. Однако, большинство отзывов подтверждают благоприятную статистику. Также, больные отмечают непродолжительность реабилитационного периода. Медицина не стоит на месте, есть надежда, что вскоре лечение онкологических заболеваний будет более простым и эффективным.
Злокачественная опухоль, также известное как лимфома Ходжкина, относится к раковым заболеваниям лимфатической системы. На начальном этапе диагностируется, что это излечимое заболевание, но оно должно справедливо вызывать страх, потому что его первые симптомы похожи на простуду.
Содержание
- Что такое болезнь Ходжкина?
- Лимфома Ходжкина — причины
- Симптомы злокачественной диссекции
- Лечение и прогноз злокачественного гранулематоза Ходжкина
Что такое болезнь Ходжкина?
Это раковая болезнь лимфатической системы. Процесс болезни включает лимфатические узлы. Заболевание начинается с конфискации одного, а затем и следующих лимфатических узлов, чаще всего расположенных в области шеи и груди. В большинстве случаев клон раковых клеток получают из так называемых В-клеток, то есть белых кровяных клеток, ответственных за выработку антител. На поздней стадии болезни Ходжкина могут вовлечь другие лимфатические органы, такие как селезенка или печень, и в конечном итоге может быть задействован любой другой негерпетический орган.
Часто болезнь Ходжкина ошибочно считается типом лейкемии, тогда как в отличие от этих заболеваний, костный мозг может быть вторично взят в ходе лимфомы, но лимфатические узлы являются первичной отправной точкой. В зависимости от гистологической гистологии гранулема классифицируется как один из пяти основных подтипов, но из-за степени распространения в организме и клинического развития она попадает в одну из четырех категорий классификации Ann Arbor. На основании этих параметров можно определить прогноз пациента и план лечения.
Лимфома Ходжкина — причины
Причина болезни Ходжкина четко не определена, но существует ряд факторов, которые составляют ее потенциал. К ним относятся, прежде всего, вирусные инфекции, упомяните здесь вирус Эпштейна-Барра, цитомегаловирус и HTLV (Т-клеточный лейкоз человека). Генетический материал первого из этих вирусов диагностируется в клетках с опухолевыми характеристиками примерно в 70% случаев.
Кроме того, потенциальные этиологические факторы включают воздействие ионизирующего излучения, иммуносупрессивную терапию, а также специфическую генетическую предрасположенность. Риск развития братьев и сестер в 10 раз выше, а в случае близнецов он в 100 раз выше, чем в общей популяции.
Симптомы злокачественной диссекции
К сожалению, во многих случаях первые симптомы злокачественного зерна относятся к группе неспецифических заболеваний, которые могут свидетельствовать о многих распространенных, доброкачественных заболеваниях и, следовательно, часто недооцениваются. Я говорю здесь о таких симптомах, как:
- потеря веса,
- лихорадка,
- повышенное потоотделение,
- чувство слабости,
- нетерпимость к физическим нагрузкам.
Более типичные заболевания:
- кожные симптомы — зуд кожи,
- непереносимость алкоголя у человека, который ранее не жаловался на подобные проблемы,
- респираторные симптомы — одышка и продолжительный кашель, несмотря на отсутствие сопутствующей инфекции,
- возможны также абдоминальные симптомы — боль, увеличение обхвата живота и постоянный дискомфорт.
В ходе исследования врач может обнаружить увеличенные безболезненные лимфатические узлы, встречающиеся почти у 95% пациентов. Могут появиться спленомегалия и увеличение печени, а также симптомы, возникающие в результате поражения органов вне лимфатической системы:
- боль в костях,
- почечная недостаточность,
- аномалии в репродуктивных органах,
- нарушения функции мочевого пузыря,
- изменения кожи,
- изменения в центральной нервной системе.
Лабораторные тесты характеризуются результатами биопсии костного мозга или подозреваемых лимфатических узлов, а базовая морфология часто показывает анемию, тромбоцитопению и нарушенный процент лейкоцитов. Кроме того, в исследованиях по визуализации происходят изменения — опухоль, видимая при рентгенографии или КТ, и реже при УЗИ брюшной полости.
Лечение и прогноз злокачественного гранулематоза Ходжкина
Среди методов лечения гранулематоза Ходжкина — лучевая терапия, химиотерапия и наиболее часто используемые — комбинированная терапия, т.е. основанная на обоих методах. Выбор лечения лимфомы Ходжкина зависит от тяжести заболевания и общего состояния пациента. Стандартной процедурой является радикальная терапия, то есть высокая эффективность, направленная на полное разрушение опухолевой ткани, несмотря на возможные побочные эффекты у пациента.
В зависимости от прогноза 5-летняя выживаемость колеблется от 40 до 80%. К неблагоприятным предикторам относятся: опухоль размером более 10 см, вовлечение экстралимфатических органов, вовлечение трех или более групп лимфатических узлов, а также отклонения в лабораторных исследованиях. Кроме того, мужской и пожилой возраст также являются неблагоприятными прогностическими факторами.
3 истории о поисках верного диагноза

15 сентября — Всемирный день осведомленности о лимфомах, задача которого — привлечь внимание к этим заболеваниям и распространить информацию. Разбираемся, что такое лимфома, кто более подвержен развитию этого вида рака, а также рассказываем истории людей, которые победили лимфому.
Группа заболеваний
Лимфома — онкологическое заболевание, поражающее лимфатическую систему. Болезнь считается редкой: в 2018 году в мире зарегистрировано около 590 тысяч новых случаев заболевания, что составляет всего 3,5% от общего количества новых случаев рака.
Лимфомы представляют собой целую группу заболеваний, среди которых выделяют две главные формы: лимфому Ходжкина и неходжкинские лимфомы (НХЛ). Лимфома Ходжкина изучена лучше других и хорошо поддается лечению — около 90% заболевших полностью выздоравливают. Но НХЛ встречаются чаще — на них приходится около 90% случаев.
Опухоль возникает из-за генетической мутации лимфоцитов: они начинают бесконтрольно делиться, дрейфуют к лимфоузлам и другим частям организма, где продолжают размножаться.
Среди многообразия видов лимфом существуют агрессивные, например, одна из наиболее часто встречающихся — диффузная В-крупноклеточная лимфома, и вялотекущие или индолентные разновидности, например, фолликулярная лимфома. В первой группе симптоматика развивается очень быстро — от дней до недель, потому что опухолевые клетки очень быстро делятся. Неагрессивные лимфомы начинаются исподволь и первое время протекают незаметно.
Причины и факторы риска
Причины появления лимфом пока остаются неизвестными, а значит, нет возможности предотвратить болезнь. Однако известны факторы, повышающие риск развития лимфом:- Возраст. С возрастом вероятность заболеть раком увеличивается. Однако есть типы лимфом, которые развиваются, в основном, у молодых людей.
- Пол. Лимфомой болеют чаще мужчины, но некоторые виды НХЛ больше распространены у женщин.
- НХЛ у близких родственников (родителя, ребенка, брата).
- Некоторые химические вещества и лекарства, физические факторы. К ним относятся, например, отдельные пестициды, препараты химиотерапии и лучевая терапия.
- Ослабленная иммунная система. Так бывает при ВИЧ-инфекции, после трансплантации органов, при носительстве некоторых генетических мутаций, ответственных за первичный иммунодефицит (например, синдром Вискотта-Олдрича).
- Аутоиммунные заболевания (ревматоидный артрит, системная красная волчанка).
- Некоторые инфекции, например, ВИЧ, вирус Эпштейна-Барр, вирус герпеса человека 8 типа, Helicobacter pylori.
- Некоторые виды грудных имплантов.
Симптомы
Лимфому можно обнаружить на ранней стадии. Для этого важно обращать внимание на симптомы, они характерны для обеих групп лимфом:- Увеличение одного и более лимфоузла. Чаще всего на шее, в подмышечной впадине, в паху. В большинстве случаев воспаленные лимфоузлы остаются безболезненными.
- Лихорадка.
- Постоянная усталость.
- Потливость по ночам.
- Необъяснимая потеря веса.
- Изнуряющий кожный зуд.
Как лечить?
В зависимости от вида и стадии лимфомы применяются химио-, лучевая, иммунная и таргетная терапии, трансплантация костного мозга. В большинстве случаев лечение комбинированное
Думала, что со мной такого произойти не может
Катя де Йонг, 42 года, домохозяйка, живет в Псковской области.
Диагноз: анапластическая крупноклеточная лимфома. Прошла 22 курса химиотерапии, перенесла трансплантацию костного мозга. В ремиссии с 2016 года.
В апреле 2013 года мы отдыхали в Египте, там у меня начала подниматься температура до 38,5C, знобило в жару. Появился болезненный шарик подмышкой. По страховке обратилась к доктору, он предположил инфекцию и назначил антибиотик в таблетках. Состояние ухудшалось, появились боли внутри тела. Антибиотик поменяли на внутривенный, но лучше не становилось.
Вернувшись в Россию, сразу обратилась в поликлинику по месту жительства. Опять предположили инфекцию, но по анализам все было чисто. А вот на рентгене легких нашли затемнения, заподозрили туберкулез и направили в тубдиспансер. Диагноз не подтвердился.
После УЗИ надключичных лимфоузлов меня прозвали «воздушный шоколад» — так много увеличенных лимфоузлов там оказалось. Мне выдали направление в онкологическую больницу в 70 км от дома.
Я была уверена, что онкологический диагноз не подтвердится — он казался страшным и смертельным. Думала, что со мной такого произойти не может. К сожалению, пункция показала наличие атипичных клеток.
Состояние ухудшалось с каждым днем, не болели только руки и ноги. Боль удавалось снимать только временно. Еда не усваивалась, таблетки и куски пищи проглотить уже не могла.
Врачи назначили день комиссии, чтобы решить вопрос с диагнозом и лечением. Это было в начале мая, доктор сказал, что впереди майские праздники, поэтому биопсию сделают только в середине месяца, потом дней 10 ждать результат. Если будут вопросы по результатам, материал придется отправлять в Санкт-Петербург для уточнения. Я объяснила, что с каждым днем все хуже себя чувствую, попросила сразу в Петербург ответ отправить, чтобы ускорить процесс. Доктор ответил, что такой необходимости нет и квоту в Санкт-Петербург мне не дадут. Сказал, что у меня лимфома Ходжкина, они ее и сами лечить могут, направление в другую больницу мне не нужно. Но это был неверный диагноз.
На семейном совете решили сменить врача и поехали самостоятельно в онкоцентр в Песочном. Там праздничных дней было немного, и вскоре мне сделали биопсию. КТ легких и малого таза, МРТ брюшной полости и иммуногистохимическое исследование для уточнения вида опухоли сделали платно. Недели через три поставили диагноз, и в конце мая меня взяли на лечение в НМИЦ онкологии им. Н. Н. Петрова. Очень благодарна грамотной работе врачей этого центра!
Лечилась я в общей сложности три года. За это время познакомилась со многими пациентами и поняла, что очень часто из регионов России сложно попасть в федеральные клиники — трудно добиться направления от местной поликлиники, получить квоту на лечение из-за большой очереди. Проблема в том, что болезнь ждать не собирается: лимфома может быть вялотекущей, а может быть очень агрессивной, как например, в моем случае. Обследования надо пройти в кратчайшие сроки и тогда станет понятно, где предпочтительней лечиться пациенту.
Разница между ближайшим и федеральным онкоцентрами не только в удаленности от дома, но иногда и в профессионализме врачей, наличии необходимого оборудования и препаратов.
Людям, которые заподозрили у себя лимфому, я бы посоветовала меньше читать интернет и не примерять на себя чужие истории. Например, считается, что при лимфоме лимфоузлы не болят. В моем случае они были очень болезненны. Необходимо четко следовать рекомендациям врачей и прислушиваться к своему сердцу - желательно, чтобы оно было «холодным». И самое главное, — не дать стержню внутри сломаться. Из возможных вариантов необходимо выбрать цель «ВЫЖИТЬ» и любыми путями двигаться к ней. На пути будут кочки и горы, важно подниматься, карабкаться и приближаться к цели.
Практически с самого начала я подозревала лимфому
Полина, 26 лет, фрилансер, живет в Северной Осетии.
Диагноз: лимфома Ходжкина. Прошла 6 курсов химиотерапии и 15 сеансов лучевой терапии. В ремиссии с 2016 года.
Моя лимфома началась по необычному сценарию. Первым звоночком были красноватые круглые уплотнения на голени обеих ног 1-2 см в диаметре. Их было немного — где-то 5-6. Недели через две после появление этих уплотнений я нащупала на шее лимфоузел, небольшой, около сантиметра. Это меня очень смутило, так как у меня никогда не увеличивались лимфоузлы. Также я стала чувствовать дискомфорт в грудной клетке, мне было сложно дышать, лежа на правом боку.
Тогда я подумала, что это межреберная невралгия, но позже оказалось, что это опухоль в 7 см сдавливала легкое. У меня не был ни ночной потливости, ни субфебрильной температуры, ни потери веса, несмотря на прогрессирующее заболевание.
В первую очередь я обратилась к терапевту, но не получила внятных объяснений. Врач лишь предположил, что это варикоз и направил к сосудистому хирургу. Тот, особо не вникая в суть дела, выписал свое лечения. Я по своей инициативе сдала общий анализ крови, и там были отклонения — повышенные СОЭ и лейкоциты, пониженные лимфоциты, которые заставили меня сомневаться в варикозе. Изучая статьи в интернете, я поняла, что эти уплотнения на ногах называются узловатой эритемой, и лечит их дерматолог. Я обратилась к дерматологу, упомянув также об увеличенных лимфоузлах (к тому времени появилось еще несколько на шее и ключице), дерматолог также не вникал в мои жалобы и прописал свое лечение.
Я продолжала искать информацию в интернете и выяснила, что увеличенные лимфоузлы могут быть от мононуклеоза, вызванного вирусом Эпштейна-Барр. Кроме того, я сделала УЗИ брюшной полости — там тоже было множество увеличенных лимфоузлов. Я по своей инициативе сдала анализ на вирус Эпштейна-Барр, и он подтвердился. Также прошла КТ: она показала все увеличенные лимфоузлы на шее, ключице, в грудной клетке, брюшной полости.
Со результатами всех обследований я пошла к инфекционисту в районную поликлинику. Но врач, пожилая женщина, всю жизнь проработавшая инфекционистом, ничего не знала о вирусе Эпштейна-Барр и о его связи с лимфомой. Тогда я обратилась к платному инфекционисту, и она заподозрила лимфому. От момента появления симптомов до постановки диагноза прошло примерно 5 месяцев.
Практически с самого начала я подозревала лимфому. У меня никогда в жизни не увеличивались никакие группы лимфоузлов. Врачи, к которым я обращалась, не слушали меня и говорили, что я слишком хорошо выгляжу для человека, у которого может быть рак, да и симптомов, по их мнению, у меня было недостаточно для постановки такого диагноза.
Я бы посоветовала воспринимать болезнь, как один из этапов жизни, не приятный, но который нужно прожить. Конечно, находясь в моменте, я так не считала: переживала, что не смогу вернуться к прежней жизни, постоянно буду бояться рецидива, не смогу иметь детей после химиотерапии — у меня пока детей нет, но репродуктивная функция полностью восстановлена. Много переживаний было связано с тем, как я буду переносить химию, но все прошло намного легче, чем я себе это представляла. Если бы можно было отмотать время назад, то я меньше бы переживала и накручивала себя.
Я не видела у себя симптомов рака
Екатерина, 22 года, студентка медицинского университета, живет в Санкт-Петербурге.
Диагноз: лимфома Ходжкина. Прошла 6 курсов химиотерапии, 18 сеансов лучевой терапии. В ремиссии с 2016 года.
В 2013 году у меня были эпизоды аритмии неуточненного генеза. Кардиолог не мог найти причину. Позднее мы выяснили, что это опухоль длиной 9 см давила на перикард. Аритмия со временем прошла, но я начала терять в весе: было желание прийти в форму, но фактическая потеря веса превышала ожидаемую. Через 6-8 мес появилась усталость, началась аменорея, но вес вернулся.
Я обратилась к гинекологу и эндокринологу. Гинеколог назначил УЗИ малого таза — там все было в норме. Эндокринолог велел проверить половые гормоны и гормоны щитовидной железы. Половые гормоны были не в норме, но доктор сказал, что это не его компетенция. Мне не пришло в голову начать свои поиски с терапевта.
Я практически не ходила к врачам, так как училась на 1 курсе в чужом городе. Гинеколог и эндокринолог от меня отмахнулись. Больше мне не к кому было пойти, и со временем я сама себя успокоила.
Я не видела у себя симптомов рака. Ежедневно проходила 10-12 км, продолжала следить за питанием: вес закономерно подрастал при погрешностях в еде. Усталость списывала недостаток витамина Д — я же все-таки в Петербурге живу.
Диагноз мне поставили в тубдиспансере в 2015 году. Плановая флюрография перед летней сессией показала затемнение в средостении. Фтизиатр дал слово разобраться: поставить диагноз за неделю и позволить мне выйти на сессию. Уже тогда на рентгене было видно, что это не туберкулез. Доктор меня поддержал и слово свое сдержал. Я очень благодарна ему, так как успела вовремя закрыть сессию. В дальнейшем я не брала академический отпуск и смогла остаться в своем университете во время лечения, которое продолжалось около полугода.
Если вы чувствуете в себе изменения, а вам говорят, что вы здоровы и это фантазия — не верьте. Ищите грамотного доктора с широким кругозором, читайте статьи на специальных сайтах для пациентов. Разберитесь в своей проблеме. Кто, если не вы?
Благодарим врача-гематолога Алексея Константиновича Титова за помощь в подготовке текста.
Татьяна Бобровицкая
Саша Васильева
Лимфогранулематоз (ходжкинская лимфома) | Фонд «Подари жизнь»
Суть болезни
Лимфогранулематоз (ЛГМ, болезнь Ходжкина, лимфома Ходжкина) – заболевание лимфатической системы, особый тип лимфомы, то есть злокачественного заболевания, где опухолевая ткань возникает из лимфоцитов. Для ЛГМ характерно прежде всего опухолевое поражение лимфатических узлов с постепенным распространением заболевания от одной группы лимфоузлов к другой. Могут поражаться также другие органы, прежде всего селезенка, а также печень, легкие, кишечник, костный мозг и т.п.
Отличительной чертой ЛГМ по сравнению с другими лимфомами является присутствие в пораженных болезнью лимфоузлах особого типа клеток, называемых клетками Березовского-Штернберга-Рид. Это гигантские клетки, возникшие из B-лимфоцитов.
В зависимости от распространенности процесса различают четыре стадии ЛГМ.
- Стадия I – вовлечены лимфоузлы только одной области или один орган вне лимфоузлов.
- Стадия II – вовлечены лимфоузлы в двух или более областях с одной стороны диафрагмы или одна группа лимфоузлов и один орган также с одной стороны диафрагмы.
- Стадия III – вовлечены лимфоузлы с обеих сторон диафрагмы; возможно также поражение селезенки и других органов вне лимфоузлов.
- Стадия IV – наблюдается распространенное поражение одного или более внутренних органов – таких как печень, костный мозг, легкие, кишечник; оно может сопровождаться или не сопровождаться поражением лимфоузлов.
В обозначении стадии заболевания могут использоваться также дополнительные символы: А (системные клинические симптомы отсутствуют), В (присутствуют), E (вовлечены не только лимфоузлы, но и другие органы), S (вовлечена селезенка).
Различают несколько гистологических вариантов ЛГМ: с нодулярным склерозом (40-50% всех случаев ЛГМ), смешанноклеточный (около 30% всех случаев ЛГМ), с лимфоидным преобладанием и с истощением лимфоидной ткани (редкие варианты).
Частота встречаемости, факторы риска
ЛГМ имеет два возрастных пика заболеваемости: один в молодом возрасте (15-35 лет), второй в пожилом. ЛГМ встречается в среднем с частотой около 1 случая на 25 тысяч населения в год, при этом дети и подростки составляют около 10-15% заболевших, а у детей дошкольного возраста болезнь встречается редко. Мужчины болеют несколько чаще женщин.
Факторы, влияющие на риск заболевания ЛГМ, постоянно изучаются. Могут играть роль как генетическая предрасположенность, так и некоторые вирусные инфекции. Так, считается, что риск развития ЛГМ повышен у людей, инфицированных вирусом Эпштейна-Барр (широко распространенным вирусом из группы герпетических вирусов). Риск развития ЛГМ увеличивается при иммунодефицитных состояниях, включая СПИД.
Признаки и симптомы
При ЛГМ наблюдается безболезненное увеличение лимфатических узлов – чаще всего шейных и надключичных, лимфоузлов грудной полости (области средостения), порой подмышечных, паховых и лимфоузлов брюшной полости. Это самый характерный симптом болезни. Взрослые больные иногда отмечают, что увеличенные лимфоузлы становятся болезненными после приема алкоголя.
Важными симптомами являются ночная потливость, повышение температуры и снижение веса. Наличие этих «системных» симптомов отражается буквой «В» в обозначении стадии болезни и играет роль в оценке активности опухоли. Среди других возможных симптомов можно назвать утомляемость, увеличение печени и/или селезенки, боли в спине, кожный зуд. Из-за увеличенных лимфоузлов грудной полости могут возникнуть затрудненное дыхание, кашель.
По мере развития опухолевого процесса самочувствие больного ухудшается. На поздних стадиях развития болезни может наблюдаться желтуха, если опухоль распространилась в печень и перекрывает желчные протоки. Могут возникать отеки лица, шеи и рук (так называемый синдром сдавления верхней полой вены), отеки ног.
Диагностика
Чтобы отличить ЛГМ от других онкологических и неонкологических заболеваний, необходимо провести исследование опухоли – увеличенного лимфатического узла или очага в других тканях тела. Для этого производят его хирургическое удаление или биопсию с микроскопическим и иммуногистохимическим исследованием образца. Обнаружение клеток Березовского-Штернберга-Рид (крупных клеток особого вида, специфичных для ЛГМ) и их предшественников (клеток Ходжкина) является важным признаком ЛГМ; эти опухолевые клетки окружены другими клетками – лимфоцитами, эозинофилами и др.
Для обнаружения конкретных пораженных опухолью участков – лимфатических узлов и/или внутренних органов – используют различные методы визуализации: рентгенографию, ультразвуковое исследование (УЗИ), компьютерную томографию (КТ) и позитронно-эмиссионную томографию (ПЭТ). Именно ПЭТ считается самым эффективным тестом для определения стадии ЛГМ и оценки ответа на лечение. Возможны и другие исследования.
Производится костномозговая пункция и/или трепанобиопсия с последующим исследованием образца костного мозга, чтобы понять, поражен ли болезнью этот орган.
Лечение
Лечение ЛГМ основано на сочетании химиотерапии и облучения. Выбор конкретной терапии зависит от варианта болезни, возраста пациента, стадии (локальное или распространенное поражение организма), сопутствующих заболеваний и других факторов.
В химиотерапии ЛГМ у детей и подростков в России успешно используют протоколы, предложенные немецкими онкогематологами. Эти протоколы позволяют получить высокий процент излечения с минимальными побочными эффектами, что очень важно при этой болезни. Также могут применяться курсы ABVD (адриабластин, блеомицин, винбластин, дакарбазин), BEACOPP (блеомицин, этопозид, адриамицин, циклофосфамид, винкристин, прокарбазин, преднизон) и другие химиотерапевтические курсы, количество которых определяют в зависимости от стадии болезни.
За химиотерапией следует лучевая терапия. Дозу облучения определяет врач-онкогематолог в зависимости от стадии заболевания, используемого протокола и облучаемого органа.
При оценке предпочтительности различных протоколов следует учитывать не только их эффективность в лечении основного заболевания, но также токсичность и повышение вероятности возникновения новых (вторичных) онкозаболеваний после терапии. Больные, излечившиеся от ЛГМ, и врачи, их наблюдающие, должны помнить о риске развития вторичных опухолей и о необходимости регулярных осмотров.
В сложных случаях (устойчивость болезни к терапии, рецидивы) может применяться высокодозная терапия с аутологичной трансплантацией костного мозга. Аллогенная трансплантация используется лишь в редких случаях.
В последние годы у больных ходжкинской лимфомой появились новые шансы. В случае отсутствия ответа на стандартную терапию или рецидива болезни могут использоваться схемы химиотерапии с новейшим препаратом «Адцетрис» (брентуксимаб ведотин) или иммунотерапии с препаратом «Опдиво» (ниволумаб).
Прогноз
ЛГМ относится к числу тех опухолевых заболеваний, которые наиболее эффективно излечиваются на современном уровне развития медицины. Среди молодых пациентов выздоравливают около 90% больных. У пожилых пациентов выживаемость хуже, но в среднем прогноз все равно достаточно хороший. Даже в случае рецидива можно излечивать около половины пациентов.
Прогноз, разумеется, зависит также от стадии заболевания: среди пациентов, у которых болезнь была диагностирована на стадиях I-II, доля излечивающихся превышает 90%, тогда как при обнаружении ЛГМ на стадии IV эта доля снижается до 65-70%.
После пятилетней ремиссии болезнь, как правило, считается излеченной. Однако и после излечения от ЛГМ необходима пожизненная онкологическая настороженность, так как вторичные опухоли иногда развиваются даже через 10-20 лет после окончания лечения. Могут возникнуть и другие отдаленные последствия – например, кардиомиопатия (поражение миокарда) как следствие химиотерапии. Благодаря разработке новых протоколов вероятность побочных эффектов уменьшается, однако полностью исключить их нельзя.
Рецидивы локальных неходжкинских лимфом после полных ремиссий Текст научной статьи по специальности «Клиническая медицина»
РЕЦИДИВЫ ЛОКАЛЬНЫХ НЕХОДЖКИНСКИХ ЛИМФОМ ПОСЛЕ ПОЛНЫХ РЕМИССИЙ
в.м. сотников
Российский научный центр рентгенорадиологии М3 РФ, Москва. 117997,
ул. Профсоюзная, д. 86 М.А. ИЛЬИН Кафедра онкологии и рентгенорадиологии,.
РУДН, Москва, 117198, ул. Миклухо-Маклая, д.8, Медицинский факультет
Анализ рецидивов необходим для совершенствования программ лечения любой группы онкологических заболеваний. Целью данной работы было изучение некоторых особенностей рецидивирования неходжкинских лимфом. Материалом исследования послужили данные наблюдения за 406 взрослыми первичными больными неходжкинскими лимфомами, с 1-11 стадиями заболевания, получившими лекарственное, лучевое или комплексное химиолучевое лечение. Рецидивы изучались только в группе больных с полной ремиссией, для исключения прогрессирования заболевания при частичной ремиссии. Средний срок наблюдения составил 64,8 месяца. В связи с особенностями клинического течения исключены кожные лимфомы. Анализировались два фактора: программа лечения и размер первичного очага. Установлено, что наименьшее количество рецидивов наблюдается после химиолучевого лечения, как за счет истинных, так и за счет генерализованных рецидивов, в то время как другие программы лечения влияют преимущественно на локальные рецидивы (лучевая терапия), либо на генерализацию заболевания (химиотерапия). Установлено, что опухоли больших размеров являются факгором прогноза генерализации, а не истинного рецидива. Следоватещно, такие больные нуждаются в максимальной интенсификации химиотерапии.
Термин "неходжкинские лимфомы" (НХЛ) объединяет ряд опухолевых заболеваний, генетически родственных происхождением из лимфоидных клеток, но существенно отличающихся по клиническим проявлениям, прогнозу и реакции на лечение.
Современные программы лечения позволяют получить полные ремиссии у большинства больных, однако проблема рецидивов и их прогнозирования продолжает оставаться актуальной. Клинические наблюдения выявляют некоторые закономерности рецидивирования различных видов неходжкинских лимфом. Так, для лимфобластных лимфом независимо от первичной их локализации характерны рецидивы по типу генерализации с поражением костного мозга и центральной нервной системы [5]. Модулярные лимфомы рецидивируют преимущественно по лимфатическим узлам [3], что и определяет целесообразность программ тотального нодального облучения при этом типе лимфом [6].
В литературе имеются сообщения о рецидивах неходжкинских лимфом после лекарственного лечения [2], лучевой терапии [1,7]. В связи с этим представляет интерес сравнение частоты и характера рецидивов после различных программ лечения неходжкинских лимфом, в том числе включающих химиотерапию и лучевую терапию. Химиолучевое лечение радиочувствительных опухолей, к которым относятся и неходжкинские лимфомы, имеет солидное теоретическое обоснование [4], которое нуждается в клинической проверке.
Лимфомы больших размеров традиционно считаются фактором риска истинных рецидивов [8]. Однако клинические наблюдения не всегда коррелируют с общепринятыми положениями, требующими статистического подтверждения.
Задача исследования.
Анализ особенностей рецидивирования локальных неходжкинских лимфом (1-11 стадии заболевания) после достижения полной ремиссии. Данная 1руппа больных лимфомами была выбрана не случайно. Изначальная клиническая локальность заболевания и его полная излеченность позволяет четко определить локализацию и размеры первичного очага, а также разграничить понятия рецидива и прогрессирования заболевания.
Материал и методы.
В 1983-2000г. в Российском научном центре рентгенорадиологии М3 и СО РФ проведено лечение 406 первичных больных с морфологически подтвержденным диагнозом неходжкинской лимфомы. Мужчин было 188, женщин - 218. Возраст больных составлял от 16 до 79 лет (средний возраст 49,2 года). В исследование включались все локализации лимфомы, как лимфатические (лимфатические узлы, селезенка, кольцо Вальдейера), так
и экстралимфатаческие (кости, желудочно-кишечный тракт, легкие, щитовидная железа и т.д.), за исключением кожных лимфом и лимфом центральной нервной системы.
Всем больным до начала лечения выполнялось тщательное обследование с использованием современных методов медицинской визуализации: ультразвуковое исследование периферических лимфатических узлов, брюшной полости, компьютерная томография грудной клетки и брюшной полости, цитологическое и гистологическое исследование костного мозга. У всех больных при обследовании констатирована 1-Н стадия заболевания по классификации Анн-Арбор, модифицированной в соответствии с особенностями клинического течения неходжкинских лимфом [9].
Больным проводились три различных программы лечения: химиолучевая программа (255 больных), лучевая терапия (82 больных), химиотерапия (69 больных). После окончания лечения. После окончания лечения все больные ежегодно проходили регулярное контрольное обследование. Сроки наблюдения за больными составили от 2 до 17 лет, в среднем 64,8 месяца.
В соответствии с рекомендациями ВОЗ и Международного противоракового союза [10] непосредственный эффект лечения злокачественных неходжкинских лимфом расценивался следующим образом.
Полная ремиссия (ПР) - исчезновение всех очагов поражения с нормализацией клеточного состава периферической крови и костного мозга на срок не менее 4 недель.
Частичная ремиссия (ЧР) - большее или равное 50% уменьшение всех или отдельных очагов при отсутствии прогрессирования других очагов в течение не менее 4 недель.
Без эффекта (БЭ) - все остальные случаи, включающие стабилизацию (уменьшение менее чем на 50% при отсутствии новых поражений или увеличение не более чем на 25%) и прогрессирование (большее или равное 25% увеличение размеров одной или более опухолей или появление новых поражений).
Мы выделяли следующие тины рецидивов:
а) истинные рецидивы - возобновление роста всех или части очагов лимфомы, существовавших до начала лечения;
б) генерализованные рецидивы - появление новых зон поражения без возобновления роста ранее существовавших очагов;
в) смешанные рецидивы (истинный рецидив + генерализация) - появление новых очагов и возобновление роста всех или части ранее существовавших очагов.
Статистическая обработка результатов исследования проводилась с использованием стандартной процедуры вычисления средних величин. Достоверность различий средних величин определялась с помощью критерия Стьюдента.
Результаты.
Полная ремиссия получена у 319 больных (78,6 %). За время последующего наблюдения рецидивы выявлены у 122 больных с полной ремиссией (38,2%). У 12 больных (3,8%) наблюдались изолированные истинные рецидивы, у 13 больных (4,1%) истинные рецидивы сочетались с генерализацией процесса (смешанные рецидивы). У 97 больных (30,4%) рецидивы протекали по типу генерализации при излеченном первичном очаге. Таким образом, среди типов рецидивов абсолютно преобладала «чистая» генерализация -79,5% всех рецидивов.
После лучевого лечения рецидивы наблюдались у 75,0% больных (8,3% - истинные, 2,1% - смешанные, 64,6% - генерализация). После химиолучевого лечения рецидивы развились у 54,6% больных (1,7% - истинные, 7,4% - смешанные, 45,5% - генерализация). После химиотерапии общее количество рецидивов - 71,4% (14,3% - истинные, 32,1% - смешанные, 25,0% - генерализация). Достоверные (Р<0,05) различия отмечены:
а) между лучевой и химиолучевой программами: по общему количеству рецидивов, количеству истинных и генерализованных рецидивов;
б) между химиолучевой программой и химиотерапией: по истинным и смешанным рецидивам.
Различия по общему количеству рецидивов и генерализован!шм рецидивам двух последних программ близки к достоверным (Р<0,1).
Структура рецидивов проанализирована раздельно в трех группах больных: с максимальным размером опухоли соответственно до 5 см (86 больных), 5-9см (127 больных), 10 и более см (106 больных) (табл.1).
Таблица 1
Структура рецидивов неходжкинских лимфом при различной величине ____________________ первичного очага ___________________________
Размер (см) Число больных Всего рецидивов Истинные рецидивы Генерализо-ванне рецидивы Смешанные рецидивы
<5 86 44,2%* 8,1%* 31,4% 4,7%
5-9 127 30,7%* 1,6%* 24,4%* 4,7%
>9 106 42,4% 2,8% 36,8%* 2,8%
Примечание: * - различие достоверно, Р<0,05.
Общее число рецидивов по выделенным группам составило 44,2±5,4%, 30,7±3,4%, 42,4±4,8% (различие между первой и второй ¡руппами достоверны, Р<0,05, между второй и третьей группами - близки к достоверным). Количество истинных рецидивов составило 8,1+2,9%, 1,6±1,1%, 2,8±1,6% (различие между первой и второй группами достоверны, Р<0,05), количество генерализованных рецидивов - 31,4±5,0%, 24,4+3,8%, 36,8±4,7% (различие между второй и третьей группами достоверны, Р<0,05). Количество смешанных рецидивов во всех трех группах существенно не различалось.
Суммируя эти данные, можно заключить, что после химиолучевого лечения развивается существенно меньшее количество рецидивов, чем после химиотерапии или лучевой терапии, примененных в качестве самостоятельных методов лечения локальных неходжкинских лимфом. В сравнении с лучевой программой это происходит за счет уменьшения числа истинных и генерализованных рецидивов, а в сравнении с химиотерапией - за счет истинных и смешанных рецидивов. Таким образом, сложение системного и локального лечебного эффекта химиотерапии и лучевой терапии в рамках программы химиолучевого лечения злокачественных неходжкинских лимфом в наибольшей степени способствует достижению длительных полных ремиссий у этой категории больных, что подтверждает проведенные ранее теоретические расчеты [4].
Наличие опухолей больших размеров у больных локальными неходжкинскими лим-фомами является фактором риска не местного, а генерализованного рецидива, что необходимо учитывать при планировании лечения. Следует подчеркнуть, что этот вывод правомерен для химиолучевого лечения, которое получало большинство больных с исходно большими опухолями. Эта группа больных нуждается в максимальной интенсификации химиотерапии. Факт увеличения общего количества рецидивов и местных рецидивов у больных с исходным размером опухоли менее 5 см пока не находит реального объяснения и требует дальнейшего детального изучения с анализом морфоиммунологических вариантов лимфомы.
Литература
1. Круглова Г.В., Иендхакар Д.Я.П. Клиника и лечение рецидивов лимфосарком после лучевой терапии // Гер. архив - 1985.-Т.6.-N 5.- С. 110-114.
2. Круглова Г.В., Жаргалбекова Р.Т. Рецидивы лимфосарком после интенсивной цикловой полихимиотерапии и их лечение // Гематол. и трансфузиол,- 1985.- Т.30.- N 7.- С.25-32.
3. Anderson J., Vose J., ¡Herman P. Clinical features and prognosis of follicular large-cell lymphoma: A report from Nebraska Lymphoma Study Group // J. Clin. Oncol - 1993.- Vol. 11.- N 2.-P.218-24.
4. Arriagada K.. Cosset J.M., Cheralier T. The value of adjunctive radiotherapy when chemotherapy the major curative method//Int. J. Radiat. Oncol. Biol., Phys.- 1990.- Vol.19.- N 5.-P. 1279-1284
5. Bernasconi C., Briisamolino E. Lymphoblastic lymphoma in adult patients: clinico-pathological features and response to in-tensive multiagent chemotherapy analogous to that, used in acute lymphoblastic leukemia // Ann. Oncol.- 1990.-Vol.1. - N 2,- P.141-146.
6. Jacobs J., Murray K.. Schults C. et al. Central lymphatic irradiation for stade III nodular malignant lymphoma long-term results // J. Clin. Oncol.- 1993.- Vol. 11.- N 2.- P.233-238.
7. Hallahan D.E., Farah H., Vokes E.E. et al. The problems of failture in patients with pathological stage I and II diffuse histiocytic lymphoma treated with radiation therapy alone // Int.J. Radiat. Oncol. Biol., Phys- 1989,- Vol. 17.-N 4,- P.767-771.
8. Shipp M.A., Klatt M.M., Jeap B.J. et al. Patterns of relapse in large cell lymphoma patients with bulk disease: implication for the use of adjuvant radiation therapy // J. Clin. Oncol.- 1989.- Vol.7.- N 2,- P.613-618.
9. Tubiana M., Le Bourgeos J.-P. Classification and the schedule of investigation the patients with haemato-sarcoms. //Bull, cancer.-1974.- Vol.61.- N 1,-P.39-50.
10 WHO Handbook for Reporting Results of Cancer Treatment.-Geneva, 1979.- Vol.48.
PATTERNS OF RELAPSE OF LOCAL NON-IIODGKINS LYMPHOMAS AFTER FULL REMISSION
V.M.SOTNIKOV
Russian scientific center of roentgenoradiology, M3 P®, Moscow, J17997,
Profsouyznaya st. 86 M.A.ILYIN
Department of oncology and roentgenoradiology RPFU, Moscow, 117198, M-Maklaya st 8,
Medical faculty.
Analysis of relapses is necessary for perfection of programs of treatment of any group of oncological diseases. The purpose of the given work was to investigate some features of relapses of non hodgkins lymphomas. The data of 406 adult therapeutically na'ive non hodgkins lymphoma patients, with l-II the stages of the disease was analyzed. Three therapeutical programs were realized: chemotherapy (69 patients), radiation therapy (82 patients) chemotherapy f radiation therapy (255 patients). Relapses were studied only in group of patients with full remissions. All primary sites of lymphoma were included, except skin and brain lymphoma.
Average time of follow up is 64,8 months (2-17 years). In connection with features of clinical current are excluded skin jihm$omh. Two factors were analyzed: the program of treatment and the size of the primary tumor. It is established, that the least quantity of relapses is observed after chemoradiation therapy. Comparing with radiation therapy chemoradiation program diminish both the true relapses and the distant relapses (P<0,05). Comparing with chemotherapy it diminish only true and mixed relapses (P<0,05).
. It is established, that big tumors (bulky disease) are the statistically proved unfavorable factor of lymphoma generalization, not the local relapse. Keeping in mind that the majority of this patients undergone chemoradiation therapy, such patients require further intensification of chemotherapy.
Key words: non-Hodgkins lymphoma, therapy, relapses
Рак лимфомы: Ходжкин против неходжкинских - Рак
Главная › Рак лимфомы: Ходжкин против неходжкинских - Рак - 2020Лимфома, тихий вид рака, который успешно лечится при своевременной диагностике (Февраль 2020).
В чем разница между лимфомой Ходжкина и Неходжкина?
- Как взрослая лимфома Ходжкина, так и неходжкинская лимфома являются видами рака, которые развиваются в лимфатической системе, являющейся частью иммунной системы организма.
- Разница между лимфомой Ходжкина и неходжкинской лимфомой заключается в том, что рак развивается у разных лимфоцитов. Если обнаружен определенный тип аномальной клетки, называемой клеткой Рида-Штернберга, лимфома классифицируется как Ходжкин. Неходжкинская лимфома может начинаться в В-лимфоцитах (также называемых В-клетками), Т-лимфоцитах или естественных киллерных клетках.
- Признаки лимфомы Ходжкина и неходжкинской лимфомы сходны и включают отек в лимфатических узлах в области шеи, подмышек, паха или желудка; лихорадка по неизвестной причине, ночные поты, потеря веса по неизвестной причине, зуд кожи и чувство усталости.
- Дополнительные симптомы неходжкинской лимфомы, которые отличаются от лимфомы Ходжкина, могут включать кожную сыпь или боль в грудной клетке, животе или костях по неизвестной причине.
- Факторы риска для лимфомы Ходжкина включают в себя молодую или позднюю взрослую жизнь, будучи мужчиной, инфицированным вирусом Эпштейна-Барра и имеющим родственник первой степени с лимфомой Ходжкина.
- Факторы риска для неходжкинской лимфомы включают старшие, мужские или белые; с наследственным иммунным расстройством, аутоиммунным заболеванием, ВИЧ / СПИДом, вирусным вирусом T-лимфотрофического вируса человека I или вирусом вируса Эпштейна-Барра или инфекцией Helicobacter pylori; и принимать иммунодепрессанты после трансплантации органов.
- Лечение лимфо