Диэтиловый эфир формула
Диэтиловый эфир | Инструкция по применению лекарств, аналоги, отзывы
Описание действующего вещества Диэтиловый эфир / Aether diaethylicus.
Формула: C4h20O, химическое название: 1,1-окси-бис-этан.
Фармакологическая группа: нейротропные средства/ наркозные средства.
Фармакологическое действие: наркозное.
Фармакологические свойства
Диэтиловый эфир является лекарственным средством для ингаляционного наркоза. Диэтиловый эфир представляет собой прозрачную, бесцветную, очень подвижную, летучую жидкость со жгучим вкусом и своеобразным запахом. Эфир для наркоза содержит 96 — 98 % диэтилового эфира. Плотность эфира медицинского составляет 0,714 — 0,717, эфира для наркоза — 0,713 — 0,714, температура кипения — соответственно 34 — 36 и 34 — 35 градусов Цельсия. При испарении 1 мл эфира для наркоза образуется 230 мл пара, который имеет плотность — 2,6 и относительную молекулярную массу — 74. Диэтиловый эфир разлагается под действием тепла, света, влаги и воздуха с образованием токсичных кетонов, пероксидов, альдегидов, которые раздражают дыхательные пути. Растворимость диэтилового эфира в воде составляет 1 к 12. Диэтиловый эфир смешивается с бензолом, спиртом, жирными и эфирными маслами во всех соотношениях. Диэтиловый эфир легко воспламеняется, включая его пары. В определенном соотношении с воздухом, кислородом, динитрогена оксидом пары эфира для наркоза являются взрывоопасными.
Диэтиловый эфир неспецифически взаимодействует с мембранами нервных клеток, в основном с двуслойными липидными мембранами аксонов спинного, продолговатого и головного мозга, и обратимо изменяет их функции и ультраструктуру. Диэтиловый эфир угнетает центральную нервную систему: препятствует синаптической передаче возбуждения (преимущественно афферентной импульсации), функционально дезинтегрирует корково-подкорковые взаимодействия, при этом сохраняется активность бульбарных центров. Диэтиловый эфир оказывает наркотическое, мышечно-расслабляющее и анальгезирующее действие. При применении диэтилового эфира отчетливо развиваются выраженные классические стадии наркоза: анальгезия, возбуждение, хирургический наркоз с тремя уровнями (поверхностный, средний, глубокий) и характерными признаками — угнетение рефлекторных реакций, отсутствие всех видов чувствительности и сознания, расслабление скелетной мускулатуры. Диэтиловый эфир вызывает наркоз, который характеризуется выраженной стадией возбуждения. Наркоз наступает медленно и нередко сопровождается сильным возбуждением и двигательной активностью. Выход из наркоза также происходит медленно.
При премедикации и на фоне других неингаляционных или ингаляционных общих анестетиков классическая картина наркоза диэтилового эфира изменяется значимо.
На стадии анальгезии диэтиловый эфир снижает функциональную активность нейронов коры головного мозга, оказывает амнестическое действие.
В стадии возбуждения диэтиловый эфир угнетает кору головного мозга, выключает субординационные механизмы, которые контролируют состояние подкорковых структур (преимущественно среднего мозга). Увеличение активности подкорковых образований проявляется вариабельностью артериального давления, частоты пульса, дыхания, психомоторным возбуждением и другими признаками. У взрослых данная стадия выражена в большей степени, чем у детей, и выражена в меньшей степени (или отсутствует) при премедикации и базисном наркозе. Диэтиловый эфир раздражает слизистые оболочки, включая ротовой полости, вызывает гиперсаливацию (усиливает секрецию слюнных желез). Через рецепторные зоны гортанного, тройничного, блуждающего нервов диэтиловый эфир увеличивает бронхиальную секрецию, вызывает ларингоспазм, кашель, спазм бронхов (который сменяется расширением бронхов при глубоком наркозе), гипертензию, расстройства деятельности сердца (брадикардия или тахикардия, остановка сердца) и дыхания (рефлекторная стимуляция или угнетение, вплоть до апноэ). При попадании слизи или слюны, которые насыщены диэтиловым эфиром, в желудок препарат раздражает его слизистую оболочку, рефлекторно стимулирует рвотный центр, вызывает тошноту и рвоту как вначале наркоза, так и при пробуждении.
В стадии хирургического наркоза диэтиловый эфир существенно угнетает передачу между нейронами в спинном и головном мозге. Диэтиловый эфир увеличивает активность отделов гипоталамуса, которые регулируют функцию симпатической нервной системы и системы гипофиз — кора надпочечников, повышает секрецию катехоламинов и глюкокортикоидов. Диэт
Диэтиловый эфир — Википедия
Материал из Википедии — свободной энциклопедии
| Диэтиловый эфир | |
|---|---|
| Систематическое наименование | 1,1-Окси-бис-этан |
| Хим. формула | C4H10O |
| Состояние | жидкость |
| Молярная масса | 74,12 г/моль |
| Плотность | 0,714 г/см³ |
| Энергия ионизации | 9,53 ± 0,01 эВ[1] |
| Т. плав. | -116,3 °C |
| Т. кип. | 34,65 °C |
| 193,4 °C | |
| Т. всп. | −49 ± 1 °F[1] |
| Пр. взрв. | 1,9 ± 0,1 об.%[1] |
| Давление пара | 440 ± 1 мм рт.ст.[1] |
| Растворимость в воде | (для 20 °С) 6,5 г/100 мл |
| Рег. номер CAS | 60-29-7 |
| PubChem | 3283 |
| Рег. номер EINECS | 200-467-2 |
| SMILES | |
| InChI | |
| RTECS | KI5775000 |
| ChEBI | 35702 |
| Номер ООН | 1155 |
| ChemSpider | 3168 |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 году Роберт Бойль вторично синтезировал эфир. Затем в 1704 году Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 году эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 году Томас Беддоус создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[4]
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа).
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
- (C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}
Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)
В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ 1 2 П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
Ссылки
|
|
Алф. указатель: 1-9 A-Z А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Щ Э Я
Синонимы:
серный эфирэтиловый эфир этоксиэтан
Внешний вид:
бесцветн. жидкость
Кристаллические модификации, цвет растворов и паров:
В твердом виде - ромбические кристаллы.Брутто-формула (система Хилла): C4H10OФормула в виде текста: C2H5OC2H5Молекулярная масса (в а.е.м.): 74,12Температура плавления (в °C): -116,3Температура кипения (в °C): 35,6Растворимость (в г/100 г или характеристика):ацетон: хорошо растворимбензол: хорошо растворим вода: 6,5 (20°C) лигроин: хорошо растворим хлороформ: хорошо растворим этанол: хорошо растворим
Дополнительное описание:
Порог восприятия запаха в воздухе (мг/л) = 0,001Метод получения 1.(лабораторный синтез)Источник информации: "Препаративная органическая химия" М. 1959 стр. 342 В круглодонную широкогорлую колбу емкостью 750 мл помещают 150 мл этилового спирта, затем порциями добавляют, при перемешивании и охлаждении, 150 мл серной кислоты (d=l,84). Колбу закрывают пробкой (резиновые не рекомендуются), сквозь которую пропущены капельная воронка, термометр и трубка, соединяющая колбу с вертикально поставленным спиральным холодильником. Приемником служит колба Бунзена, на боковой отвод которой надета каучуковая трубка, отводящая пары эфира в раковину водопровода. Сборник охлаждают водой со льдом. Ртутный шарик термометра и трубка капельной воронки должны быть погружены в жидкость (но не глубоко). В капельную воронку, с хорошо смазанным краном, вливают 300 мл этилового спирта. Содержимое колбы нагревают на горелке с предохранительной сеткой. Когда температура достигнет 140°, к смеси начинают по каплям, приливать спирт с такой скоростью, чтобы, несмотря на начавшуюся отгонку эфира, уровень жидкости в колбе оставался постоянным. Температура не должна превышать 145° (иначе образуется этилен). По окончании приливания спирта смесь нагревают еще 5 минут, после чего горелку гасят. Дистиллят, содержащий, кроме эфира, воду, спирт и сернистую кислоту, дважды промывают в делительной воронке 100 мл холодного 5%-ного раствора едкого натра. Эфирный слой после отделения дважды промывают 50%-ным раствором хлористого кальция, взятым в количестве, равном половине объема дистиллята. Тщательно отделенный эфирный слой переливают в сухую склянку и сушат хлористым кальцием (не менее 30 г) в течение 4—5 часов. Высушенный эфир отфильтровывают от хлористого кальция и перегоняют с дефлегматором на водяной бане, собирая фракцию, кипящую при 33— 38°. Выход - около 135 г (66% от теоретического). Все работы с эфиром следует проводить вдали от огня. Метод очистки или выделения из смесей 1.Источник информации: Гитис С.С., Глаз А.И., Иванов А.В. "Практикум по органической химии: Органический синтез" М.: Высшая школа, 1991 стр. 47Удалить пероксиды можно действием щелочей или восстановителей — сульфита натрия или соли железа (II). В первом случае эфир встряхивают с порошкообразным гидроксидом калия. Восстановление осуществляют насыщенным на холоду и разбавленным затем в три раза водой раствором сульфита натрия или концентрированным подкисленным раствором соли железа (II). Очистку ведут до тех пор, пока проба перестанет давать реакцию на перокснды. На 1 л эфира берут около 70 г щелочи, 70... 75 мл раствора сульфита натрия или 10...20 мл концентрированного раствора соли железа (11), разбавленного 100 мл воды. Исходный раствор соли железа готовят из 60 г кристаллического сульфата железа (II), 6 мл концентрированной серной кислоты и 110 мл воды, либо из 100 г хлорида железа (II), 42 мл концентрированной соляной кислоты и 85 мл воды. Метод очистки или выделения из смесей 2.Источник информации: Гитис С.С., Глаз А.И., Иванов А.В. "Практикум по органической химии: Органический синтез" М.: Высшая школа, 1991 стр. 47-48Очищенный от пероксидов эфир для удаления примеси этилового спирта промывают водой, а затем насыщенным на холоду раствором хлорида кальция. Промытый эфир переливают в склянку, закрывающуюся корковой пробкой, вносят в нее 150 г безводного хлорида кальция и оставляют стоять не менее чем на сутки, время от времени перемешивая смесь. Затем эфир фильтруют через большой складчатый фильтр в чистую, сухую склянку, следя за тем, чтобы все горелки в радиусе 3 м были выключены. В эфир вносят тонко нарезанные кусочки натрия, очищенного от оксидов, и закрывают корковой пробкой с хлоркальциевой трубкой. Если водород больше не выделяется и поверхность свежих кусочков натрия остается блестящей, то склянку закрывают хорошей корковой пробкой и ставят в темное место. Если поверхность натрня сильно изменилась, необходимо отфильтровать эфир в другую сухую темную склянку и повторить обработку натрием. Иногда эфир дополнительно перегоняют над натрием со всеми предосторожностями, используя предварительно нагретую воздушную баню. Природные и антропогенные источники:Выделяется в небольшой концентрации гречихой при цветении.Плотность:0,7135 (20°C, г/см3)0,70778 (25°C, г/см3) Показатель преломления (для D-линии натрия):1,3526 (20°C)Давление паров (в мм.рт.ст.):1 (-74,3°C)10 (-48,1°C) 40 (-27,7°C) 200 (2,2°C) 400 (17°C) Диэлектрическая проницаемость:4,3 (25°C)Дипольный момент молекулы (в дебаях):1,15 (20°C)Динамическая вязкость жидкостей и газов (в мПа·с):0,242 (20°C)Поверхностное натяжение (в мН/м):17,01 (20°C)Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):172 (ж)Энтальпия кипения ΔHкип (кДж/моль):26,6Температура вспышки в воздухе (°C):-41Температура самовоспламенения на воздухе (°C):164Теплота сгорания Qp(кДж/моль):2726,7Критическая температура (в °C):193,4Критическое давление (в МПа):3,61Дополнительная информация:Входит в список IV (прекурсоры) наркотических и психотропных веществ.
Источники информации:Алф. указатель: 1-9 A-Z А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Щ Э Я Еще по теме: |

|
Формула Диэтилового эфира структурная химическая
Структурная формула
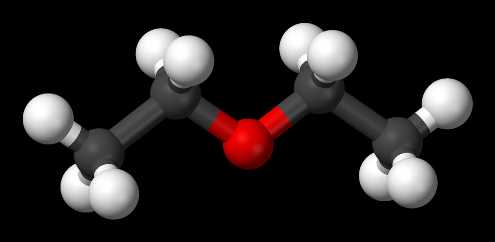 |
Истинная, эмпирическая, или брутто-формула: C4H10O
Химический состав Диэтилового эфира
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12.011 | 4 | 64,8% |
| H | Водород | 1.008 | 10 | 13,6% |
| O | Кислород | 15.999 | 1 | 21,6% |
Молекулярная масса: 74,123
Диэтиловый эфир (этиловый эфир, серный эфир). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В технике применяется как растворитель нитратов целлюлозы в производстве бездымного пороха, природных и синтетических смол, алкалоидов.Применяется как экстрагент для разделения плутония и продуктов его деления при получении и переработке ядерного топлива, при выделении урана из руд. Так же применяется как компонент топлива в авиамодельных компрессионных двигателях и при запуске бензиновых двигателей внутреннего сгорания в суровых зимних условиях.
Диэтиловый эфир — Википедия
Материал из Википедии — свободной энциклопедии
| Диэтиловый эфир | |
| Общие | |
|---|---|
| Систематическое наименование | 1,1-Окси-бис-этан |
| Хим. формула | C4H10O |
| Физические свойства | |
| Молярная масса | 74,12 г/моль |
| Плотность | 0,714 г/см³ |
| Энергия ионизации | 9,53 ± 0,01 эВ[1] |
| Термические свойства | |
| Т. плав. | -116,3 °C |
| Т. кип. | 34,65 °C |
| 193,4 °C | |
| Т. всп. | −49 ± 1 °F[1] |
| Пр. взрв. | 1,9 ± 0,1 об.%[1] |
| Давление пара | 440 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 60-29-7 |
| PubChem | 3283 |
| Рег. номер EINECS | 200-467-2 |
| SMILES | |
| InChI | |
| RTECS | KI5775000 |
| ChEBI | 35702 |
| Номер ООН | 1155 |
| ChemSpider | 3168 |
| Безопасность | |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[6]
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
- (C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}
Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)
В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
Диэтиловый эфир — Википедия. Что такое Диэтиловый эфир
| Диэтиловый эфир | |
| Общие | |
|---|---|
| Систематическое наименование | 1,1-Окси-бис-этан |
| Хим. формула | C4H10O |
| Физические свойства | |
| Молярная масса | 74,12 г/моль |
| Плотность | 0,714 г/см³ |
| Энергия ионизации | 9,53 ± 0,01 эВ[1] |
| Термические свойства | |
| Т. плав. | -116,3 °C |
| Т. кип. | 34,65 °C |
| 193,4 °C | |
| Т. всп. | −49 ± 1 °F[1] |
| Пр. взрв. | 1,9 ± 0,1 об.%[1] |
| Давление пара | 440 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 60-29-7 |
| PubChem | 3283 |
| Рег. номер EINECS | 200-467-2 |
| SMILES | |
| InChI | |
| RTECS | KI5775000 |
| ChEBI | 35702 |
| Номер ООН | 1155 |
| ChemSpider | 3168 |
| Безопасность | |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[6]
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
- (C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}
Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)
В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
| Диэтиловый эфир | |||
|---|---|---|---|
| |||
| Систематическое наименование | Этоксиэтан | ||
| Хим. формула | C4H10O | ||
| Состояние | жидкость | ||
| Молярная масса | 74,12 г/моль | ||
| Плотность | 0,714 г/см³ | ||
| Энергия ионизации | 9,53 ± 0,01 эВ[1] | ||
| Температура | |||
| • плавления | -116,3 °C | ||
| • кипения | 34,65 °C | ||
| • разложения | 193,4 °C | ||
| • вспышки | −49 ± 1 °F[1] | ||
| Пределы взрываемости | 1,9 ± 0,1 об.%[1] | ||
| Давление пара | 440 ± 1 мм рт.ст.[1] | ||
| Растворимость | |||
| • в воде | (для 20 °С) 6,5 г/100 мл | ||
| Рег. номер CAS | 60-29-7 | ||
| PubChem | 3283 | ||
| Рег. номер EINECS | 200-467-2 | ||
| SMILES | |||
| InChI | |||
| RTECS | KI5775000 | ||
| ChEBI | 35702 | ||
| Номер ООН | 1155 | ||
| ChemSpider | |||
Эфир диэтиловый - это... Что такое Эфир диэтиловый?
Эфи́р диэти́ловый (лат. Aether medicinalis, Аеther pro narcosi, англ. Diethyl ether, код CAS 60-29-7, брутто-формула C4H10O) — лекарственное средство общеанестезирующего действия.
Применяют в хирургической практике для ингаляционного наркоза и в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
Физические свойства
Бесцветная, прозрачная, весьма подвижная, летучая, легковоспламеняющаяся жидкость со своеобразным запахом и жгучим вкусом. Эфир для наркоза содержит 96—98 % диэтилового эфира. Плотность эфира для наркоза 0,713—0,714; эфира медицинского 0,714—0,717; температура кипения 34—35°C и 34—36°C соответственно. При испарении 1 мл эфира для наркоза образуется 230 мл пара, имеющего плотность 2,6 и относительную молекулярную массу 74. Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути. Растворимость в воде 1:12. Смешивается со спиртом, бензолом, эфирными и жирными маслами во всех соотношениях. Легко воспламеняется (воспламенение иногда возможно даже при контакте со спиралью закрытых электронагревателей), пары эфира в определенном соотношении с кислородом, воздухом и закисью азота взрывоопасны.[3]
Фармакологическое действие
Средство для ингаляционной общей анестезии, оказывает анальгезирующее и миорелаксирующее действие, обладает большой широтой терапевтического действия. Общая анестезия при применении эфира относительно безопасна, легко управляема. Скелетная мускулатура хорошо расслабляется. Оказывает прямое отрицательное инотропное действие (снижение сократимости миокарда компенсируется повышением концентрации катехоламинов в крови). Вызывает временное (до 24 ч) снижение функции печени и почек, снижает перистальтику кишечника (стимуляция симпатоадреналовой системы), уменьшает ОЦК и плазмы (примерно на 10%). В отличие от фторотана, трихлорэтилена и циклопропана эфир не повышает чувствительность миокарда к эпинефрину и норэпинефрину.
Период вводной анестезии продолжителен (12-20 мин). Пробуждение наступает через 20-40 мин после прекращения подачи эфира, а полностью угнетение сознания проходит через несколько часов.[1]
Фармакокинетика
При ингаляционном введении эфир всасывается в кровь и проникает в головной мозг. Относительно низкая растворимость эфира в крови обусловливает постепенное нарастание его концентрации в альвеолах в начальной стадии анестезии и постепенное снижение при прекращении его поступления в организм. Почти весь эфир выводится из организма в неизмененном виде через дыхательные пути (незначительная часть выводится почками). Запах эфира в выдыхаемом воздухе может сохраняться в течение более 24 ч.[1]
Применение
- Показания
Ингаляционная общая анестезия по открытой (капельно), полуоткрытой, полузакрытой и закрытой системам (в основном при кратковременных хирургических вмешательствах).
Поддержание общей анестезии при проведении комбинированной общей анестезии с применением психоактивных ЛС и периферических миорелаксантов.
- Противопоказания
Гиперчувствительность, острые заболевания дыхательных путей, внутричерепная гипертензия, артериальная гипертензия; ХСН, печеночная и/или почечная недостаточность, кахексия, сахарный диабет, ацидоз.
Необходимость проведения в ходе хирургического вмешательства электрокоагуляции или использования электроножа.
- Побочное действие
Кашель, психомоторное возбуждение, повышение АД, тахикардия, гиперсекреция бронхиальных желез; тошнота и рвота.
В послеоперационном периоде - рвота, угнетение дыхательного центра; бронхопневмония, бронхит, ларингит, трахеит, отек легких (токсического генеза), парез кишечника, снижение секреции желчи, метаболический ацидоз, снижение клубочковой фильтрации и диуреза.[1]
Режим дозирования
При полуоткрытой системе: 2-4 об.% эфира во вдыхаемой смеси поддерживают анальгезию и выключение сознания, 5-8% - поверхностная общая анестезия, 10-12% - глубокая общая анестезия. Для усыпления больного могут потребоваться концентрации до 20-25%.
- Передозировка
Симптомы: при острой ингаляционной интоксикации - головная боль, тошнота, боль в пояснице, возбуждение, неадекватное поведение; затем - астения, сонливость, потеря сознания. Дыхание редкое и поверхностное, цианоз, акроцианоз, тахикардия, нитевидный пульс, выраженный мидриаз, снижение АД, остановка сердца.
При хронической интоксикации - снижение аппетита, тошнота (редко рвота), запоры, апатия, бледность кожных покровов, головная боль, головокружение, непереносимость этанола.
Лечение. Немедленное прекращение подачи эфира, удаление пострадавшего из зоны действия токсичного соединения на свежий воздух или в хорошо проветриваемое помещение. Ингаляции увлажнённого кислорода, щелочные масляные ингаляции, при упорном кашле - этилморфин, кодеин. В/в вводят 20-30 мл 40% раствора декстрозы с 5 мл 5% раствора аскорбиновой кислоты, аналептики, при необходимости - седативные ЛС. При угнетении дыхания - ИВЛ (нужно учитывать возможность развития токсического отека легких), при остановке сердца - непрямой массаж сердца.
При случайном попадании эфира в ЖКТ - вызывать рвоту, промыть желудок (8-10 л воды или 2% раствора натрия гидрокарбоната), дать выпить мелкоистолченный активированный уголь (2-3 ст.ложки), после чего вызвать повторную рвоту, а через 10-15 мин дать солевое слабительное. В дальнейшем - симптоматическое лечение.
- Взаимодействие
Усиливает действие недеполяризующих миорелаксантов, анксиолитиков, антипсихотических, седативных и снотворных ЛС.
Минимальная альвеолярная концентрация снижается при одновременном применении динитроген оксида.[1]
Особые указания
Эфир для наркоза должен применяться только персоналом, обученным для проведения общей анестезии.
Ингаляционная эфирная общая анестезия должна не проводиться глубже III (1-2) уровня хирургической стадии.
При подаче больших концентраций эфира (10-25%) в период вводной общей анестезии вследствие раздражающего влияния могут появиться раздражение слизистых оболочек дыхательных путей, ларингоспазм и слюнотечение (в настоящее время вводную эфирную анестезию применяют редко).
Для уменьшения вызываемых рефлекторных реакций и снижения гиперсекреции предварительно вводят атропин.
Пары эфира легко воспламеняются; с кислородом, воздухом, динитроген оксидом образуют в определенных концентрациях взрывоопасные смеси.
Предельно допустимая концентрация паров эфира в воздухе рабочей зоны равна 300 мг/куб.м.
При проведении общей эфирной анестезии по закрытой системе необходимо соблюдать меры, предупреждающие возможность взрыва.
С целью уменьшения возбуждения эфирную общую анестезию часто применяют после вводной анестезии барбитуратами. Иногда начинают введение в анестезию с помощью динитроген оксида, а эфир используют для поддержания общей анестезии.
Применение миорелаксантов позволяет усилить расслабление мускулатуры и значительно уменьшить количество необходимого для анестезии эфира - до 2-4 об.% (для поддержания общей анестезии при полуоткрытой системе).
Миорелаксирующее действие эфира не устраняется антихолинэстеразными ЛС.
Для общей анестезии можно применять эфир только из склянок, открытых непосредственно перед операцией (при воздействии света, воздуха, повышенной температуры и влаги в эфире образуются вредные продукты - перекиси, альдегиды, кетоны, вызывающие сильное раздражение дыхательных путей).
Частое вдыхание паров эфира вызывает лекарственную зависимость.[1]
Формы выпуска
Одной из разновидностей эфира для наркоза является стабилизированный эфир (лат. Аеthеr pro nаrсоsi stаbilisatum). Добавление стабилизатора (антиоксиданта) удлиняет срок годности препарата. Выпускается в герметично укупоренных склянках оранжевого стекла по 100 и 150 мл с подложенной под пробку металлической фольгой. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям Государственной фармакопеи.
Помимо эфира для наркоза выпускается также медицинский эфир (лат. Аеthеr medicinalis). Этот препарат менее очищен, чем предыдущий, и для наркоза непригоден. Применяют местно в стоматологической практике, наружно (для растираний), а также для приготовления настоек, экстрактов. Иногда назначают внутрь при рвоте. Высшие дозы для взрослых внутрь: разовая — 0,33 мл (20 капель), суточная — 1 мл (60 капель).
- Хранение
Список Б. Хранить в защищённом от света, прохладном месте, вдали от источников огня.
Примечания
Серный эфир: формула, свойства и применение
В современной мире нужно постоянно развиваться, узнавать что-то новое, нельзя стоять на месте. Однако, по непонятным причинам, под развитием многие понимают только лишь погоню за моделями айфонов, освоение появляющихся и уже существующих социальных сетей, просмотр видеороликов (в большинстве случаев абсолютно бесполезных) или же изучение лишь определенной тематики. Едва ли многие не химики могут сказать, что такое серный эфир. Или рассказать о его свойствах. А кто знает, где применяется это вещество? Почему серный эфир называется именно так? К сожалению, ответить на все эти вопросы могут лишь единицы. Что же такое эфир в принципе? Какова формула, свойства и применение серного эфира?
Классы соединений под названием "Эфир"
Изначально все классы соединений, относящиеся к эфирам, так и назывались – эфиры, не было разделения на три группы, которые существуют на сегодняшний день:
- Простые эфиры - это класс соединений, в которых между двух углеводородных радикалов находится кислород, то есть, оба радикала имеют по связи с одним и тем же кислородом. Наиболее известным представителем этого класса является этиловый эфир.
- Сложные эфиры - так называют производные карбоновых и минеральных кислот (так называемых оксикислот), у которых в молекуле вместо гидроксильной группы (-ОН) кислой функции находится спиртовой остаток. Безусловно, определение сложное и непонятное, общая формула таких соединений: R-C(=O)-R'. Представителями являются этилацетат, бутилбутират, бензилформиат.
- Полиэфиры - это класс высокомолекулярных соединений. Их получают в результате поликонденсации многоосновных кислот, то есть они содержат два атома и более водорода. Например, соляная кислота - HCl - одноосновная кислота, азотная - HNO3 - тоже. А вот серная - H2SO4 - и фосфорная - H3PO4 - многоосновные (серная - двухосновная, фосфорная - трех), как и их альдегиды с многоатомными спиртами (у этих спиртов две и более гидроксильных -ОН групп).

Что такое серный эфир?
Достоверно неизвестно где, когда, как и кем был впервые получен диэтиловый эфир. Причем здесь это вещество? Да просто у серного эфира несколько названий, в числе которых еще и этиловый. Этоксиэтан (еще одно название) - это простой эфир, молекула которого состоит из двух этильных групп (-С2Н5) и кислорода, с которым оба радикала (этильные группы) связаны. Доподлинно неизвестно, когда и кем был впервые получен – по этому вопросу имеется несколько точек зрения. Есть предположения, что в девятом веке Джабир ибн Хайян был первым, кто получил диэтиловый эфир. Но также возможно, что лишь в 1275 году каталанский миссионер Раймунд Луллий смог стать первопроходцем в области синтеза этоксиэтана. Относится вещество к алифатическим простым эфирам (то есть не имеет ароматических связей).

Способы получения
Название серного эфира тесно связан со способом получения, которым был освоен еще в средние века. Речь идет о перегонке этилового спирта и серной кислоты. Но название было дано этому веществу, точнее именно эфиром он назван, лишь в 1729 году. До этого момента можно встретить такое название как «сладкое купоросное масло» (раньше серную кислоту называли купоросным маслом).
Однако это не единственный метод синтеза диэтилового эфира. Его можно получить в качестве побочного продукта в результате гидратации этилена в среде серной или фосфорной кислот. Основная часть диэтилового эфира образуется на стадии гидролиза сульфатов. Химическая формула серного эфира выглядит следующим образом: (С2Н5)2О. Систематическое название (по международной системе СИ) - 1,1-окси-бис-этан. Брутто-формула вещества - С4Н10О.
Физические свойства
Серный эфир является легколетучей жидкостью, которая очень подвижна. Он не имеет цвета, полностью прозрачен. У этой жидкости достаточно специфический запах и очень жгучий вкус. Диэтиловый эфир разлагается под воздействием света, влаги, воздуха. При нагревании он также разлагается, как и от вышеперечисленных факторов. В результате его разложения образуются достаточно токсичные вещества, которые оказывают раздражающее действие на дыхательные пути.
Этиловый эфир относится к легковоспламеняющимся жидкостям, его пары образуют с воздухом и кислородом взрывоопасные смеси. При взаимодействии с водой образует азеотропную смесь.

Серный эфир: свойства химические
Для диэтилового эфира, как представителя класса простых эфиров, характерны свойства этого класса соединений. В результате разложения образует альдегиды, пероксиды, кетоны. При взаимодействии с сильными кислотами образует оксониевые соли, которые являются весьма нестойкими соединениями. С кислотами Льюиса (химические соединения, которые являются акцепторами электронной пары), напротив, образует достаточно стабильные соединения. Смешивается с этиловым спиртом, бензолом в любых соотношениях.

Применение этоксиэтана
Существует две основные области применения этилового эфира: медицина (фармакология) и техника. С точки зрения действия на организм человека, диэтиловый эфир является общеанестезирующим веществом, то есть используется в качестве наркоза, обезболивающего. Во время проведения подготовительных операций для пломбирования (стоматологическая практика) используется местно "дырочек" в зубах от кариеса и корневого канала. Хирурги же применяют этоксиэтан в качестве ингаляционного наркоза: пациент вдыхает пары эфира, в результате воздействия которого центральная нервная система «обездвиживается». Такой эффект полностью проходит.
Нашел применение серный эфир и в качестве растворителя. Речь идет уже о технической области применения. Также может применяться в качестве теплоносителя, гораздо реже выступает в роли хладагента. В авиамодельных двигателях компрессионного типа используется как один из компонентов топлива.

Алкилсерные кислоты (сложные эфиры серной кислоты)
Алкилсерные кислоты являются одними из важнейших представителей сложных эфиров неорганических кислот (минеральных), которые имеют немаловажное значение в области синтеза органических соединений. Сложный эфир серной кислоты, формула общая этих соединений, представители наиболее значимые являются интересной темой для обсуждения. Итак, общая формула алкилсерных кислот выглядит следующим образом: R-CH2-O-SO2-OH. Эти вещества достаточно просто получить - они легко образуются при взаимодействии серной кислоты со спиртами. В ходе реакции также выделяется вода. Наиболее важными представителями этого класса соединений являются эфиры метилового (метилсерная кислота) и этилового (этилсерная кислота) спиртов.

Выводы
Итак, серный эфир - это алифатический простой эфир, который представляет собой прозрачную, бесцветную жидкость со своеобразным запахом и жгучим вкусом. Получается из спирта этилового при воздействии на него кислот (в частности серной). Применяется в медицине и технике.
Диэтиловый эфир - это... Что такое Диэтиловый эфир?
Диэтиловый эфир (этиловый эфир, серный эфир). По химическим свойствам — типичный алифатический простой эфир.
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается со спиртом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
Синтез
Впервые получен в XIII веке алхимиком Луллием.
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например перегонкой смеси этилового спирта и H2SO4 при температуре порядка 140—150 °C.
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия и применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре — 55 °F
В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.:Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чем не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М., 1979, с. 332-40;
- Грефе Ю.,Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.