Что такое изопропанол
Изопропанол — Википедия
| Изопропанол | |||
|---|---|---|---|
| |||
| Систематическое наименование | Пропан-2-ол | ||
| Традиционные названия | Изопропиловый спирт | ||
| Хим. формула | C3H8O | ||
| Рац. формула | CH3CH(OH)CH3 | ||
| Состояние | жидкость | ||
| Молярная масса | 60,09 г/моль | ||
| Плотность | 0,7851 г/см³ | ||
| Динамическая вязкость | 0,00243 Па·с | ||
| Энергия ионизации | 10,1 ± 0,1 эВ[1] | ||
| Температура | |||
| • плавления | -89,5 °C | ||
| • кипения | 82,4 °C | ||
| • вспышки | 11,7 °C | ||
| • самовоспламенения | 400 °C | ||
| Пределы взрываемости | 2 ± 1 об.%[1] | ||
| Мол. теплоёмк. | 155,2 Дж/(моль·К) | ||
| Давление пара | 4,4 кПа при 20 °C | ||
| Константа диссоциации кислоты pKa{\displaystyle pK_{a}} | 16,5 | ||
| Растворимость | |||
| • в бензоле | хорошо растворим | ||
| • в ацетоне | растворим | ||
| Показатель преломления | 1,3776 (nD, 20°C) | ||
| Дипольный момент | 1,66 Д | ||
| Рег. номер CAS | 67-63-0 | ||
| PubChem | 3776 | ||
| Рег. номер EINECS | 200-661-7 | ||
| SMILES | |||
| InChI | |||
| RTECS | NT8050000 | ||
| ChEBI | 17824 | ||
| Номер ООН | 1219 | ||
| ChemSpider | 3644 | ||
| ЛД50 | 12800 мг/кг (кролик) | ||
| Токсичность | Класс опасности 3 | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Изопропанол ('Изопропи́ловый спирт, пропано́л-2, втор-пропанол, диметилкарбино́л, ИПС, Ch4CH(OH)Ch4{\displaystyle {\mathsf {CH_{3}CH(OH)CH_{3}}}}) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1 с неразветвлённой углеродной цепью.
При нормальных условиях изопропанол — прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью[2]. Хорошо растворяет многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. Растворяет некоторые виды пластмасс и резины.
Показатель преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Смеси паров изопропанола с воздухом образуют взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[3]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры, с щелочными металлами образует алкоголяты. Гидроксильная группа способна замещаться на атом галогена. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон[4]. Реагирует с сильными окислителями, образуя ацетон.
Изопропанол получают методами гидрирования ацетона и гидратации пропилена[5][6].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена:
- Ch4CH=Ch3+h3O→h3SO4(Ch4)2CHOH{\displaystyle {\mathsf {CH_{3}CH{\text{=}}CH_{2}+H_{2}O{\xrightarrow[{}]{H_{2}SO_{4}}}(CH_{3})_{2}CHOH}}}
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (CH3)2CHOSO2OH, серной кислоты и воды. На второй стадии процесса сернокислотный экстракт нагревается с водой, и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора: ортофосфорной кислоты на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[4].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle {\mathsf {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}}}}
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора[7][8].
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности[9].
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание[10].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[11].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием. Также используется при обслуживании оргтехники, в частности для очистки поверхностей фотобарабанов лазерных принтеров.
Медицина[править | править код]
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
- Ингаляционное
В больших количествах изопропиловый спирт ядовит (считается, что в 6 раз более этанола), требует осторожного обращения.
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[12].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Как и все летучие спирты, огнеопасен. Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[13].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства[править | править код]
Изопропиловый спирт обладает наркотическим действием[12], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[14]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть[13].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — doi:10.3109/15563650.2014.914527.
- ↑ Ссылка один (англ.),Ссылка два
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke, Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ ООО Синтез Ацетон (неопр.) (недоступная ссылка). Дата обращения 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ Papa, A. J. "Propanols" // Ullmann's Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ "Guide to Local Production: WHO-recommended Handrub Formulations" (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer's Ear) (неопр.) (26 февраля 2010). Дата обращения 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (неопр.) (недоступная ссылка). Дата обращения 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
Изопропанол или Изопропиловый спирт | Журнал Ярмарки Мастеров
Изопропанол или Изопропиловый спирт, для техники Alcohol ink.
C3-H8-O
Многие даже и не слышали о таком замечательном продукте, как изопропиловый спирт.
А ведь именно он является одним из главных ингридиентов в таких сферах, как :
- Парфюмерия
- Косметика
- Бытовая химия
- Омывающая жидкость для авто
- Медицинская сфера
- Очистка и обезжириватель оргтехники
- Растворитель органических веществ в промышленности
В каждой сфере используется своя концентрация этого продукта. От 0.01% до 99.9 %.
В России есть несколько заводов производящих изопропанол, и он скажу я вам отличного качества, потому как с ним трудно напортачить, он очень неприхотливый.
Главное на что стоит обращать внимание, что бы спирт был не химически чистым, а АБСОЛЮТИРОВАННЫМ!!! Это главнее даже самой марки.
В Азербайджане так же выпускает довольно хороший спирт, который так же можно использовать во всех сферах.
Единственным существенным минусом является сильный токсичный запах, вышеперечисленных производителей.
Но в технике Alcohol Ink, спиртовые чернила или алкогольные (много названий техника одна), человек вдыхает эти пары и при долгой работе, в случае если помещение не проветривается, могут начаться головные боли.
Отчаиваться не стоит, ибо есть еще один производитель, на которого я бы обратила внимание, это Shell. Об этой фирме можно написать целую лекцию, как минимум о том, что в самом начале своего существования, фирма торговала антиквариатом и раковинами для ванн, если интересно пишите, я расскажу.
Так вот изопропиловый спирт этой марки обладает наивысшей степенью очистки, что делает его запах не таким таксичным.
Именно поэтому, многие магазины продающие алкогольные чернила, продают Shell, это забота о своих клиентах, вы получаете не только высокую очистку спирта, но и трезвую голову!
P.S. Пары изопропилового спирта не накапливаются в организме. И если вы захотите сесть за руль после вашего творчеста, можете не переживать, промили не набегут.
P.S.p.s Пары изопропилового спирта не являются токсичными, в полной мере этого слова.
39) Изопропанол — выводим воду из топливного бака — Ford Focus Hatchback, 1.6 л., 2013 года на DRIVE2
Озадачился Я как-то поисками ИЗОПРОПАНОЛА (Изопропилового спирта) для своих нужд в области радиотехники.

ИЗОПРОПАНОЛ
Зная, что Изопропанол (изопропиловый спирт) обладает очень хорошими обезжиривающими и очищающими свойствами, решил немного углубиться в физ. и хим. свойства данного вещества.
Хим.формула изопропанола
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом. Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности.
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание.
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита.
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Из всего прочитанного, для себя сделал такие выводы, что изопропанол:
— практически не оказывает вредного влияния ни на резину, ни на пластик, ни на другие орг.соединения ;
— очень хорошо впитывает воду…

Как вы знаете, а если даже и не знаете, то должны понимать, что со временем в бензобаке автомобиля накапливается вода. Путей её попадания туда несколько. Это и конденсат, и наличие в бензине, и даже на автомойке, после струи Керхера… Вода тяжелее бензина, следовательно, она оседает на дно. Пока на улице тепло, всё нормально…но стоит ударить лютым морозам, как вода тут же замерзнет и может попросту заблокировать работу топливной системы… Поэтому с водой в бензобаке надо бороться… Её надо выводить оттуда, но это не так просто, так как вода не смешивается с бензином… Так вот на помощь приходят знания химии — воду хорошо растворяют в себе (то есть смешиваются) спирты — после чего они сгорают как бензин.
Так вот, едва ли не лучшими свойствами по впитыванию воды обладает именно изопропиловый спирт (даже лучше, чем этиловый (пищевой, медицинский).

Себе приобрел литровую бутылку. Кстати, в магазинах (строймаг, малярных) этот продукт не нашёл. Заказывал на сайте, торгующем подобной пром.химией.
Пол литра оставил, опять же, для радиотехнических нужд.
Остальные 0.5L залил в пустой бензобак перед полной заправкой для лучшей смешиваемости.

Теперь я спокоен, это была первая обработка за почти 5 лет — ещё на несколько лет !
Особенно актуально для авто, эксплуатирующихся в северных регионах с отрицательными температурами.
Спасибо за внимание!
Изопропиловый спирт: применение, состав, свойства
Изопропиловый спирт — химическое вещество с формулой Ch4CH(OH)Ch4. Его часто называют еще пропанол-2, изопропанол или сокращенно ИПС. У нас продается изопропиловый спирт, поэтому представляем посетителям интернет-магазина небольшой рассказ о нем.
Свойства изопропилового спирта
Изопропанол — вторичный спирт алифатического ряда. Способен образовывать различные эфиры, вступает в реакцию с активными металлами, при конденсации с ароматическими соединениями получают производные, например, изопропилбензол.
Отличный растворитель и сам растворяется в бензоле и ацетоне, а с водой и органическими растворителями смешивается в любых пропорциях.
Изопропанол хорошо растворяет натуральные и некоторые синтетические смолы, этилцеллюлозу, поливинил бутирал, большинство масел. Не подходит для работы с резинами и некоторыми пластиками. С водой образует азеотропную смесь, на 87,9% состоящую из пропанола-2. С растворами солей в химические реакции не вступает, что используется для выделения его из водного раствора.
 Изопропиловый спирт представляет собой жидкость без цвета, с резким спиртовым запахом, более «грубым», чем запах этилового спирта. Температура замерзания: 89,5 °С ниже нуля. Пары вещества легко смешиваются с воздухом и при большой концентрации образуют взрывоопасную смесь, поэтому работать с ним следует в хорошо проветриваемых помещениях и держать его подальше от открытого огня и нагревательных приборов.
Изопропиловый спирт представляет собой жидкость без цвета, с резким спиртовым запахом, более «грубым», чем запах этилового спирта. Температура замерзания: 89,5 °С ниже нуля. Пары вещества легко смешиваются с воздухом и при большой концентрации образуют взрывоопасную смесь, поэтому работать с ним следует в хорошо проветриваемых помещениях и держать его подальше от открытого огня и нагревательных приборов.
Изопропанол токсичен при вдыхании и употреблении внутрь, может вызывать раздражение кожи, отравления, вплоть до смертельного исхода. Пары обладают наркотическим воздействием. Изопропиловый спирт токсичнее этилового, но и опьяняет в десятки раз быстрее, поэтому человек оказывается просто не в состоянии принять смертельную дозу. Гораздо опаснее длительное вдыхание паров с содержанием в воздухе свыше ПДК.
Применение изопропилового спирта
Основная его сфера применения — в качестве растворителя в промышленности, в парфюмерии, в бытовой химии, в репеллентах. Цена изопропилового спирта доступная, что вкупе со множеством полезных свойств делает его востребованным веществом. Его применяют:
— В автомобильной промышленности. Особенно ценится свойство ИПС замерзать при очень низких температурах. Чем выше концентрация в растворе изопропанола, тем ниже температура замерзания жидкости. Его используют в антифризах, стеклоочистителях, добавляют в бензин.
— В медицине — в качестве дезинфицирующего средства (60-70% раствором пропитывают тампоны и салфетки, очищают руки).
— Как промежуточное звено при получении других реактивов в химии. Из изопропанола в промышленных масштабах получают ацетон, изопропилбензол.
— В фармакологии используют при анализах с помощью газовой хроматографии.
— Для консервации органических материалов (альтернатива формальдегиду), для сохранения анализов в медицине и биологии.
— Изопропиловый спирт в качестве очистителя применяется в электротехнике, электронике, металлургии, в мебельном и оптоволоконном производстве и т. д.
— В быту. Пропанол-2 менее токсичен, чем большинство используемых в хозяйстве растворителей. С его помощью ударяют пятна, клей, масла, краску, грязь с тканей, бумаги, деревянных, металлических и стеклянных поверхностей.
Изопропиловый спирт и изопропанол одно и тоже
| Изопропанол | |
|---|---|
 | |
| Общие | |
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ [1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.% [1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 ( nD , 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| RTECS | NT8050000 |
| ChEBI | 17824 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, сокр. ИПС — широко используемое сокращение) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует 1 изомер изопропанола — пропанол-1, обладающий прямой цепью.
При нормальных условиях прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью [2] .
Как и все летучие спирты, огнеопасен. Токсичен (считается, что в 6 раз более этанола), требует осторожного обращения.
Содержание
Свойства [ править | править код ]
Химические свойства [ править | править код ]
Рациональная химическая формула изопропилового спирта CH 3 CH ( OH ) CH 3 <displaystyle <ce >> и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон [3] .
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства [ править | править код ]
Бесцветная жидкость с характерным спиртовым запахом, более резким и неприятным, чем у этанола, их можно отличить по запаху.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К) . Удельная теплота сгорания 34,1 МДж/кг .
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение [4] :
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
Получение [ править | править код ]
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена [5] [6] .
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>>"> CH 3 CH = CH 2 + H 2 SO 4 ⟶ ( CH 3 ) 2 CHOSO 2 OH + H 2 O ⟶ ( CH 3 ) 2 CHOH <displaystyle <ce (Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>> (Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>>"/> .
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата ( CH 3 ) 2 CHOSO 2 OH <displaystyle <ce <(Ch4)2CHOSO2OH>>> , серной кислоты H 2 SO 4 <displaystyle <ce
>> и воды H 2 O <displaystyle <ce >> . На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты H 3 PO 4 <displaystyle <<ce >>> на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами [3] .
Современный способ гидрирования ацетона водородом:
C H 3 C O C H 3 + H 2 → k a t C H 3 C H ( O H ) C H 3 <displaystyle mathrm COCH_<3>+H_<2><xrightarrow >CH_<3>CH(OH)CH_<3>> > 3>
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора [7] [8] .
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск) [9] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск) [8] [10] .
Применение [ править | править код ]
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности [11] .
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание [12] .
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита [13] .
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина [ править | править код ]
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека [ править | править код ]
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает [14] .
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей [15] .
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко [2] .
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов [2] .
Наркотические свойства [ править | править код ]
Изопропиловый спирт обладает наркотическим действием [14] , наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола [16] . Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть [15] .
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
- 67-63-0Y
- CHEBI: 17824Y
- ChEMBL582Y
- 3644Y
- D00137Y
- ND2M416302Y
1,96 гр Р при 25 ° С
1,77 гр Р при 30 ° C
Внешний MSDS
закрытый тигль: 13 ° C (55 ° F)
3600 мг / кг (перорально, мышь)
5045 мг / кг (перорально, крыса)
6410 мг / кг (перорально, кролик)
12000 частей на миллион (крыса, 8 ч)
12800 частей на миллион (мышь, 3 ч)
Диэлектрическая постоянная (ε г ) и т.д.
твердое тело-жидкость-газ
Изопропиловый спирт ( ИЮПАК название пропан-2-ол ; обычно называют изопропанол или 2-пропанол) представляет собой соединение с химической формулой CH 3 CHOHCH 3 . Это бесцветное , воспламеняется химическое соединение с сильным запахом . В качестве изопропиловых групп , связанных с гидроксильной группой, это самый простым пример вторичного спирта , где спирт атом углерода присоединен к двум другим атомам углерода. Это структурный изомер из 1-пропанола и этилового эфира .
Он используется при изготовлении самых разнообразных промышленных и бытовых химических веществ, а также является общим компонентом химических веществ , таких как антисептики , дезинфицирующие и моющие средства.
содержание
имена
Изопропиловый спирт также известен как 2-пропанол, Sec -пропила спирта, IPA, или изопропанол. ИЮПАК считает изопропанол неверное имя в качестве углеводородного изопропан не существует.
свойства
Изопропиловый спирт смешивается в воде, этаноле , эфире и хлороформе . Оно растворяет этилцеллюлозу , поливинилбутираль , многие масла, алкалоиды, камедь и природные смолы. В отличие от этанола или метанола , изопропилового спирта не смешивается с растворами солей и могут быть отделены от водных растворов путем добавления соли , такие как хлорид натрия . Процесс просторечия называется высаливанием , и причины концентрируют изопропиловый спирт , чтобы отделить в отдельный слой.
Изопропиловый спирт образует азеотропную смесь с водой, которая дает температуру кипения 80,37 ° C (176,67 ° F) и композицией 87,7 мас% (91% по объему) изопропилового спирта. Водно-изопропил смеси спиртов привели к снижению точки плавления. Она имеет слегка горьковатый вкус, и это не безопасно пить.
Изопропиловый спирт становится все более вязким при понижении температуры и замерзает при -89 ° С (-128 ° F).
Изопропиловый спирт имеет максимальную оптическую плотность при 205 нм в качестве ультрафиолетовой и видимой области спектра.
Реакции
Изопропиловый спирт может быть окислен до ацетона , который является соответствующим кетоном . Это может быть достигнуто с помощью окислительных агентов , таких как хромовая кислота , или путем дегидрирования изопропилового спирта над медным нагретым катализатором :
Изопропиловый спирт часто используется в качестве как растворитель и гидрид источника в сокращении Меервейно-Ponndorf-Верлея и другие передачи гидрогенизации реакций. Изопропиловый спирт может быть превращен в 2-бромпропан с помощью трибромида фосфора , или дегидратирует до пропена при нагревании с серной кислотой .
Как и большинство спиртов, изопропиловый спирт реагирует с активными металлами , такими как калий с образованием алкоголятов , которые можно назвать isopropoxides . Реакция с алюминием (инициирована следом ртути ) используется для приготовления катализатора изопропоксида алюминия .
история
В 1920 году Standard Oil сначала получают изопропиловый спирт гидратацией пропена . Его используют главным образом в то время не было тереть спирт , а для окисления в ацетон , чей первой главной польза была в первой мировой войне для подготовки кордита , бездымного, низкий взрывной пропеллент.
производство
В 1994 году 1,5 миллиона тонн изопропилового спирта были произведены в Соединенных Штатах, Европе и Японии. Это в первую очередь получают путем объединения воды и пропена в реакции гидратации или путем гидрирования ацетона . Есть два маршрута для процесса гидратации и оба процесса требуют, чтобы изопропиловый спирт быть отделен от воды и других побочных продуктов путем перегонки . Изопропиловый спирт и вода образуют азеотроп и простая перегонка дает материал , который является 87,9% по массе изопропилового спирта и 12,1% по весу воды. Чистый ( безводный ) изопропиловый спирт производится путем азеотропной перегонки влажного изопропилового спирта с использованием либо диизопропиловый эфира или циклогексана в качестве азеотропных агентов.
Косвенная гидратация
Косвенная гидратация пропена реагирует с серной кислотой с образованием смеси сульфатов эфиров. Этот процесс может использовать низкокачественный пропен, и преобладает в США. Эти процессы дают прежде всего изопропиловый спирт , а не 1-пропанола, так как добавление воды или серной кислоты к пропена следует правилу Марковникова . После гидролиза этих сложных эфиров пара производит изопропиловый спирт, путем перегонки. Диизопропиловый эфир является значительным побочным продуктом этого процесса; он возвращается обратно в процесс и гидролизуют с получением желаемого продукта.
Прямая гидратация
Прямая гидратация реагирует пропна и воду, либо в газовой фазе или в жидкой фазе, при высоких давлениях в присутствии твердых или поддерживаемых кислотных катализаторов . Этот тип процесса обычно требует пропилена более высокой чистоты (> 90%). Прямая гидратация чаще используется в Европе.
Гидрирование ацетона
Сырой ацетон гидрирует в жидкой фазе над никелем Ренея или смесь из меди и оксида хрома с получением изопропилового спирта. Этот процесс полезен, когда она соединена с избытком производства ацетона, таких как процесс кумола .
Пользы
растворитель
Изопропиловый спирт растворяет широкий спектр неполярных соединений. Кроме того , быстро испаряется, уходит почти нулевой следы масла, по сравнению с этанолом, и является относительно нетоксичным, по сравнению с альтернативными растворителями. Таким образом, он широко используется в качестве растворителя и в качестве моющей жидкости, особенно для растворения масла. Вместе с этанол, н-бутанол, и метанол, он принадлежит к группе растворителей, спиртов около 6,4 млн т из которых были использованы во всем мире в 2011 году.
Примеры такого применения включают в себя чистящие очки , электронные устройства , такие как контактные штифты (например , те , на ROM картриджей ), магнитной ленте и дисковых головок (таких , как те , в аудио- и видеомагнитофонов и гибких дисков дисков), Линзы лазеров в оптическом диске диски (например, компакт – диск , DVD ) и удаление термопасты с радиаторов и IC пакетов (например, ЦП ).
промежуточный
Изопропиловый спирт этерифицируют с получением изопропилацетата , другой растворитель. Он вступает в реакцию с сероуглеродом и гидроксидом натрия , чтобы дать isopropylxanthate натрия , в гербицид и флотации руды реагент. Изопропиловый спирт реагирует с тетрахлоридом титана и алюминия металла с получением титана и алюминия isopropoxides , соответственно, бывший катализатор, и последний химический реагент. Это соединение может служить в качестве химического реагента в себе, действуя в качестве донора в дигидрофосфате гидрирования с переносом .
медицинская
Спирт затирания , дезинфицирующее средство для рук , и дезинфицирующие колодки обычно содержат 60-70% раствор изопропилового спирта в воде . Вода требуется , чтобы открыть поры мембраны бактерий, который действует в качестве шлюза для изопропилового спирта. 75% об / об растворе в воде может быть использован в качестве дезинфицирующего средства для рук. Изопропиловый спирт используется в качестве вспомогательного средства в воде сушки для профилактики наружного отита , более известной как ухо пловца.
Раннее использует в качестве анестетика
Несмотря на то, изопропиловый спирт может быть использован для анестезии, многие его негативные атрибуты или недостатки запретить это использование. Изопропиловый спирт также может быть использован так же, как эфир в качестве растворителя или в качестве анестезирующего средства путем вдыхания паров или перорально. Ранние применения включали использование в качестве растворителя для общей анестезии мелких млекопитающих и грызунов ученых и некоторых ветеринары. Тем не менее, это было вскоре прекращено, так как возникло много осложнений, в том числе раздражение дыхательных путей, внутреннего кровотечения, а также зрительные и слуховые проблемы. В редких случаях наблюдается дыхательная недостаточность приводит к смерти животных.
автомобильный
Изопропиловый спирт является основным ингредиентом в «газовой сушилки» топливных присадок . В значительных количествах воды является проблемой в топливных баках, так как она отделяется от бензина и может замерзнуть в линиях питания при низких температурах. Алкоголь не удаляет воду из бензина, но Спирт , растворяет воду в бензине. После того, как растворимая , вода не создает такой же риск , как нерастворимую воду, так как он больше не накапливается в линиях подачи и замерзает, но потребляется с самим топливом. Изопропиловый спирт часто продается в аэрозольных баллончиках в качестве ветрового стекла или дверного замок обледенения. Изопропиловый спирт также используется для удаления тормозной жидкости следы от гидравлических тормозных систем, так что тормозная жидкость (обычно DOT 3 , DOT 4 , или минеральное масло ) не загрязнять тормозные колодки и привести к ухудшению торможения.
лаборатория
В качестве биологического образца консерванта, изопропиловый спирт обеспечивает сравнительно нетоксичной альтернативу формальдегид и другие синтетические консерванты. Изопропиловый спирт растворы 70-99% используются для сохранения образцов.
Изопропиловый спирт часто используется в экстракции ДНК . Лабораторный работник добавляет его в раствор ДНК для осаждения ДНК, который затем образует осадок после центрифугирования. Это возможно потому , что ДНК является нерастворимым в изопропиловом спирте.
безопасности
Изопропиловый спирт пара является более плотной , чем воздух и воспламеняется , с диапазоном воспламеняемости от 2 до 12,7% в воздухе. Это следует держать вдали от источников тепла и открытого пламени. Перегонка изопропилового спирта в течение магния сообщалось, образуя пероксиды , которые могут взорваться от концентрации. Изопропиловый спирт является раздражителем кожи. Носить защитные перчатки рекомендуется.
токсикология
Изопропиловый спирт и его метаболита , ацетон , действуют в качестве центральной нервной системы (ЦНС) депрессантов . Отравление может произойти от приема пищи, ингаляции, или поглощения кожи. Симптомы изопропилового спирта включают отравление гиперемию , головную боль , головокружение , депрессия ЦНС , тошнота , рвота , анестезии , переохлаждение , низкое кровяное давление , шок , угнетение дыхания и кома . Передозировка может вызвать фруктовый запах на дыхании в результате его метаболизма в ацетон . Изопропиловый спирт не вызывает анион разрыв ацидоза , но он производит osmolal зазора между вычисленным и измеренным osmolalities сыворотки, как и другие спирты.
Изопропиловый спирт окисляется с образованием ацетона алкогольдегидрогеназы в печени, и имеет биологическую полураспада в организме человека от 2,5 до 8,0 часов. В отличие от метанола или этиленгликоля отравления, метаболиты изопропилового спирта являются менее токсичными, и лечение в основном поддерживает. Кроме того, нет никаких указаний на использование Fomepizole , ингибитор дегидрогеназы спирта, если совместно проглатывание смесью метанол или этиленгликоль не подозревается.
Основное различие между пропанол-2 и изопропанолом, что пропанол-2 имеет такое название в системе IUPAC (уникальное имя, присвоенное химическому веществу), химическая формула у него C3H8O. Для обоих терминов применяется общее название — изопропиловый спирт.
Оба термина обозначают одно и то же химическое соединение, которое имеет химическую формулу C3H8O. Таким образом, это спиртовое соединение, имеющее гидроксильную функциональную группу.
Содержание
- Обзор и основные отличия
- Что такое 2-пропанол
- Что такое изопропанол
- Сравнение — пропанол-2 против изопропанола
- Резюме
Что такое пропанол-2?
Пропанол-2 — это название IUPAC для соединения, имеющего химическую формулу C3H8O. Следовательно, пропанол-2 представляет собой спирт, который содержит гидроксильную группу (-OH) в качестве своей функциональной группы. Он существует в виде бесцветной жидкости при комнатной температуре, и он также легко воспламеняется. Кроме того, он также имеет сильный запах.
При рассмотрении химической структуры, он имеет три атома углерода в виде цепи, и гидроксильная группа присоединяется к среднему углероду, в то время как все остальные вакантные позиции содержат атомы водорода. Таким образом, он является вторичным спиртом и является структурным изомером 1-пропанола.
Некоторые химические и физические данные о соединении следующие:
- Молярная масса составляет 60,1 г / моль.
- Внешний вид бесцветный.
- Температура плавления составляет -89 ° С.
- Температура кипения составляет 82,6 ° С.
- Смешивается с водой, этанолом, эфиром и хлороформом.
- Становится все более вязким с понижением температуры.
Что такое изопропанол?
Изопропанол — это общее название для соединения, имеющего химическую формулу C3H8O. Название этого соединения в IUPAC — пропанол-2, и оно также распространено как изопропиловый спирт .
Он получает общее имя из своей структуры; молекула представляет собой спирт, и она имеет изопропильную группу, связанную с гидроксильной группой, что делает ее вторичным спиртом.
В чем разница между пропанолом 2 и изопропанолом?
Оба термина пропанол-2 и изопропанол описывают одно и то же химическое соединение, которое имеет химическую формулу C3H8O; только терминология отличается друг от друга. В частности, пропанол-2 является названием IUPAC для соединения, тогда как изопропанол является общим названием. Следовательно, кроме применения этого термина, нет никакой разницы между пропанол-2 и изопропанолом.
Кроме того, другим распространенным названием, которое мы используем в повседневной жизни, является изопропиловый спирт. Хотя все три термина называют одно и то же химическое соединение, они получили свои названия в соответствии с химической структурой соединения. Пропанол-2 получил свое название из-за присоединения гидроксильной группы ко 2-му углероду молекулы пропана. С другой стороны, изопропанол или изопропиловый спирт получил свое название из-за связи изопропильной группы с гидроксильной группой.
Резюме — пропанол-2 против изопропанола
Оба термина пропанол-2 и изопропанол описывают одно и то же химическое соединение. Таким образом, только терминология отличается. Следовательно, ключевое различие между пропанолом-2 и изопропанолом состоит в том, что 2-пропанол является названием IUPAC для соединения, имеющего химическую формулу C3H8O, тогда как изопропанол является общим названием для того же соединения.
“>
применение спирта, гост 9805 84, формула
Изопропиловый спирт (изопропанол) – это органическое соединение, относящееся к классу спиртов. В соответствии с особенностями применения он является техническим спиртом. Изопропиловый спирт имеет формулу Ch4CH(OH)Ch4. Его еще называют медицинский спирт.
Читайте также
Читайте также

Изопропиловый спирт
Изопропиловый спирт представляет собой прозрачную жидкость с горьковатым вкусом и сильным спиртовым запахом. Огнеопасен. Имеет низкую плотность. Обладает характерными физическими и химическими свойствами.
Физические свойства изопропанола
Вещество в жидком состоянии имеет плотность 0,79 г/см3. Такая плотность ниже, чем у воды, поэтому изопропанол более летучий, чем вода. Он начинает кипеть при 83 градусах Цельсия. При концентрации более 2,5% в определенных условиях может взрываться. Самопроизвольное воспламенение происходит при нагреве до температуры выше 450 градусов Цельсия. Сочетание паров изопропилового спирта с воздухом способно образовывать взрывоопасную взвесь.
Спирт неплохо растворяется в ацетоне, бензоле. При добавлении в смесь воды и изопропанола поваренной соли он выделяется в отдельную фракцию.
Еще одним свойством изопропанола является постепенное увеличение вязкости при охлаждении. При значениях ниже – 70 °С имеет сиропообразную консистенцию.
Наиболее сильная линия поглощения молекул изопропанола приходится на ультрафиолетовую часть спектра (204 нм).
Химические свойства изопропанола
Изопропиловый спирт легко превращается в ацетон. Это происходит при его реакции с такими окислителями, как хромовая кислота либо с использованием нагретой меди. В ходе данной реакции от спирта отщепляется молекула водорода.
Изопропанол является растворителем и может повреждать изделия из пластика и резины. При нагревании с участием серной кислоты из него может образовываться пропилен.
Подобно многим другим спиртам, изопропиловый спирт вступает в реакцию с некоторыми металлами, например, с калием.
Получение изопропилового спирта
Масштабы производства изопропанола составляют миллионы тонн в год. Для промышленного получения изопропилового спирта используют воду и пропилен (реакция гидратации). Выделяют прямую и косвенную гидратацию. Косвенная гидратация активно используется в США. Для нее используется сырье низкого качества.
Прямая гидратация, для которой используется высокоочищенный пропилен, применяется в Европе.
Под косвенной гидратацией понимают такое взаимодействие серной кислоты и пропилена, при котором образуется смесь сложных эфиров. Гидролиз данных соединений с использованием пара приводит к выделению изопропилового спирта. При этом также выделяется диизопропиловый эфир. Он является побочным компонентом и затем также используется для получения изопропилового спирта.
При прямой гидратации происходит реакция воды и пропилена с участием катализаторов. Она протекает в условиях высокого давления. Данная реакция дает более качественный спирт со степенью очистки более 90 процентов. В результате получается спирт изопропиловый абсолютированный.
Для отделения спирта от воды и других продуктов реакции используется метод дистилляции. Первоначально образуется смесь, состоящая из 88 процентов спирта и 12 процентов воды. Такой спирт называют влажным. Для получения чистого продукта используется метод азеотропной дистилляции, для чего применяется циклогексан и другие соединения.
При производстве изопропилового спирта необходимо соблюдение стандартов, регламентируемых в соответствии с ГОСТ 9805 84: спирт изопропиловый, технические условия.
Использование изопропанола
Изопропиловый спирт применяется в различных сферах человеческой деятельности. Среди них такие, как лакокрасочная промышленность, нефтепереработка, переработка древесины, химическая, парфюмерная и мебельная промышленность, автохимия.
При производстве лаков и красок он используется в качестве растворителя. В области нефтепереработки изопропиловый спирт нашел применение в качестве добавки к маслам и как растворитель.
При деревообработке его применяют для извлечения древесной смолы.
В химической и парфюмерной промышленности данное вещество используют как растворитель для эфиров и других веществ.
В сфере автохимии этот спирт нашел применение при производстве антифризов и других, требующихся для работы автомобилей, жидкостей.
Изопропиловый спирт используют в парфюмерной промышленности
Изопропиловый спирт можно обнаружить в составе парфюмерии, косметики, бытовой химии, веществ для дезинфекции. Также его используют в слесарном деле.
Большая часть изопропилового спирта реализуется в процессе производства различных видов продукции. Его часто применяют в фармацевтическом деле, что связано с низкой токсичностью примесей. Некоторая часть изопропилового спирта используется в химии при получении ацетона. Однако чаще его применяют для получения изопропилбензола. Около 5 тонн в год используется в бытовых целях и в косметике.
Еще одним направлением использования изопропанола является включение его в состав бензина в качестве добавки.
Применение изопропанола в качестве растворителя
Изопропиловый спирт легко испаряется и обладает более низкой (в сравнении с другими растворителями) токсичностью. Как растворитель он подходит для многих составов. Все это обусловило активное использование этого спирта в качестве растворяющего и чистящего средства, особенно при очистке изделий от масляных загрязнений. Изопропиловый спирт можно применять для очистки деталей в электронной технике, клавиатуры, ЖК мониторов. Может быть неплохим вариантом в качестве чистящего средства в домашнем хозяйстве. Подойдет он для таких материалов, как ткань и древесина. В то же время его нельзя использовать для очистки винила.
Применение в химической промышленности и медицине
Изопропиловый спирт является сырьем для производства изопропилацетата, который также является растворителем. Реакция изопропанола с алюминием и четыреххлористым титаном приводит к выделению титана.
Изопропанол применяют в медицине в составе тампонов для дезинфекции, которые содержат водный раствор данного соединения. Также его используют в качестве осушающего средства в целях предотвращения появления наружного отита (одного из заболеваний ушей).
Использование изопропанола в автомобилестроении
Изопропанол используют в качестве основного ингредиента в составе топлива в целях растворения водной фракции в составе бензина. Это исключает риск замерзания воды. В продаже можно встретить аэрозольные баллончики, основное назначение которых – борьба с обледенением ветрового стекла. Также его используют для очистки тормозных систем от остатков тормозной жидкости.
Применение в биологии
Изопропиловый спирт используют как консервант для органики и для хранения анализов. Для консервации можно также использовать формальдегид, но он более токсичен.
Изопропанол нередко используют при исследованиях ДНК. Дело в том, что молекула ДНК не растворяется в этом спирте. В ходе исследований изопропиловый спирт добавляется в подготовленную ДНК в целях преципитирования.
Токсикология
Изопропанол негативно воздействует на организм человека. При попадании его на кожу вызывает ее раздражение. При приеме внутрь может наблюдаться понос, головокружение, головная боль, тошнота, рвота, депрессивное состояние и даже кома.
Также могут отмечаться следующие нежелательные явления:

Желудочно-кишечные расстройства
- Желудочно-кишечные расстройства.
- Повышение кровяного давления.
- Гастрит.
- Уменьшение частоты сердечных сокращений.
Наибольшее воздействие это вещество оказывает на нервную систему. Известны также случаи таких серьезных последствий отравления, как некроз скелетной мускулатуры.
Проникновение спирта в организм может произойти вследствие вдыхания, впитывания в кожу, употребления внутрь. Опасной считается доза в 15 грамм этого спирта для взрослого человека.
Отравление посредством употребления внутрь иногда происходит у детей. При этом до летального исхода дело, как правило, не доходит. При приеме небольших количеств этого спирта наблюдается в основном диарея.
Ингаляционное отравление маловероятно, так как это вещество не слишком летучее. Поэтому для накопления молекул в воздухе помещений требуется большая площадь разлива и определенное время. При сжигании наблюдается распад изопропанола на молекулы углекислого газа и молекулы воды. При этом не выделяются нежелательные вещества, нет дыма и сажи.
Основной негативный эффект изопропанола обусловлен тем, что в организме человека он преобразуется в ацетон. Время выведения изопропилового спирта составляет от 3 до 8 часов.
Однако он менее токсичен, чем метиловый спирт. По сравнению с этанолом у него более выражен наркотический эффект. В течение определенного времени происходит опьянение. При высокой концентрации паров изопропилового спирта может наступить потеря сознания.
Изопропиловый спирт не накапливается в теле человека, поэтому хроническое отравление им маловероятно.
В целях исключения риска отравления рекомендуется руководствоваться следующими требованиями:
- хорошо проветривать помещения;
- не держать это вещество в доступном для детей месте;
- не использовать не по назначению.
Купить изопропиловый спирт можно в крупных городах, в том числе в Москве по низкой цене. При этом продажа осуществляется в небольшом количестве. Большой объем этого спирта можно приобрести по заказу в интернет-магазинах.
Вылечить алкоголизм невозможно???
- Испробовано множество способов, но ничего не помогает?
- Очередное кодирование оказалось неэффективным?
- Алкоголизм разрушает вашу семью?
Не отчаивайтесь, найдено эффективное средство он алкоголизма. Клинически доказанный эффект, наши читатели испробовали на себе ... Читать далее>>
Читайте также
Как применять изопропиловый спирт для помощи в быту- Инструкция +Видео
Изопропиловый спирт представляет собой бесцветную жидкость с резким специфическим запахом. Другое название вещества, которое часто можно встретить – изопропанол, диметикарбинол, 2-пропанол, ИПС.
Широкое применение изопропилового спирта в различных отраслях обусловлено его химическими свойствами.
Свойства ИПС
- Смешивается с водой и ругими органическими растворителями;
- Растворяет почти все смолы и масла;
- Не вступает в химические реакции с растворами солей;
- Замерзает при температуре ниже -90 градусов.
ИПС является аналогом этилового и метилового спирта, при этом отличается более безопасным составом, доступностью и низкой ценой. Он нашел свое применение в разных отраслях промышленности, косметологии и медицине, а также в быту.
Применение изопропанола
в промышленности
Наибольшее распространение в отраслях промышленности изопропиловый спирт получил благодаря тому, что способен растворять большую часть масел и смол, при этом быстро испаряется с поверхности и повреждает ее. Помимо этого, он менее токсичен, чем другие растворители.
Наличие вышеперечисленных свойств позволяет использовать его в следующих отраслях промышленности:
- Мебельная и лакокрасочная. Здесь изопропиловый спирт применяется для того, чтобы растворять клей, краску и масла;
- В электронике. Им обезжиривают и осушают различные производимые детали и соединения;
- Фармацевтика. Служит в качестве исходного сырья для большого количества фармацевтических товаров;
- Химическая промышленность. Выступает в качестве промежуточного звена при получении других растворителей и является сырьем для промышленного производства ацетона;
- Лесохимическая – извлечение смолы из древесины;
- Полиграфии и типографии – помогает увеличивать яркость цвета при печати;
- Автохимия. Изопропиловый спирт применяется при производстве незамерзающей жидкости, антифриза;
- Бытовая химия. Добавляется во влажные салфетки очищающие средства.
Косметология
Изопропанол используется в таких косметических средствах, как лаки для ногтей, средства для волос, кремы после бритья, очищающие лосьоны и маски. Применение в этой сфере обусловлено низкой токсичностью, способностью растворяться в воде и оказывать дезинфицирующее воздействие.
ВАЖНО! Косметические средства, в составе которых есть изопропанол не подходят для сухого типа кожи.
Медицина
Широкое применение изопропиловый спирт получил и в медицине. В медучереждениях он может применяться как в разбавленном виде, для дезинфекции рук перед осмотрами или операциями, или в чистом виде для пропитки перевязочных материалов, дезинфекции инструментов или мест введения медицинской иглы.
Бытовые нужды
Благодаря своей способности выступать в качестве растворителя, средства для очищения и дезинфекции, изопропиловый спирт широко применяется и в домашних условиях. Его используют е в чистом виде, а готовят раствор, для которого спирт смешивается в равных пропорциях с дистиллированной водой и переливается в емкость с распылителем.

Итак, чем может помочь раствор изопропанол в быту:
- Очищает диски, матрицы зеркальных фотоаппаратов, мониторы, компьютерные мыши и клавиатуры, экраны электроники от пыли, следов пальцев и загрязнений;
- Удаляет клей, чернила и краску с ткани, стекол и древесины;
- Используется для дезинфицирования и очистки кистей для макияжа;
- Устраняет зуд от укусов комаров и других насекомых;
- Уничтожает насекомых-вредителей;
- Дезинфекция рук;
- Альтернатива антиперсперанту – эффективно справляется с запахом пота.
Некоторые водители применяют раствор изопропилового средства в автомобиле, для обработки автостекол от замерзаний. Для этого к раствору добавляется немного бытового чистящего средства.
Места продажи
Купить изопропиловый спирт достаточно сложно. Для этого можно обратиться напрямую к производителю, но в таком случае, возможна только оптовая закупка. В аптеке это вещество просто так купить не получится, для этого потребуется рецепт от врача. Для бытовых целей можно приобрести небольшое количество специализированных магазинах, занимающихся продаже химических реактивов.
Меры предосторожности
Как и любое химическое соединение, ИПС – опасное вещество, которое требует осторожного обращения. Использовать спирт необходимо в хорошо проветриваемом помещении, так как переизбыток его паров и попадание в организм могут привести к интоксикации. Хранить ИПС необходимо вдалеке от огня и попадания прямых солнечных лучшей, в местах, недоступных для детей.
Спирт не обладает способностью впитываться в кожные покровы, но при регулярном взаимодействии может привести к химическому ожогу. Категорически запрещается допускать попадания веществ на слизистые оболочки.
Изопропиловый спирт (Пропанол-2) - что это такое? Ответ от ПСПРОФФ
Спирт изопропиловый (изопропанол, пропанол-2, диметилкарбинол) представляет собой полностью прозрачную, бесцветную жидкость с ярко выраженным неприятным запахом. Химическая формула – C3H8O. Плотность – 0,7851 г/см3. Хорошо растворяется в ацетоне и бензоле. Температура замерзания зависит от массовой доли пропанола-2 (изопропилового спирта) в смеси. При концентрации 50 % жидкость замерзает при температуре -21 оС, 100 % – наблюдается переохлаждение при -90 оС.
Окисление пропанола-2 возможно как в паровой, так и в жидкой фазе, при этом в обоих случаях оно может протекать без катализаторов, но с использованием перекиси водорода в качестве инициатора. Окисление спирта в жидкой фазе приводит к образованию перекиси водорода и ацетона. Облучение вещества ультрафиолетом приводит к образованию антрагидро-хинонового радикала. Окисление воздухом проводится с использованием металлических катализаторов. Реакция плохо поддается контролю. Ее протекание и интенсивность напрямую зависят от температуры.
Применение
Изопропанол, в отличие от этилового спирта, стоит дешево, поэтому широко используется в производстве как заменитель этанола. Его часто используют при изготовлении дезинфицирующих средств, косметики, бытовой химии, антифризов, парфюмерии. Также он применяется для очистки металлических, стеклянных и других поверхностей от жира и грязи. Используется для промывки плат после пайки. Плюс этого спирта как очистителя – он быстро испаряется и не оставляет следов.
Техника безопасности
По ГОСТ 12.1.007 изопропиловый спирт относится к 3-му классу опасности. Самовоспламеняется при 450 оС, температура вспышки – 12 оС. Он токсичен и при высокой концентрации паров может воздействовать на организм при вдыхании. Смешиваясь с воздухом в виде пара, образует взрывоопасную смесь.
Концентрация паров изопропанола в рабочей зоне, где находятся люди, не должна превышать 10 мг/м3 . При возникновении аварийных ситуаций в качестве средства защиты следует использовать противогаз марки А или БКФ.
Транспортировка и хранение
Перевозить жидкость можно с использованием любого транспорта. Главное правило транспортировки и хранения – не допускать, чтобы спирт контактировал с другими веществами.
Решение вопросов перевозки мы готовы взять на себя – наша компания занимается продажей изопропанола с доставкой по Москве и России. При этом нас можно купить этот спирт совсем недорого. Чтобы заказать данную продукцию, воспользуйтесь формой обратной связи или позвоните нам по номеру +7 (495) 940-70-18.
Каким бывает изопропиловый спирт?
Химические характеристики

Физические характеристики изопропилового спирта
Летучесть вещества значительно выше, чем у воды. Это связано с его низкой плотностью, которая составляет 0,79 г/см3. Его кипение начинается при температуре 83°C, а при 450°C наступает самопроизвольное возгорание.
Если концентрация изопропанола превышает 2,5%, он становится взрывоопасным. Низкая температура снижает его вязкость. При показателях – 70°C вещество приобретает жидкую форму.
Ещё одно характерное свойство изопропанола – способность растворяться в бензоле и ацетоне.
Химическая формула изопропанола
При реакции с нагретой медью или хромовой кислотой, изопропанол превращается в ацетон. Во время этого процесса происходит отщепление молекулы водорода от спирта.
Поскольку изопропанол является растворителем, он легко повреждает резиновые и пластиковые изделия. Он имеет способность вступать в реакцию с такими металлами как калий.
| Показатель | Стандарт для технического изопропанола | Стандарт для абсолютизированного изопропанола | Метод анализа |
|---|---|---|---|
| Плотность (t 20 С) | 0,814-0,819 г/см3 | 0,785-0,786 г/см3 | раздел 1, ГОСТ 18995.1 |
| Внешний вид, цвет | жидкость без цвета и примесей | жидкость без цвета и примесей | пункт 4,2 |
| Изопропанол | от 87% | от 97% | пункты 4,3; 4,4 |
| Максимальная цветность | 10 | 5 | пункт 4,5 |
| Кислоты (в пересчете на уксусную кислоту) | до 0,001% | до 0,0007% | пункт 4,6 |
| Сернистые соединения (в пересчете на серу) | до 0,0001% | до 0,00005% | пункт 4,7 |
| Бромное число | не определяется | до 0,006 | пункт 4,8 |
| Вода | не определяется | до 0,15% | пункт 4,9 |
| Карбонильные соединения (в пересчете на СО2) | до 0,8% | не определяется | пункт 4,10 |
| Дизопропиловый эфир | не определяется | до 0,03% | пункт 4,11 |
| Ацетон | не определяется | до 0,03% | пункт 4,12 |
| Смешиваемость с водой | не определяется | выдерживает испытание | пункт 4,13 |
| Нелетучий остаток | не определяется | до 0,0005% | пункт 4,14 |
| Вещества, не растворимые в воде | выдерживает испытание | не определяется | пункт 4,14 |
Вещество в жидком состоянии имеет плотность 0,79 г/см3. Такая плотность ниже, чем у воды, поэтому изопропанол более летучий, чем вода. Он начинает кипеть при 83 градусах Цельсия. При концентрации более 2,5% в определенных условиях может взрываться. Самопроизвольное воспламенение происходит при нагреве до температуры выше 450 градусов Цельсия. Сочетание паров изопропилового спирта с воздухом способно образовывать взрывоопасную взвесь.
Спирт неплохо растворяется в ацетоне, бензоле. При добавлении в смесь воды и изопропанола поваренной соли он выделяется в отдельную фракцию.
Еще одним свойством изопропанола является постепенное увеличение вязкости при охлаждении. При значениях ниже – 70 °С имеет сиропообразную консистенцию.
Наиболее сильная линия поглощения молекул изопропанола приходится на ультрафиолетовую часть спектра (204 нм).
Взаимодействие
Поскольку спирт токсичен и обладает резким запахом, его использование допустимо только в хорошо вентилируемых помещениях. Ни в коем случае нельзя применять вещество внутрь. Это может привести к таким неприятным последствиям:
- тяжелейшее отравление;
- анафилактический шок;
- гибель.
Изопропиловый спирт относится к третьему классу токсичности (умеренно ядовит). Работая с ним, необходимо проявить максимальную осторожность. Попадая внутрь, 15% изопропиловый спирт переходит в ацетон. Это вызывает ацетонурию, которая проявляется следующими признаками:
- запах ацетона изо рта и в моче;
- кишечные расстройства, рвота с характерным запахом ацетона;
- бледность кожи;
- сильная слабость;
- повышение температуры.
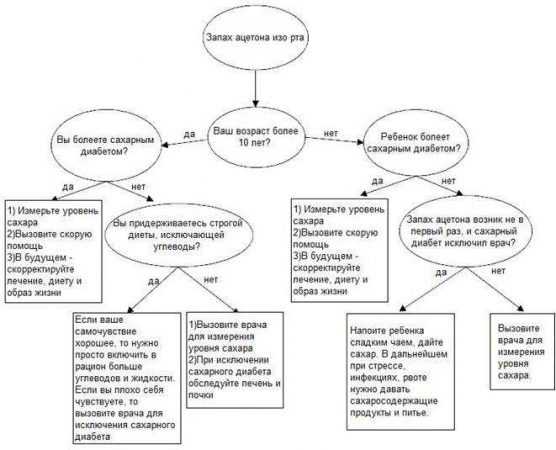
Ацетонурия
Антисептическое, дезинфицирующее.
При местном использовании побочные реакции, как правило, не возникают. Иногда возможны: сухость кожи, чувство пощипывания и покалывания (особенно при наличии ссадин и ран).
https://www.youtube.com/watch?v=NJp0eEXYNDo
Лекарственное взаимодействие вещества не описано. При местном использовании спирт не вступает во взаимодействие с другими средствами.
Фармакодинамика и фармакокинетика
Вещество раздражает дыхательные пути и глаза, при непродолжительном вдыхании больших концентраций вызывает сильную головную боль, угнетает работу ЦНС. При вдыхании концентраций, в несколько раз превышающих предельно допустимые, может привести к потере сознания.
При приеме внутрь средство подвергается метаболизму в печени, превращается в ацетони алкогольдегидрогеназу, оказывает токсическое действие на организм. Однако небольшие его концентрации, как правило, не приводят к каким-либо серьезным расстройствам в работе различных систем органов. Серьезного токсического воздействия можно добиться, приняв внутрь более 50 мл средства.
Следует отметить, что при приеме внутрь вещество вызывает опьянение, похожее на алкогольное. Скорость окисления спирта в организме примерно в 2,5 раза ниже, чем у этанола, эффект от приема сохраняется намного дольше.
При местном использовании вещество угнетает жизнедеятельность грамположительных и грамотрицательных бактерий, некоторых видов грибов (например, Candida). Не проникает в системный кровоток, быстро испаряется с поверхности кожи или впитывается.
Изопропанол, инструкция по применению (Способ и дозировка)
Широкое применение данного продукта способствует его активному производству. Ежегодно в мире изготавливается более 5 тонн изопропанола. Для этого применяют гидратацию (использование пропилена с водой).
Гидратация может быть прямой и косвенной. В первом случае для производства изопропилового спирта используют высококачественное сырьё, во втором – низкого качества.
Метод получения изопропилового спирта
Прямая гидратация базируется на участии катализаторов. Под действием реакции создаётся высокое давление, в результате чего на выходе получается спирт абсолютированный. Это продукт высшего качества, степень очистки которого превышает 90%.
Первоначальная смесь состоит на 88% из влажного спирта и на 12% – из воды. Для получения чистого продукта его необходимо отделить от компонентов реакции. Для этого применяют азеотропную дистилляцию, в процессе которой используют различного рода соединения, такие как циклогексан. Прямую гидратацию используют преимущественно в странах Европы.

Косвенная гидратация осуществляется посредством взаимодействия пропилена с серной кислотой. В результате их реакции образуются сложные эфиры. Такой способ производства активно применяют в США.
Получение изопропилового спирта осуществляется согласно ГОСТу 9805 84.
Способ применения лекарственного средства различается в зависимости от формы выпуска и показаний.
Антисептики для местного использования, содержащие спирт в составе, наносят тонким слоем на предварительно очищенную и сухую кожу или другую поверхность для дезинфекции. Затем средство втирают в кожу до полного его высыхания, в течение минуты.
При проведении предоперационной обработки рук особое внимание следует уделять пространству между пальцами и ногтевым пластинам.
Вероятность передозировки при местном использовании крайне мала. При случайно приеме внутрь наступает алкогольное отравление, тошнота, головная боль, возможен фруктовый аромат изо рта. Терапия –промывание желудка, энтеросорбенты.
Где применяют

Изопропанол в качестве заменителя этилового спирта
Изопропиловый спирт используется преимущественно как растворитель в промышленном производстве и в качестве заменителя этилового спирта, что позволяет применять его при изготовлении товаров автохимии.
Особое значение отведено изопропиловому спирту в медицинской сфере. Он выступает в качестве дезинфицирующего средства при обработке кожи перед инъекцией.
Поскольку вещество относится к дешевым, но очень эффективным растворителям, спектр его применения довольно широкий. Изопропанол используют при производстве:
- лакокрасочных материалов;
- бытовой химии;
- средств гигиены;
- парфюмерной и косметической продукции;
- полиграфических материалов;
- фармацевтических товаров;
- топлива;
- ацетона.
С помощью изопропанола извлекают древесинную смолу, поэтому он активно используется в деревообрабатывающей отрасли.
Применение в качестве растворителя
Популярность изопропанола в этом качестве неслучайна, поскольку, в отличие от других растворителей, он менее токсичен. Составы с его применением используют для чистки деталей электротехники, клавиатуры и прочего.
Он хорошо справляется с очищением древесины и тканей, что позволяет активно применять его в домашнем хозяйстве. Но чистить винил изопропиловым спиртом противопоказано.

Очищение древесины с помощью изопропилового спирта
Изопропанол в медицине и химическом производстве

Водный раствор изопропилового спирта используеться для дезинфекции
По медицинским показателям изопропанол используется в качестве осушающего средства для профилактики наружного отита.
Водный раствор изопропанола активно применяется для дезинфекции.

В химической отрасли из вещества добывают изопропилацетат. Данное вещество, вступая в реакцию с четыреххлористым титаном и алюминием, способствует выделению титана.
Применение в биологических исследованиях
Использование изопропанола в иследованиях
Благодаря тому, что молекулы ДНК не растворяются в изопропиловом спирте, его активно применяют при данного рода исследованиях. Добавление спирта в подготовленную ДНК способствует преципитации.
Ещё спирт активно используют для хранения анализов. С этой целью можно применять и формальдегид, но поскольку он более токсичен, предпочтение отдается изопропанолу.
Интоксикация изопропанолом
Интоксикация веществом может произойти в силу ряда причин. Самая опасная из них – употребление изопропилового спирта вместо алкоголя. Поскольку он стоит дешевле, злоупотребляющие алкоголем люди пытаются сэкономить, подвергая свою жизнь большой опасности. В лучшем случае это закончится ожогом слизистой, болью, инвалидностью, в худшем – гибелью.
Отравление изопропанолом
Нередко отравление веществом происходит в результате его попадания внутрь через кожу или органы дыхания. Даже в этом случае изопропанол хорошо всасывается в кровь и человеку становится плохо. Опасной дозой считается 15 грамм, в результате чего возникают сильные головные боли, слабость, рвота, повышение давления, боли в желудке.
Первое, что необходимо сделать в этом случае – вызвать бригаду скорой помощи.
С целью предотвращения отравления изопропанолом настоятельно рекомендуется:
- тщательно проветривать помещение, где хранится спирт;
- хранить вещество в недоступном для детей месте;
- использовать изопропанол только по назначению.
Вероятность хронического отравления изопропиловым спиртом очень мала, поскольку он не накапливается в организме.
Пропанол-1 — Википедия
Материал из Википедии — свободной энциклопедии
| Пропанол-1 | |||
|---|---|---|---|
| |||
| Систематическое наименование | пропан-1-ол | ||
| Традиционные названия | пропиловый спирт, 1-пропанол | ||
| Хим. формула | C3H7OH | ||
| Состояние | жидкость | ||
| Молярная масса | 60,09 г/моль | ||
| Плотность | 0,80 г/см³ | ||
| Динамическая вязкость | 2,256*10-3 Па·с | ||
| Энергия ионизации | 10,15 ± 0,01 эВ[1] | ||
| Температура | |||
| • плавления | −127 °C | ||
| • кипения | 97,4 °C | ||
| • вспышки | 72 ± 1 °F[1] | ||
| Пределы взрываемости | 2,2 ± 0,1 об.%[1] | ||
| Мол. теплоёмк. | 147,2 (25°C) Дж/(моль·К) | ||
| Теплопроводность | 0,16 Вт/(м·K) | ||
| Энтальпия | |||
| • образования | -302 кДж/моль | ||
| • плавления | 89,43 кДж/моль | ||
| • кипения | 749,01 кДж/моль | ||
| Коэфф. тепл. расширения | 0,956 *10-3 K-1 | ||
| Давление пара | 1,928 (20°C), 6,986 (40°C), 20,292 (60°C), 50,750 (80°C) кПа | ||
| Константа диссоциации кислоты pKa{\displaystyle pK_{a}} | 16 | ||
| Растворимость | |||
| • в воде | смешивается | ||
| Показатель преломления | 1,3850 | ||
| Дипольный момент | 1,68 D | ||
| Рег. номер CAS | 71-23-8 | ||
| PubChem | 1031 | ||
| Рег. номер EINECS | 200-746-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | UH8225000 | ||
| ChEBI | 28831 | ||
| Номер ООН | 1274 | ||
| ChemSpider | 1004 | ||
| ЛД50 | 1870 мг/кг | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Пропиловый спирт (пропан-1-ол, 1-пропанол) C3H7OH — одноатомный спирт. Встречается в природе в небольших количествах как продукт ферментации. Так, он является компонентом сивушного масла. Существует изомер 1-пропанола — изопропиловый спирт (пропан-2-ол, 2-пропанол).
Бесцветная жидкость со спиртовым запахом, смешивается с водой и образует с ней азеотропную смесь (т. кип. 87,5—88,0°С, 71,8 % по массе 1-пропанола). Растворим в этаноле, диэтиловом эфире, ацетоне, бензоле и других органических растворителях.
Пропиловый спирт обладает всеми химическими свойствами первичных одноатомных спиртов. Так он может быть превращён в галогеналканы: взаимодействие с йодом и красным фосфором даёт 1-йодпропан с 80 % выходом[2], тогда как взаимодействие хлорида фосфора (III) при катализе хлоридом цинка либо хлористого тионила при катализе ДМФА даёт 1-хлорпропан[3].
Реакция 1-пропанола с уксусной кислотой в присутствии серной кислоты даёт пропилацетат[4]. В то время как кипячение только с муравьиной кислотой в течение суток даёт пропилформиат с выходом 65 %.
.
Окисление бихроматом калия с серной кислотой в условиях отгонки образующего пропаналя позволяет получать его с выходом 50 %[5]. Более глубокое окисление хромовым ангидридом даёт пропионовую кислоту.
Взаимодействие со щелочными металлами даёт соответствующие пропиолаты металлов. Причём реакция протекает менее интенсивно чем с этиловым спиртом и намного менее интенсивно чем с водой.
- 2Ch4Ch3Ch3OH+2Na→2Ch4Ch3Ch3ONa+h3{\displaystyle {\mathsf {2CH_{3}CH_{2}CH_{2}OH+2Na\rightarrow 2CH_{3}CH_{2}CH_{2}ONa+H_{2}}}}
В промышленности 1-пропанол получают путём гидроформилирования этилена с последующим гидрированием образовавшегося пропаналя.
- C2h5+CO+h3→Ch4Ch3CHO+D{\displaystyle {\mathsf {C_{2}H_{4}+CO+H_{2}\rightarrow CH_{3}CH_{2}CHO+D}}}
- Ch4Ch3CHO+h3→Ch4Ch3Ch3OH{\displaystyle {\mathsf {CH_{3}CH_{2}CHO+H_{2}\rightarrow CH_{3}CH_{2}CH_{2}OH}}}
1-Пропанол получается в качестве побочного продукта при сбраживании зерна на этанол, но этот способ получения не имеет особого промышленного значения.
1-Пропанол применяют в качестве растворителя для восков, полиамидных чернил, природных и синтетических смол, полиакрилонитрила; в производстве полиэтилена низкого давления; для получения карбометоксицеллюлозы; как обезжириватель металлов; сорастворитель поливинилхлоридных адгезивов; желатинирующий и пластифицирующий агент целлюлозноацетатных плёнок; алкилирующий агент. Его используют также для синтеза пропионовой кислоты, пропионового альдегида, пропилацетата, пропиламина, ПАВ, пестицидов, некоторых фармацевтических препаратов.
Топливо[править | править код]
1-Пропанол имеет высокое октановое число (118)[6]. Однако производство его слишком дорого для того, чтобы он стал широко применяемым топливом.
Употребление пропилового спирта, также как и этилового спирта, вызывает алкогольное опьянение. В организме человека пропиловый спирт окисляется до пропионовой кислоты, более едкой, чем уксусная кислота, в связи с чем токсичность пропилового спирта значительно выше, чем у этилового (ЛД50 для пропилового спирта 1870 мг/кг, для этилового спирта 7060 мг/кг). В то же время по сравнению с метиловым спиртом, ЛД50 которого составляет 1500 мг/кг, пропиловый спирт относительно безопасен.[источник?]
ПДК пропилового спирта в воздухе рабочей зоны 10 мг/м3 (среднесменная за 8 часов) и 30 мг/м3 (максимально-разовая)[7], в атмосферном воздухе населенных пунктов — не более 0,3 мг/м3.
По данным[8] порог восприятия запаха мог достигать (среднее значение в группе) 540[9] и даже 25000 мг/м3; в работе[10] — 660 мг/м3 (то есть в 66 (22) раза выше ПДКрз).
На 2011 год был зафиксирован один смертельный случай отравления пропиловым спиртом[11].
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0533.html
- ↑ Органикум. Том 1. Москва, Мир, 1992, стр. 274
- ↑ Методы получения химических реактивов и препаратов. Москва, ИРЕА, Выпуск 2, 1961, стр. 45 (см. стр. 46)
- ↑ Органикум. Том 2. Москва, Мир, 1992, стр. 84 (см. табл. на стр. 85)
- ↑ Синтезы органических препаратов. Сборник 2.Москва, Иностранная Литература, 1949, стр. 424
- ↑ Bioalcohols (неопр.). Biofuel.org.uk. Дата обращения 16 апреля 2014.
- ↑ (Роспотребнадзор). № 1794. Пропан-1-ол (пропиловый спирт) // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» (рус.) / утверждены А.Ю. Поповой. — Москва, 2018. — С. 123. — 170 с. — (Санитарные правила).
- ↑ Pliska V. and G. Janicek. Die Veranderungen der Wahrnehmungsschwellen - Konzentration der Riechstoffe in Einiger Homologischen Serien (нем.) // Heymans Institute of Pharmacology Archives internationales de pharmacodynamie. — 1965. — Vol. 156. — P. 211–216. — ISSN 0003-9780.
- ↑ Janicek G., V. Pliska, and J. Kubátová. Olfactometric Estimation of the Threshold of Perception of Odorous Substances by a Flow Olfactometer (чешск.) // Československá hygiena. — Praha, 1960. — Vol. 5. — P. 441–447. — ISSN 0009-0573.
- ↑ William S. Cain. Odor Intensity: Differences in the Exponent of the Psychophysical Function (англ.) // Perception & Psychophysics. — Springer-Verlag, 1969. — November (vol. 6 (iss. 6). — P. 349–354. — ISSN 1943-3921. — doi:10.3758/BF03212789.
- ↑ N-PROPANOL Health-Base Assessment and Recommendation for HEAC (неопр.) (недоступная ссылка). Дата обращения 31 июля 2012. Архивировано 7 августа 2012 года.
Обсуждение:Изопропанол — Википедия
Материал из Википедии — свободной энциклопедии
Есть подозрение на наличие зафикисированных смертельных случаев
http://ms-marple.livejournal.com/256629.html
109.188.127.38 21:59, 9 ноября 2013 (UTC)Артур
Наркотические свойства изопропанола[править код]
Уважаемый Sirozha, будьте добры объясните, почему Вы откатили 4 последние правки. Константин Земляникин 05:56, 11 августа 2011 (UTC)
- Потому что они нарушают авторские права трех интернет-ресурсов. Почитайте Википедия:Авторские права --Sirozha.ru 07:47, 11 августа 2011 (UTC)
- Я хочу включить данную информацию в статью. Как Вы предлагаете решить ситуацию? Каким образом следует включить информацию, чтобы она не нарушала авторских прав? Константин Земляникин 14:25, 11 августа 2011 (UTC)
- Вы можете переписать информацию СВОИМИ СЛОВАМИ и сделать ссылки источник. Лучше, конечно, на какую нибудь энциклопедию или учебник Sirozha.ru 17:04, 11 августа 2011 (UTC)
- Я хочу включить данную информацию в статью. Как Вы предлагаете решить ситуацию? Каким образом следует включить информацию, чтобы она не нарушала авторских прав? Константин Земляникин 14:25, 11 августа 2011 (UTC)
Sirozha, объясните пожалуйста, почему Вы считаете что "Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена" ?
По моим сведениям мощности предприятии получающего изопропанол гидрированием ацетона водородом превышают в разы мощности предприятия получающего изопропанол сернокислотной гидратацией пропилена.
На чём основывается Ваше убеждение в несомненной правоте текущего высказывания ?аноним
- Пожалуйста, приведите ВП:АИ, подтверждающие вашу точку зрения --Sirozha.ru 13:11, 28 ноября 2011 (UTC)
Изопропанол - неверное название[править код]
Один из способов названия спиртов является добавление окончания "ол" к названию исходного алкана (не алкильного радикала). Так как не существует такого алкана как "изопропан", то называть 2-пропанол изопропанолом неправильно.
Денис
Я нихрена не понял. "развитых странах пропанол-2 широко используется в товарах личной гигиены и в медицине, благодаря низкой токсичности" " Безопасность Токсичность довольно высокая ". Так какая у него токсичность, че вы тут понаписали ? 109.229.86.228 22:01, 3 сентября 2016 (UTC)мимопроходил
- Да, изопропанол не токсичен наружно (и даже обладает лечебным действием против всяких там экзем) и всего в 2 раза токсичнее этилового спирта, но при этом он и в 2 раза более опьяняющ, но распадается он не на альдегид (пропанол-1 распадается на пропаналь), а на ацетон, который хоть и менее токсичен чем "перегар" (ацеталь), но вызывает рвоту, головную боль и сильное состояние похмелье. Причем это начинается не после бутылки изопропанола, а уже на стадии всасывания в желудке, поэтому нормальный пить его не будет. Поэтому этанол активно заменили изопропанолом дл целей дезинфекции, подтверждаю, сам был в больнице не так давно (живу в глубинке), при протирании перед инъекцией пахло именно изопропанолом. Этиловый спирт остался только в виде одноразовых салфеток для протирания перед инъекцией, ну и в виде не совсем легальных растворов вроде асептолина. 95.78.216.96 06:35, 5 мая 2019 (UTC)
- на самом деле изопропил токсичен и вонюч, а в статье просто наврано в угоду тем кто его использует. фруктами он пахнет, хех.. ) шутники...) 46.188.29.89 18:12, 11 сентября 2016 (UTC)
- Ну во-первых это вам не бутилацетат чтобы грушами пахнуть. Пахнет он специфически, надо сказать не так противно как этиловый спирт, даже немного приятно. Так что утверждение вонюч совершенно неверно — вы наверное валерьяновую и масляную кислоту не нюхали прямо из бутыли задыхом. Ибо они пахнут рвотой и сразу тошнить начинает (может и вырвать). Вот уж что действительно вонюче. 95.78.216.96 06:35, 5 мая 2019 (UTC)
Казнить нельзя помиловать[править код]
Вода способствует проникновению сквозь мембраны пор бактерий, таким образом обеспечивая... 1) Поры у мембран или у бактерий? 2) У мембран бывают поры? 3) У бактерий бывают поры? Если же речь не о порах, а о спорах (бактерий), то непонятно, какая польза для обеззараживания в их проникновении сквозь мембраны. И сквозь какие именно мембраны - тоже непонятно. --Michael MM (обс.) 04:28, 16 декабря 2017 (UTC)
- Где это ерунда написана? У мембран бывают поры, но бактерии через них не проникнут, разве что всякие спирохеты или плазмодии, но они и просто через мембраны проникают делая дырку в них. Изопропиловый спирт убивает споры бактерий, но не всех, и не все вирусы. Это все таки не формалин, который убивает все и моментально. 95.78.216.96 06:39, 5 мая 2019 (UTC)
Из раздела "Влияние на человека/Пероральное" следует что для опьянения пить изопропанол предпочтительнее этанола. При том же эффекте опьянения токсичность ниже. Нет ли тут ошибки? 85.140.232.216 02:21, 30 января 2018 (UTC)
- Токсичность (по памяти) у изопропанола ровно в два раза выше, чем у этанола. Но фишка в том, что фермент алкогольдегидрогеназа содержится не только в печени, но и в стенке желудка. И из-за разветвленности цепи она перерабатывает изопропанол не в пропаналь (едкий, но не токсичнее ацеталя), а в ацетон, который вообще почти не токсичен, зато замечательно активирует D2-рецепторы в желудке, гортани, глотке, на корне языка и в рвотном ядре продолговатого мозга, которые дружно отвечают на это рвотой. И даже если рвоты не будет (при низкой концентрации), то и опьянения не будет, просто будет стойко (и долго) нести ацетоном от дыхания 95.78.216.96 06:51, 5 мая 2019 (UTC)
По поводу брехни и источников[править код]
Слушайте, предлагаю вычистить всю хрень из статьи, либо если есть мотивация нормально прошерстить источники (включая обязательно научные иноязычные!!!!). Спирт все таки важный, ходовой, заменил этанол в медицине как антисептик, продается бутылями для отмывки плат в радиотехнических магазинах... С вашего позволения, вычищаю все нахрен и вставляю шаблоны типа "дополнить". Откатите — ваше дело, но подумайте о важности статьи и о том, что на текущий момент она наполнена какой-то фигней! 95.78.216.96 06:56, 5 мая 2019 (UTC)