Альбумин формула химическая
Альбумины — Википедия
Альбумины (от лат. albus — белый) — простые растворимые в воде белки, умеренно растворимые в концентрированных растворах соли и свёртывающиеся при нагревании (денатурация белка). Их относительная молекулярная масса составляет примерно 65000 Да, не содержат углеводов. Вещества, содержащие альбумин, такие как яичный белок, называются альбуминоидами. Альбуминоидами являются также сыворотка крови, эндосперм растений.
Кроме воды растворимы в солевых растворах, кислотах и щелочах; при гидролизе распадаются на различные аминокислоты. Альбумины могут быть получены в кристаллическом виде.
Проявляют высокую связывающую способность по отношению к различным низкомолекулярным соединениям, содержат гидрофильные и липофильные связи.
Наиболее известный вид альбумина — сывороточный альбумин. Он содержится в крови в сыворотке (отсюда название), но он также может встречаться в других жидкостях (например, в спинно-мозговой жидкости).
Сывороточный альбумин синтезируется в печени и составляет большую часть среди всех сывороточных белков. Альбумин, содержащийся в крови человека, называется человеческий сывороточный альбумин, он составляет около 55 % от всех белков, содержащихся в плазме крови.
Поскольку концентрация альбумина высока, а размеры его молекулы невелики, этот белок на 80 % определяет коллоидно-осмотическое давление плазмы.
Общая площадь поверхности множества мелких молекул сывороточного альбумина очень велика, поэтому они особенно хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью и плохо растворимых в воде веществ. К веществам, связываемым сывороточным альбумином, относятся билирубин, уробилин, жирные кислоты, соли желчных кислот, некоторые экзогенные вещества — пенициллин, сульфамиды, ртуть, липидные гормоны, некоторые лекарства, такие как варфарин, фенобутазон, хлофибрат и фенитоин и т. д. Одна молекула альбумина может одновременно связать 25—50 молекул билирубина (молекулярная масса 585 Да). По этой причине сывороточный альбумин иногда называют «молекулы-такси». Конкуренция между лекарствами за места связывания на молекуле альбумина может вызвать увеличение концентрации в свободном виде одного из лекарств или обоих, что повлияет на их активность.
На мембранах клеток имеются рецепторы к альбуминам — альбандины.
Наиболее широко используются человеческий сывороточный альбумин и бычий сывороточный альбумин, часто применяемый в медицинских и молекулярно-биологических лабораториях.
Нормальный уровень сывороточного альбумина у взрослых составляет от 35 до 50 г/л. Для детей в возрасте менее 3 лет нормальный уровень — в пределах 25—55 г/л.
Низкий уровень альбумина (гипоальбуминемия) может возникать из-за болезни печени, нефротического синдрома, ожогов, энтеропатии с потерей белка, недоедания, на поздних сроках беременности, злокачественных новообразований. Приём ретинола (витамина А) в некоторых случаях может повысить уровень альбумина до высоких субнормальных значений (49 г/л). Лабораторные эксперименты показали, что приём ретинола регулирует синтез человеческого альбумина.
Высокий уровень альбумина (гиперальбуминемия) почти всегда возникает в результате обезвоживания.
Другие типы включают в себя альбумины яичного белка (кональбумин, овальбумин, авидин), C-реактивный белок, лактальбумин (альфа-лактальбумин), парвальбумин, рицин.
Измерение уровня альбумина является компонентом теста функции печени. Измерение уровня альбумина может проводиться и как самостоятельный анализ.
Яичный, молочный, сывороточный альбумины применяются в кондитерском и текстильном производстве, в фармации и медицине. Молочный альбумин составляет основу итальянского молочного продукта рикотта и его аналогов у других народов. По методу академика Б. Патона альбумин применяется в качестве сварочного материала в хирургических операциях, по методике плазменной сварки живых тканей кишечника и желудка человека. Яичный альбумин так же используются в некоторых способах фотопечати.
Альбумин, его свойства и функции (стр. 1 из 2)
Реферат на тему
Альбумин, его свойства и функции
Работу выполнила
Ворожцова Анастасия
Содержание
Что такое альбумин
Физические и химические свойства
Биологические свойства и функции
Сывороточный альбумин
Транспортная функция сывороточного альбумина
Когда же уровень альбумина в крови бывает сниженным?
Гипоальбумения
Альбумин представляет собой самую большую фракцию белков плазмы крови человека - 55 - 65%. В состав белковой молекулы альбумина входят все 20 аминокислот. Синтез альбумина происходит в печени. Основная функция альбумина в организме человека - поддержание коллоидно-онкотического давления крови. В процессе голодания в первую очередь расходуется альбумин плазмы, что приводит к снижению коллоидно-осмотического давления и формированию "голодных" отеков. Альбумин связывает и транспортирует билирубин, различные гормоны, жирные кислоты, ионы кальция, хлора, лекарственные вещества. Гиперальбуминемия встречается редко, вызывает сильное обезвоживание организма и выраженный венозный застой. Вещества, содержащие альбумин, такие как яичный белок, называются альбуминоиды. Альбуминоидами являются также сыворотка крови, семена растений.
Кроме воды растворимы в солевых растворах, кислотах и щелочах; при гидролизе распадаются на различные аминокислоты. Альбумины могут быть получены в кристаллическом виде. Свертывается при нагревании (денатурация белка) нейтральны. Их относительная молекулярная масса составляет примерно 65000 дальтон, не содержат углеводов. Примерами их могут служить: альбумин белка куриного яйца, альбумин кровяной сыворотки, альбумин мускульной ткани, молочный альбумин.
Основными биологическими функциями альбумина являются поддержание онкотического давления плазмы, транспорт молекул и резервом аминокислот. Проявляют высокую связывающую способность по отношению к различным низкомолекулярным соединениям. Альбумин несет еще одну функцию в крови - транспортную. Дело в том, что благодаря большому числу молекул альбумина и их мелкому размеру, они отлично переносят на себе как продукты жизнедеятельности организма, такие как билирубин, желчные элементы. А еще молекулы альбумина переносят на себе и лекарства, например, некоторые виды антибиотиков, сульфаниламиды, кое-какие гормоны и даже яды.
Наиболее известный вид альбумина - сывороточный альбумин. Он содержится в крови в сыворотке (отсюда название), но он также может встречаться в других жидкостях (например, в спинно-мозговой жидкости). Сывороточный альбумин синтезируется в печени и составляет большую часть среди всех сывороточных белков. Альбумин, содержащийся в крови человека, называется человеческий сывороточный альбумин, он составляет около 60 % от всех белков, содержащихся в плазме крови.
Общая площадь поверхности множества мелких молекул сывороточного альбумина очень велика, поэтому они особенно хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью и плохо растворимых в воде веществ. К веществам, связываемым сывороточным альбумином, относятся билирубин, уробилин, жирные кислоты, соли желчных кислот, некоторые экзогенные вещества - пенициллин, сульфамиды, ртуть, липидные гормоны, некоторые лекарства, такие как варфарин, фенобутазон, хлофибрат и фенитоин и т.д. Одна молекула альбумина может одновременно связать 25-50 молекул билирубина (молекулярная масса 500). По этой причине сывороточный альбумин иногда называют "молекулы-такси". Соревнования между лекарствами при использовании ими "посадочных мест" на молекуле альбумина может вызвать увеличение их активности и лечебного действия.
Наиболее широко используются человеческий сывороточный альбумин и бычий сывороточный альбумин, часто применяемый в медицинских и молекулярно-биологических лабораториях.
Нормальный уровень сывороточного альбумина у взрослых составляет от 35 до 50 г/л. Для детей в возрасте менее 3-х лет нормальный уровень - в пределах 25-55 г/л.
Низкий уровень альбумина (гипоальбуминемия) может возникать из-за болезни печени, нефритического синдрома, ожогов, энтеропатии с потерей белка, недоедания, на поздних сроках беременности, злокачественных новообразований. Приём ретинола (витамина А) в некоторых случаях может повысить уровень альбумина до высоких субнормальных значений (49 г/л). Лабораторные эксперименты показали, что приём ретинола регулирует синтез человеческого альбумина.
Высокий уровень альбумина (гиперальбуминемия) почти всегда возникает в результате обезвоживания.
Различным структурным классам связываемых веществ (называемых обычно лигандами) на молекуле альбумина соответствуют отдельные специфичные центры связывания. Для многих лигандов альбумина известна направленность их транспорта в организме от одних органов и тканей к другим. Так, например, токсические продукты жизнедеятельности и ионы тяжелых металлов должны быть доставлены в соответствующие органы выделения. Такой же метаболит как триптофан доставляется главным образом в центральную нервную систему, где превращается в нейромедиа-тор серотонин. Можно полагать, что в ряде случаев лиганд может не только избирательно освобождаться в капиллярах определенных тканей, но эта "разгрузка" должна производиться достаточно быстро и полно. Простейшая избирательность "адреса доставки" может быть достигнута снижением равновесной концентрации свободного лиганда в кровеносных капиллярах или межклеточной жидкости тканей-адресатов, вследствие быстрого всасывания и связывания лигандов структурами самой ткани. Не исключено, однако, что в органах и тканях существуют специальные специфические механизмы регуляции связывания и освобождения лигандов, взаимодействующих с альбумином.
Одним из механизмов регуляции скорости, прочности и емкости связывания отдельных классов транспортируемых альбумином лигандов может быть изменение в капиллярах и интерстиции отдельных тканей некоторых физико-химических характеристик, таких как рН, ионная сила, ионный состав, температура, то есть направленное отклонение от среднего отдельных компонентов гомеостаза крови и межклеточной жидкости. Предпосылки для такого механизма имеются как в свойствах самого белка-транспортера, так и в известных потенциальных возможностях гомеостатических сдвигов в различных органах и тканях организма. Для сывороточных альбуминов характерны изменения структурных и физико-химических свойств в области средних физиологических значений рН, температуры (структурная перестройка при 30° - 40°С). Известно и влияние этих переходов на связывание некоторых классов лигандов. Уже это может служить предпосылкой для рассматриваемого механизма регуляции транспорта.
С другой стороны, средние значения основных физико-химических параметров крови крупных кровеносных сосудов подвержены вариациям от ткани к ткани и при изменении физиологического состояния организма. В зависимости от физиологического состояния, от локализации того или иного органа или ткани в теле теплокровного животного, от температуры и влажности окружающей среды и от специфики и интенсивностибиоэнергетических и других метаболических процессов в данной ткани, температура в кровеносных капиллярах и в интерстициальном пространстве может варьировать от 10-15° до 42°. При физических нагрузках, воспалительных процессах и некоторых нарушениях обмена веществ (например, при кетозе) значение рН в периферических органах и тканях также может существенно отличаться от указанной средней величины. Концентрация осмотически активных веществ в сыворотке крови составляет в среднем 0,3 моля/л. Ионный состав плазмы крови обычно постоянен. Однако, при некоторых патологических состояниях, а также при бессолевой диете, усиленном потоотделении и др. могут происходить значительные изменения ионного состава плазмы крови, сопровождающиеся уменьшением содержания в ней Ма,$, К, Са и других ионов.
Такие изменения температуры, рН, ионной силы и ионного состава внутренней среды организма могут оказывать существенное влияние на взаимодействие лигандов с сывороточным альбумином, а значит и на его транспортные функции. Однако даже в нормальном физиологическом состоянии эти параметры могут подвергаться значительным отклонениям от средних значений в капиллярах и межклеточном пространстве отдельных тканей. Причиной таких отклонений могут служить, например, ионообменные процессы в выстилке капилляров и на поверхности клеток. Высокой эффективности таких процессов способствует значительное отношение поверхности к объему в капиллярах и межклеточных щелях, по сравнению с крупными сосудами.
альбумин кровь сывороточный
Понижен уровень альбумина в организме в тех случаях, когда его меньше вырабатывается в организме, либо когда он выводится из него. В норме молекула альбумина живет от восемнадцати до двадцати суток. Альбумин в крови является еще и хранилищем протеинов в организме. Если Вы, например, проводите голодание на воде, то именно за счет альбуминов и будет пополняться потребность организма в белке. Поэтому во время голодовки количество альбумина уменьшается. То же самое происходит и во время беременности. У организма увеличивается потребность в белках для строительства нового организма. Также, уровень альбумина уменьшен во время кормления грудью. Курильщики, Вас эта проблема также касается. В крови курильщика уровень альбумина понижен. Ведь печени не до этого, ей и так тяжело приходится. Поэтому страдает выработка альбумина.
Есть люди, генетически предрасположенные к пониженному уровню альбумина в крови. При множестве тяжелых внутренних болезней также страдает выработка альбумина. Это может быть и онкологическое заболевание, и болезни печени, и нарывы на теле.
Содержание
Реферат на тему
Альбумин, его свойства и функции
Работу выполнила
Ворожцова Анастасия
Что такое альбумин 3
Физические и химические свойства 3
Биологические свойства и функции 3
Сывороточный альбумин 4
Транспортная функция сывороточного альбумина 5
Когда же уровень альбумина в крови бывает сниженным? 7
Гипоальбумения 8
Что такое альбумин
Альбумин представляет собой самую большую фракцию белков плазмы крови человека - 55 - 65%. В состав белковой молекулы альбумина входят все 20 аминокислот. Синтез альбумина происходит в печени. Основная функция альбумина в организме человека - поддержание коллоидно-онкотического давления крови. В процессе голодания в первую очередь расходуется альбумин плазмы, что приводит к снижению коллоидно-осмотического давления и формированию "голодных" отеков. Альбумин связывает и транспортирует билирубин, различные гормоны, жирные кислоты, ионы кальция, хлора, лекарственные вещества. Гиперальбуминемия встречается редко, вызывает сильное обезвоживание организма и выраженный венозный застой. Вещества, содержащие альбумин, такие как яичный белок, называются альбуминоиды. Альбуминоидами являются также сыворотка крови, семена растений.
Физические и химические свойства
Кроме воды растворимы в солевых растворах, кислотах и щелочах; при гидролизе распадаются на различные аминокислоты. Альбумины могут быть получены в кристаллическом виде. Свертывается при нагревании (денатурация белка) нейтральны. Их относительная молекулярная масса составляет примерно 65000 дальтон, не содержат углеводов. Примерами их могут служить: альбумин белка куриного яйца, альбумин кровяной сыворотки, альбумин мускульной ткани, молочный альбумин.
Биологические свойства и функции
Основными биологическими функциями альбумина являются поддержание онкотического давления плазмы, транспорт молекул и резервом аминокислот. Проявляют высокую связывающую способность по отношению к различным низкомолекулярным соединениям. Альбумин несет еще одну функцию в крови - транспортную. Дело в том, что благодаря большому числу молекул альбумина и их мелкому размеру, они отлично переносят на себе как продукты жизнедеятельности организма, такие как билирубин, желчные элементы. А еще молекулы альбумина переносят на себе и лекарства, например, некоторые виды антибиотиков, сульфаниламиды, кое-какие гормоны и даже яды.
Сывороточный альбумин
Наиболее известный вид альбумина - сывороточный альбумин. Он содержится в крови в сыворотке (отсюда название), но он также может встречаться в других жидкостях (например, в спинно-мозговой жидкости). Сывороточный альбумин синтезируется в печени и составляет большую часть среди всех сывороточных белков. Альбумин, содержащийся в крови человека, называется человеческий сывороточный альбумин, он составляет около 60 % от всех белков, содержащихся в плазме крови.
Общая площадь поверхности множества мелких молекул сывороточного альбумина очень велика, поэтому они особенно хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью и плохо растворимых в воде веществ. К веществам, связываемым сывороточным альбумином, относятся билирубин, уробилин, жирные кислоты, соли желчных кислот, некоторые экзогенные вещества - пенициллин, сульфамиды, ртуть, липидные гормоны, некоторые лекарства, такие как варфарин, фенобутазон, хлофибрат и фенитоин и т.д. Одна молекула альбумина может одновременно связать 25-50 молекул билирубина (молекулярная масса 500). По этой причине сывороточный альбумин иногда называют "молекулы-такси". Соревнования между лекарствами при использовании ими "посадочных мест" на молекуле альбумина может вызвать увеличение их активности и лечебного действия.
Наиболее широко используются человеческий сывороточный альбумин и бычий сывороточный альбумин, часто применяемый в медицинских и молекулярно-биологических лабораториях.
Нормальный уровень сывороточного альбумина у взрослых составляет от 35 до 50 г/л. Для детей в возрасте менее 3-х лет нормальный уровень - в пределах 25-55 г/л.
Низкий уровень альбумина (гипоальбуминемия) может возникать из-за болезни печени, нефритического синдрома, ожогов, энтеропатии с потерей белка, недоедания, на поздних сроках беременности, злокачественных новообразований. Приём ретинола (витамина А) в некоторых случаях может повысить уровень альбумина до высоких субнормальных значений (49 г/л). Лабораторные эксперименты показали, что приём ретинола регулирует синтез человеческого альбумина.
Высокий уровень альбумина (гиперальбуминемия) почти всегда возникает в результате обезвоживания.
Альбумины - это... Что такое Альбумины?
АльбуминАльбумины (лат.: albus, белый) — простые растворимые в воде белки, умеренно растворимые в концентрированных растворах соли и свёртывающиеся при нагревании (денатурация белка). Их относительная молекулярная масса составляет примерно 65000, не содержат углеводов. Вещества, содержащие альбумин, такие как яичный белок, называются альбуминоиды. Альбуминоидами являются также сыворотка крови, семена растений.
Физические и химические свойства
Кроме воды растворимы в солевых растворах, кислотах и щелочах; при гидролизе распадаются на различные аминокислоты. Альбумины могут быть получены в кристаллическом виде.
Биологические свойства и функции
Проявляют высокую связывающую способность по отношению к различным низкомолекулярным соединениям, содержат гидрофильные и липофильные связи.
Сывороточный альбумин
Наиболее известный вид альбумина — сывороточный альбумин. Он содержится в крови в сыворотке (отсюда название), но он также может встречаться в других жидкостях (например, в спинно-мозговой жидкости).
Сывороточный альбумин синтезируется в печени и составляет большую часть среди всех сывороточных белков. Альбумин, содержащийся в крови человека, называется человеческий сывороточный альбумин, он составляет около 55 % от всех белков, содержащихся в плазме крови.
Поскольку концентрация альбумина высока, а размеры его молекулы невелики, этот белок на 80 % определяет коллоидно-осмотическое давление плазмы.
Общая площадь поверхности множества мелких молекул сывороточного альбумина очень велика, поэтому они особенно хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью и плохо растворимых в воде веществ. К веществам, связываемым сывороточным альбумином, относятся билирубин, уробилин, жирные кислоты, соли желчных кислот, некоторые экзогенные вещества — пенициллин, сульфамиды, ртуть, липидные гормоны, некоторые лекарства, такие как варфарин, фенобутазон, хлофибрат и фенитоин и т. д. Одна молекула альбумина может одновременно связать 25—50 молекул билирубина (молекулярная масса 500). По этой причине сывороточный альбумин иногда называют «молекулы-такси». Соревнования между лекарствами при использовании ими «посадочных мест» на молекуле альбумина может вызвать увеличение их активности и лечебного действия.
На мембранах клеток имеются рецепторы к альбуминам — альбандины.
Наиболее широко используются человеческий сывороточный альбумин и бычий сывороточный альбумин, часто применяемый в медицинских и молекулярно-биологических лабораториях.
Нормальный уровень сывороточного альбумина у взрослых составляет от 35 до 50 г/л. Для детей в возрасте менее 3-х лет нормальный уровень — в пределах 25—55 г/л.
Низкий уровень альбумина (гипоальбуминемия) может возникать из-за болезни печени, нефритического синдрома, ожогов, энтеропатии с потерей белка, недоедания, на поздних сроках беременности, злокачественных новообразований. Приём ретинола (витамина А) в некоторых случаях может повысить уровень альбумина до высоких субнормальных значений(49 г/л). Лабораторные эксперименты показали, что приём ретинола регулирует синтез человеческого альбумина.
Высокий уровень альбумина (гиперальбуминемия) почти всегда возникает в результате обезвоживания.
Другие типы альбуминов
Другие типы включают в себя альбумины яичного белка (кональбумин, овальбумин, авидин), C-реактивный белок, лактальбумин (альфа-лактальбумин), парвальбумин, рицин.
Измерение уровня альбумина
Изменение уровня альбумина является компонентом теста функции печени. Измерение уровня альбумина может проводиться и как самостоятельный анализ.
Применение
Яичный, молочный, сывороточный альбумины применяются в кондитерском и текстильном производстве, в фармации и медицине. По методу академика Б. Патона альбумин применяется в качестве сварочного материала в хирургических операциях, по методике плазменной сварки живых тканей кишечника и желудка человека.
См. также
Плазмозамещающие и перфузионные растворы — АТХ код: B05
| B05A |
| ||
|---|---|---|---|
| B05B |
| ||
| B05C |
| ||
| B05D |
| ||
| B05X |
| ||
| B05Z |
Бычий сывороточный альбумин — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 мая 2014; проверки требуют 10 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 мая 2014; проверки требуют 10 правок.Бычий сывороточный альбумин (сокращённо БСА, англ. Bovine Serum Albumin, BSA) — белок плазмы крови крупного рогатого скота с молекулярной массой 69 000 Да, одноцепочечный, состоящий из 607 аминокислотных остатков.
Бычий сывороточный альбумин (БСА) — наиболее широко изученный и наиболее распространённый протеин крови (70% от общего протеинового состава). Его концентрация в плазме составляет 35-55 мг/мл.
Бычий сывороточный альбумин представляет собой глобулу в форме сплюснутого эллипсоида вращения с полуосями 17 на 42 ангстрем, состоящую из 607 аминокислотных остатков, их список и количество представлены в таблице:
| Ala 48 | Cys 35 | Asp 41 | Glu 58 |
| Phe 30 | Gly 17 | His 16 | Ile 15 |
| Lys 60 | Leu 65 | Met 5 | Asn 14 |
| Pro 28 | Gln 21 | Arg 26 | Ser 32 |
| Thr 34 | Val 38 | Trp 2 | Tyr 21 |
БСА обладает достаточно сложной пространственной структурой, образующих три домена, каждый из которых, в свою очередь подразделяется на два поддомена (A-B и C). Каждый поддомен можно разбить на 3 спирали X, Y и Z. Вторичную структуру БСА, по данным (1H NMR) на 50-68% составляют альфа спирали, 16—18 % бета складки. Третичная структура образована дисульфидными связями, которых в молекуле БСА насчитывается 17 штук (по количеству цистеиновых аминокислотных остатков). Молекулярная масса БСА = ~69 кДа.
Он является удобной моделью для изучения свойств глобулярных белков.
Благодаря доступности исходного материала, стабильным методикам выделения, и, как результат, относительно невысокой цене и хорошей изученности свойств, бычий сывороточный альбумин широко применяется в лабораторной практике.
БСА применяется в качестве стандарта в различных методах количественного определения белков, в качестве стандарта молекулярной массы белков (маркера) в гель-хроматографии и электрофорезе белков в денатурированном состоянии (SDS-PAGE), а также как стандартный антиген при определении изменения иммунного ответа под действием иммуномодуляторов или других факторов. Так же используется для стабилизации некоторых ферментов, в частности эндонуклеаз рестрикции. Предотвращает адгезию ферментов к стенкам сосуда.
Примитивные способы:
- «В кровяную сыворотку (кровь, лишённую фибрина) наливают воды в количестве, превышающем по объему в двадцать раз объем сыворотки, затем глобулин осаждают, осторожно прибавляя уксусную кислоту. Дав жидкости отстояться, её фильтруют и нейтрализуют содой, выпаривают при 40° и диализом выделяют большую часть солей».
- «Для технических целей его готовят, выпуская кровь прямо из животного в неглубокие цинковые чашки емкостью в несколько литров. В них её охлаждают, пока она не свернется; нужно тщательно стараться не взбалтывать свежевыпущенную кровь, поэтому место, где производится операция, следует выбирать поблизости от животного. Когда кровь окончательно свёртывается, её переносят в такие же чаши с перфорированными днищами и режут кровяной сгусток на мелкие кусочки, чтобы дать возможность стечь сыворотке. Сыворотку собирают и выпаривают при умеренной температуре, остаток называется альбумином. Следует избегать всякого сотрясения, так как при этом разрываются красные кровяные тельца, и цвет продукта портится. Пять быков дают около 20 литров сыворотки и около 2 кг альбумина».
Альбумин Википедия
АльбуминАльбумины (от лат. albus — белый) — простые растворимые в воде белки, умеренно растворимые в концентрированных растворах соли и свёртывающиеся при нагревании (денатурация белка). Их относительная молекулярная масса составляет примерно 65000 Да, не содержат углеводов. Вещества, содержащие альбумин, такие как яичный белок, называются альбуминоидами. Альбуминоидами являются также сыворотка крови, эндосперм растений.
Содержание
- 1 Физические и химические свойства
- 2 Биологические свойства и функции
- 3 Сывороточный альбумин
- 4 Другие типы альбуминов
- 5 Измерение уровня альбумина
- 6 Применение
- 7 См. также
Физические и химические свойства[ | ]
Кроме воды растворимы в солевых растворах, кислотах и щелочах; при гидролизе распадаются на различные аминокислоты. Альбумины могут быть получены в кристаллическом виде.
Биологические свойства и функции[ | ]
Проявляют высокую связывающую способность по отношению к различным низкомолекулярным соединениям, содержат гидрофильные и липофильные связи.
Сывороточный альбумин[ | ]
| В этом разделе не хватает ссылок на источники информации.Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 30 декабря 2019 года. |
Наиболее известный вид альбумина — сывороточный альбумин. Он содержится в крови в сыворотке (отсюда название), но
Альбумины
Альбумины – простые низкомолекулярные гидрофильные белки. В молекуле альбумина содержится 600 аминокислот. Молекулярная масса 67 кДа. Альбумины, как и большинство других белков плазмы крови, синтезируются в печени. Примерно 40% альбуминов находится в плазме крови, остальное количество - в интерстициальной жидкости и в лимфе.
ФУНКЦИИ АЛЬБУМИНОВ
Определяются их высокой гидрофильностью и высокой концентрацией в плазме крови.
1. Поддержание онкотического давления плазмы крови. Поэтому при уменьшении содержания альбуминов в плазме падает онкотическое давление, и жидкость выходит из кровяного русла в ткани. Развиваются "голодные" отеки. Альбумины обеспечивают около 80% онкотического давления плазмы. Именно альбумины легко теряются с мочой при заболеваниях почек. Поэтому они играют большую роль в падении онкотического давления при таких заболеваниях, что приводит к развитию «почечных» отеков.
2. Альбумины – это резерв свободных аминокислот в организме, образующихся в результате протеолитического расщепления этих белков.
3. Транспортная функция. Альбумины транспортируют в крови многие вещества, особенно такие, которые плохо растворимы в воде: свободные жирные кислоты, жирорастворимые витамины, стероиды, некоторые ионы (Ca2+, Mg2+). Для связывания кальция в молекуле альбумина имеются специальные кальцийсвязывающие центры. В комплексе с альбуминами транспортируются многие лекарственные препараты, например, ацетилсалициловая кислота, пенициллин.
Глобулины
В отличие от альбуминов глобулины не растворимы в воде, а растворимы в слабых солевых растворах.
1-ГЛОБУЛИНЫ
В эту фракцию входят разнообразные белки. 1-глобулины имеют высокую гидрофильность и низкую молекулярную массу - поэтому при патологии почек легко теряются с мочой. Однако их потеря не оказывает существенного влияния на онкотическое давление крови, потому что их содержание в плазме крови невелико.
Функции 1-глобулинов
1. Транспортная. Транспортируют липиды, при этом образуют с ними комплексы - липопротеины. Среди белков этой фракции есть специальный белок, предназначенный для транспорта гормона щитовидной железы тироксина - тироксин-связывающий белок.
2. Участие в функционировании системы свертывания крови и системы комплемента- в составе этой фракции находятся также некоторые факторы свертывания крови и компоненты системы комплемента.
3. Регуляторная функция. Некоторые белки фракции1-глобулинов яляются эндогенными ингибиторами протеолитических ферментов. Наиболее высока в плазме концентрация1-антитрипсина. Содержание его в плазме от 2 до 4 г/л (очень высокое), молекулярная масса - 58-59 кДа. Главная его функция - угнетение эластазы - фермента, гидролизующего эластин (один из основных белков соединительной ткани).1-антитрипсин также является ингибитором протеаз: тромбина, плазмина, трипсина, химотрипсина и некоторых ферментов системы свертывания крови. Количество этого белка увеличивается при воспалительных заболеваниях, при процессах клеточного распада, уменьшается при тяжелых заболеваниях печени. Это уменьшение - результат нарушения синтеза1-антитрипсина, и связано оно с избыточным расщеплением эластина. Существует врожденная недостаточность1-антитрипсина. Считают, что недостаток этого белка способствует переходу острых заболеваний в хронические.
К фракции 1-глобулинов относят также1-антихимотрипсин. Он угнетает химотрипсин и некоторые протеиназы форменных элементов крови.
2-ГЛОБУЛИНЫ. Высокомолекулярные белки. Эта фракция содержит регуляторные белки, факторы свертывания крови, компоненты системы компемента, транспортные белки. Сюда относится ицерулоплазмин. Этот белок имеет 8 участков связывания меди. Он является переносчиком меди, а также обеспечивает постоянство содержания меди в различных тканях, особенно в печени. При наследственном заболевании - болезни Вильсона - уровень церулоплазмина понижается. Вследствие этого повышается концентрация меди в мозге и печени. Это проявляется развитием неврологической симптоматики, а также циррозом печени.
126.
Методом высаливания можно получить три фракции белков плазмы крови: альбумины, глобулины, фибриноген. Электрофорез на бумаге позволяет разделить белки плазмы крови на 6 фракций:
Альбумины - 54-62%, Глобулины: 1-глобулины 2,5-5%,2-глобулины 8,5-10%,-глобулины 12-15%,-глобулины 15,5-21%,фибриноген (остается на старте) - от 2 до 4%.
Современные методы позволяют получить свыше 60 индивидуальных белков плазмы крови. Количественные соотношения между белковыми фракциями постоянны у здорового человека. Иногда нарушаются количественные соотношения между различными фракциями плазмы крови. Это явление называется ДИСПРОТЕИНЕМИЯ. Бывает, что содержание общего белка плазмы при этом не нарушается.
Иногда содержание общего белка плазмы понижается. Такое явление известно как ГИПОПРОТЕИНЕМИЯ. Может развиться: а) при длительном голодании; б) когда есть патология почек (потеря белка с мочой).
Реже, но иногда встречается ГИПЕРПРОТЕИНЕМИЯ - повышение содержания белка в плазме выше, чем 80г/л. Такое явление характерно для состояний, при которых происходит значительные потери жидкости организмом: неукротимая рвота, профузный понос (при некоторых тяжелых инфекционных заболеваниях: холера, тяжелая форма дизентeрии).
129.
. Кислотно - основное равновесие– солтношение концентраций водородных и гидроксильных ионов в биологических средах.
Состоянию нормы соответствует определенный диапазон колебаний рН крови – с 7.37 до 7.44 со средней величеной 7.40. Регуляторными системами, которые обеспечивают постоянство рН крови являются буферные с-мы.
Бикарбонатная– самая управляемая с-ма клеточной жидкости и крови. Состоит из углекислоты и бикарбонатов. Механизм её действия заключается в том, что при выделении в кровь больших кол-в кислых продуктов водородные ионы соединяются с анионами бикарбоната, что приводит к образованию слабодиссациирующей угольной к-ты, избыток которой сразу разлагается на Н2О и СО2, который удаляется ч-з легкие при гипервентиляции. И так, несмотря на снижение уровня концентрации бикарбоната в крови, нормальное соотношение м-у концентрацией Н2СО3 и бикарбоната (1:20) сохраняется. рН крови остается в норме. Если в крови увеличивается кол-во основных ионов, то они соединяются со слабой угольной к-той образуя ионы бикарбоната и воду. Для сохранения нормальных соотношений основных компонентов буферной с-мы в этом случае подключаются физиологические механизмы регуляции кислотноосновного состояния: происходит задержка в плазме крови некоторого количестваСО2 в результате гиповентиляции легких, а почки начинают выделять основные соли в большем кол-ве.
Фосфатная.Буферное действие этой системы основано на возможности связывания водородных ионов ионами НРО42-с образованием Н2РО4-(Н+ + НПО42- --- Н2РО4-), а так же на взаимодействие ионов ОН-с ионами Н2РО4-(ОН-+ Н2РО42---- НРО42-+ Н2О). эта система находится в тесной связи с бикарбонатной.
Белковая. При сдвиге рН в щелочную сторону диссоциация основных групп угнетается и белок ведет себя как к-та. Связывая основания эта к-та дает соль. С увеличением рН возрастает кол-во белков в ф-ме соли, а при уменьшении растет количество белков плазмы в ф-ме к-ты.
Гемоглобиновая – самая мощная с-ма крови. Участие гемоглобина в регуляции рН крови связана с его ф-ей – транспорт О2. Константа диссоциации кислотных групп гемоглобина меняется в зависимости от его насыщения О2. При насыщении он становится боле сильной к-той(ННbО2) и увеличивает отдачу в р-р ионов Н2. если гемоглобин отдает О2, он становится очень слабой органической к-той (ННb).
Нарушение кислотно - основное равновесия – ацидоз.
130.
эритроциты(в 1мл. 5*109, Эритроциты живут 100-120 дней. Ежедневно образуется 250 млрд эритроцитов.) – красные кровяные клетки лишенные ядра, ибосом, митохондрий, лизосом. Образуются в красном костном мозге. Продолжительность жизни 125 дней, разрушаются в селезенки и в печени. Почти целиком заполнены гемаглабином.
Главная функция - транспорт газов: перенос О2и СО2. Он возможен благодаря большому содержанию гемоглобина и высокой активности фермента карбоангидразы.
Обмен эритроцитов имеет ряд особенностей:
1. В зрелых эритроцитах не идут реакции биосинтеза белков.
2. Образование энергии - только путем гликолиза, субстрат - только глюкоза.
В эритроцитах существуют механизмы предохранения гемоглобина от окисления:
1. Активно протекает ГМФ-путь распада глюкозы, дающий НАДФ.H2
2. Высока концентрация глютатиона - пептида, содержащего SH-группы
131.
Гемоглобин(Hb) имеет молекулярную массу 80000 Да. Это сложный белок с четвертичной структурой: состоит из нескольких субъединиц. У Hb 4 субъединицы. Каждая субъединица состоит из небелковой части - гема и белка глобина (всего 4 гема и 4 глобина в молекуле гемоглобина).
СИНТЕЗ ГЕМА
дельта-аминолевулинатсинтаза является ключевым ферментом биосинтеза гема. Коферментом дельта-аминолевулинатсинтазы является пиридоксаль-фосфат (производное витамина В6). Фермент ингибируется по принципу отрицательной обратной связи избытком гема.
Порфобилиногенсинтаза тоже угнетается избытком гема.
Необходимо знать схему дальнейших реакций, протекающих при синтезе гема:
Гем имеет тетрапиррольную структуру, т.е. состоит из 4-х замещенных пиррольных колец, соединенных между собой с помощью метиновых мостиков. Эта структура называется порфирином (без железа). Протопорфирин, в который включено железо, называется ГЕМ.
Железо в Hb имеет степень окисления “+2” и координационное число 6. Двумя ковалентными связями Fe связано с азотами пиррольных колец. Две координационные связи идут на связь с остатками гистидина в молекулах глобина. Белковая часть Hb состоит из 4-х попарно одинаковых протопорфириновых циклов.
Молекула HbA (Hb взрослого человека) содержит- 2 альфа- и 2 бета-полипептидные цепи. Этот тип гемоглобина составляет приблизительно 95-97% от всего количества гемоглобина в крови.
HbA2(2 альфа- и 2 дельта-цепи) у взрослого примерно 2%.
HbF (2 альфа и 2 гамма-цепи) - примерно 2% у взрослого. HbF - фетальный гемоглобин. В крови новорожденного такого гемоглобина содержится примерно 80%. В отличие от HbA этот тип гемоглобина имеет гораздо большее сродство к кислороду.
Сейчас установлено 5 видов HbA. Все они имеют 2 альфа- и 2 бета-цепи, но в минорных формах HbA присоединяются остатки простых сахаров (глюкозы) - гликозилированные формы гемоглобина.
У больных сахарным диабетом гликозилированных форм гемоглобина больше, чем у здоровых людей. Если снизить уровень сахара крови, то количество гликозилированнных форм снижается.
В крови человека иногда встречаются аномальные формы гемоглобина, которые отличаются от нормального Hb по аминокислотному составу полипептидных цепей. При этом изменяются изоэлектрическая точка, заряд, форма белковой молекулы. Заболевания, которые связаны с изменением структуры полипептидных цепей называются гемоглобинопатиями.
Серповидноклеточная анемия - характеризуется появлением HbS. В бета-цепи глутаминовая кислота заменена на валин вследствие мутации. Это приводит к изменению свойств Hb. Возрастает гидрофобность молекулы. Молекулы агрегируют. Эритроцит под микроскопом выглядит как серп.
В ряде случаев наблюдается одно из нарушений синтеза нормальных цепей Hb. Если нарушается синтез бета-цепей - то заболевание называется: бета-талассемия. Если нарушен синтез альфа-цепи, то альфа-талассемия.
134.
РАСПАД ГЕМОГЛОБИНА
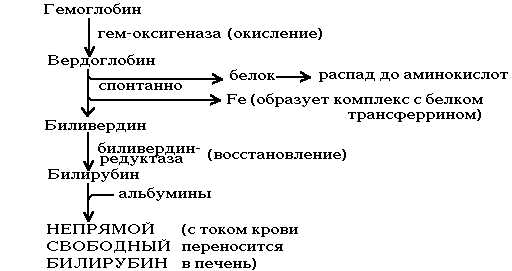
Происходит в мононуклеарных фагоцитах (в селезенке и печени). Сначала происходит разрыв связи между I-м и II-м кольцами. Фермент - НАДзависимая оксигеназа. После ее действия образуется пигмент зеленого цвета - вердоглобин. В его составе сохраняется и железо и белок. В дальнейшем вердоглобин распадается на составные части: белок, железо и пигмент-биливердин. Железо образует комплекс с белком трансферрином, и этот комплекс поступает в ткани, где оно снова может быть использовано для синтезов или депонироваться в виде комплекса с белком ферритином.
Билирубин плохо растворим в воде, поэтому он адсорбируется на альбумине крови. Такой комплекс называется СВОБОДНЫМилиНЕПРЯМЫМ БИЛИРУБИНОМ. Он свободный, потому что не связан ни с каким другим веществом ковалентными связями; непрямой, потому что не дает прямой реакции с диазореактивом Эрлиха (для определения этого вида билирубина необходимо предварительно осадить альбумины).
В печени непрямой билирубин подвергается обезвреживанию путем связывания с глюкуроновой кислотой. В реакции расходуется УТФ. При этом к молекуле билирубина присоединяются 2 молекулы глюкуроновой кислоты (образование билирубиндиглюкуронида). Это вещество малотоксично и хорошо растворяется в воде, называется ПРЯМЫМ СВЯЗАННЫМ БИЛИРУБИНОМ, т.к. определяется в прямой реакции с диазореактивом Эрлиха и связан ковалентно с глюкуроновой кислотой. В таком виде билирубин поступает в желчь и вместе с ней выводится из организма.
При определении содержания билирубина используют диазореактив Эрлиха, который дает розовую окраску с билирубином и по ее интенсивности судят о концентрации билирубина в крови.
В крови человека примерно 75% непрямого билирубина от его общего количества. Общее содержание билирубина в норме (прямой+непрямой) от 8 до 20 мкмоль/л.
Билирубин - это конечный продукт распада гемоглобина у человека. Однако, поступив с желчью в кишечник, он превращается под действием ферментов микрофлоры кишечника. Сначала от него отщепляется глюкуроновая кислота, затем происходит частичное восстановление и образуется вещество, называемое "мезобилиноген", а затемстеркобилиноген. Стеркобилиноген в основном выводится с калом и на воздухе (в кале) превращается в стеркобилин, а мезобилиноген частично всасывается из кишечника по системе v.portae, т.е. попадает в печень и там разрушается. Поэтому его нет у здоровых людей в крови. Небольшая часть стеркобилиногена тоже всасывается из кишечника через систему геморроидальных вен, т.е. попадает сразу в большой круг кровообращения, минуя печень, поэтому часть его выводится с мочой.
Значит, стеркобилиноген является компонентом мочи в норме.
В НОРМЕ:
Кровь:
Билирубин (в основном непрямой) - в норме (8-17мкмоль/л)
Гемоглобин - в норме (мужчины - 130-145 г/л; женщины - 110-130 г/л
Моча: светло-желтого цвета, стеркобилиноген - в норме, мезобилиногена нет.
Кал: нормальной окраски, стеркобилиноген - в норме
135.
ГЕМОЛИТИЧЕСКАЯ ЖЕЛТУХАНаблюдается при усилении распада эритроцитов. Билирубина образуется больше, чем в норме и скорость экскреции тоже увеличивается. Непрямой билирубин повышается в крови. В моче билирубина нет, а содержание стеркобилина в кале и в моче повышено.
136.
ПАРЕНХИМАТОЗНАЯ ЖЕЛТУХА(паренхиматозная). Наблюдается при повреждении гепатоцитов (например, при вирусном гепатите). Билирубин не обезвреживается. Желчные пигменты поступают не только в кишечник, но и в кровь. Т.е. в крови повышается содержание не только прямого, но и непрямого билирубина. Наблюдается билирубинурия. В моче обнаруживают мезобилиноген.
137.
ОБТУРАЦИОННАЯ ЖЕЛТУХА(механическая) Наблюдается при закупорке желчных протоков (например, при желчнокаменной болезни). Желчь продолжает вырабатываться, но поступает не только в желчные протоки, а также в кровь. В крови повышается уровень билирубина, в основном - прямого билирубина. Наблюдается билирубинурия. Содержание стеркобилина в моче и в кале снижено (кал становится светлым, а моча темнеет за счет прямого билирубина).
138.
ЛЕЙКОЦИТЫ
Клетки, выполняющие защитные функции - способны к фагоцитозу. В лейкоцитах много активных протеаз, расщепляющих чужеродные белки. В момент фагоцитоза увеличивается выработка перекиси водорода и увеличивается активность пероксидазы, что способствует окислению чужеродных частиц (антибактериальное действие). Лейкоциты богаты внутриклеточными низкоспецифичными протеиназами - катепсинами, локализованными в лизосомах. Катепсины способны к практически тотальному протеолизу белковых молекул. В лизосомах лейкоцитов в значительных количествах содержатся и другие ферменты: например, рибонуклеазы и фосфатазы.
139.
СИСТЕМА СВЕРТЫВАНИЯ КРОВИ И ФИБРИНОЛИЗА.
Это единая система, которая выполняет следующие функции:
1) Поддержание крови в сосудах в жидком состоянии.
2) Осуществление гемостаза (предотвращение больших кровопотерь).
Гемостаз - сложный ферментативный процесс, в результате которого образуется кровяной сгусток.
Система свертывания крови - это многокомпонентная система, в состав которой входят белки, фосфолипиды, обломки клеточных мембран и ионы кальция.
Компоненты системы свертывания крови принято называть "факторами". Факторы бывают тканевыми, плазменными и тромбоцитарными. Тканевые и плазменные факторы обозначаются римскими цифрами, а тромбоцитарные - арабскими. Если фактор является активным, то за цифрой ставится буква "а".
Большинство белков системы свертывания крови обладает ферментативной активностью. Все факторы свертывания крови, кроме фXIII, являются сериновыми протеиназами, которые катализируют реакции ограниченного протеолиза.
В ходе реакций свертывания крови все белки-ферменты сначала выступают в роли субстрата, а затем - в роли фермента. Среди белков, участвующих в свертывании крови, есть такие, которые не обладают ферментативной активностью, но специфически ускоряют протекание ферментативной реакции. Они называются параферментами. Это фV (проакцелерин) и фVIII(антигемофильный глобулин А).
Большинство факторов свертывания крови синтезируется в неактивной форме в виде проферментов. Проферменты активируются и их действие направлено на протекание прямой реакции свертывания крови - на превращение фибриногена в фибрин, которой является основой кровяного сгустка.
Есть 2 механизма свертывания крови - внешний и внутренний.
ВНЕШНИЙ механизм запускается с участием внешних(тканевых) факторов, ВНУТРЕННИЙ - при участии факторов, источником которых служит сама кровь, плазма, собственно ферменты и форменные элементы крови. РАЗЛИЧАЮТСЯ ВНЕШНИЙ И ВНУТРЕННИЙ МЕХАНИЗМЫ ТОЛЬКО НАЧАЛЬНЫМИ СТАДИЯМИ ДО АКТИВАЦИИ ПРОТРОМБИНА (фII - протромбин). ПОСЛЕДУЮЩИЕ СТАДИИ ПРОТЕКАЮТ ОДИНАКОВО И В ТОМ, И В ДРУГОМ СЛУЧАЯХ.
НАЧАЛЬНЫЕ СТАДИИ ВНЕШНЕГО МЕХАНИЗМА.
Для пуска внешнего механизма необходим первичный сигнал: повреждение тканей (клеток), оказавшихся в контакте с кровью, или эндотелия сосуда. При этом разрушаются клеточные мембраны и из клеток высвобождается тканевой тромбопластин (фIII ). Он активирует фVII - прконвертин.
Активация фVII, а также все последующие реакции до активации протромбина протекают на матрице, которая состоит из липопротеиновых осколков клеточных мембран. В ходе активации фVII происходит конформационная перестройка его молекулы, в результате формируется активный центр этого белка-фермента.
Активный фVIIa образует комплекс с тканевыми фосфолипидами и ионом кальция. Этот комплекс обладает протеолитической активностью и вызывает активацию фактора X (Прауэра-стюарта).
Активный фактор Xа тоже обладает протеолитической активностью и активирует протромбин.
НАЧАЛЬНЫЕ СТАДИИ ВНУТРЕННЕГО МЕХАНИЗМА.
Начальные стадии внутреннего механизма называются "контактная фаза" или“контактная стадия”.Происходит контакт фXII (хагемана) с чужеродной поверхностью (например, игла шприца, лезвие ножа, стекло). В результате происходит конформационная перестройка фXII и он активируется - переходит в фXIIa.
Активация фXII, а также последующие реакции внутреннего механизма, так же, как и при внешнем механизме, протекают на матрице - тромбопластине, который освобождается при разрушении тромбоцитов.
XIIa действует на XI (Розенталя), превращая его в XIa.
XIa действует на фIX (антигемофильный глобулин В) (обязательно в присутствии ионов кальция!), и переводит его в фIXa.
фIXa образует комплекс с тромбоцитарными фосфолипидами, ионами кальция и параферментом - фVIIIa. В составе этого комплекса фIXa обладает протеолитической активностью и переводит фX в фXa.
Следующие стадии, начиная с активации протромбина (фII), протекают одинаково для обоих механизмов свертывания крови.
Протромбин - белок, который синтезируется в печени. Для синтеза протромбина необходим витамин "К". Реакция синтеза протромбина катализируется комплексом, состоящим из активного фXa, фосфолипидов, иона кальция и парафермента Va. В ходе этой реакции резко уменьшается сродство данного комплекса к матрице и активный тромбин,или фIIa, освобождается с матрицы и гидролизует пептидные связи между аргинином и глутаминовой кислотой в молекуле своего субстрата - фибриногена, превращая его в фибрин-мономер.
На следующей стадии мономеры фибрина спонтанно агрегируют с образованием регулярной полимерной структуры "мягкого" сгустка растворимого фибрин-полимера. При этом происходит захват фибрин-полимером компонентов крови - формируется тромб (сгусток).
Сначала сгусток рыхлый и мягкий, связи между молекулами фибрин-полимера слабые (нековалентные). Но затем под действием активного фXIIIa (фибриназа) (фXIII активируется фактором IIa - тромбином) происходит прочная ковалентная “сшивка” молекул фибрин-полимера. Образуются межмолекулярные связи между карбоксильными группами глутамина и аминогруппами лизина: так растворимый фибрин-полимер переходит в нерастворимый фибрин-полимер.
После образования нитей фибрина происходит их сокращение (ретракция кровяного сгустка), которое происходит с затратой АТФ.
Процесс тромбообразования постоянно контролируется антитромбином III - ингибитором сериновых протеиназ. Кроме того, протекание большинства реакций свертывания крови на матрице обеспечивает:
1) высокую эффективность процесса
2) локальность процесса - процесс свертывания протекает только в месте повреждения (это предотвращает процесс диссеминированного внутрисосудистого свертывания (ДВС-синдром).
Скорость свертывания крови зависит не только от работы системы свертывания, но и от присутствия естественных антикоагулянтов - веществ, предотвращающих свертывание крови.
154.
Внутренняя поверхность дыхательных путей покрыта тонким слоем слизи. Слизь имеет в своем составе растворенные в воде ионы Na+, Cl–, K+, Ca2+, муцины, сульфатированные протеогликаны, сурфактант, лизоцим, лактоферрин и секреторный IgA. Разные компоненты слизи синтезируются в разных отделах дыхательных путей и даже в респираторном отделе легких (вода, ионы, сурфактант), источником муцинов являются подслизистые железы.
- альбумины - Биохимия
Глобулярный белок плазмы крови, синтезируется исключительно в печени. Хотя по классификации его относят к простым белкам, отмечается широкая микрогетерогенность молекул альбумина, что связано с количеством и качеством агрегированных с альбумином молекул.
Физиологическое значение альбумина заключается:
1. В поддержании коллоидно-осмотического (онкотического) давления крови (благодаря высокой гидрофильности).
2. Транспортная функция – благодаря большому количеству заряженных и гидрофобных участков альбумин связывает и переносит
- пигменты (билирубин) – одна молекула альбумина может одновременно связать 25-50 молекул билирубина,
- длинноцепочечные жирные кислоты – основная физиологическая функция, 6-8 штук на одну молекулу альбумина,
- катионы (в основном Ca2+ и Mg2+, и другие металлы, например Hg+) благодаря большому количеству глутамата,
- анионы, например Cl–,
- соли желчных кислот,
- витамины,
- гормоны (альдостерон, прогестерон, гидрокортизон),
- органические красители,
- лекарственные вещества (дигоксин, барбитураты, пенициллин, ацетилсалициловая кислота, сердечные гликозиды).
Клинико-диагностическое значение
Изменения концентрации альбумина в крови могут иметь как абсолютный (истинный), так и относительный характер. Сдвиги абсолютного характера являются следствием колебаний содержания белка в крови. В свою очередь, относительные изменения зависят от объема крови, т.е. наблюдаются при обезвоживании или гипергидратации.
Гиперальбуминемия
Истинное повышение концентрации белка в крови обычно не наблюдается.
Относительная гиперальбуминемия вызывается потерями внутрисосудистой жидкости в результате профузных поносов (например, холере), усиленном потоотделении, неукротимой рвоте, несахарном диабете, при тяжелых и обширных ожогах и генерализованных перитонитах.
Гипоальбуминемия
Истинная (абсолютная) гипоальбуминемия связана:
- с недостаточным потреблением белка с пищей – заболевания желудочно-кишечного тракта, сужение пищевода при опухолях, частичное или полное голодание;
- со снижением синтеза белка в печени – несбалансированный аминокислотный состав пищи, хронические паренхиматозные гепатиты, интоксикации, злокачественные новообразования, лечение кортикостероидами;
- с усиленным распадом белка – кахексия, тяжелые инфекции, длительные воспалительные процессы, лихорадочные состояния, тиреотоксикозы;
- с потерей белка – нарушения проницаемости капиллярных стенок, кровоизлияния, ожоги, острые и хронические кровотечения, нефротический синдром.
Относительная гипоальбуминемия связана с нарушением водного баланса – гипергидратация при гиперальдостеронизме, при почечной недостаточности со снижением экскреции солей, при использовании для питья морской воды, при неадекватных инфузиях солевых растворов.
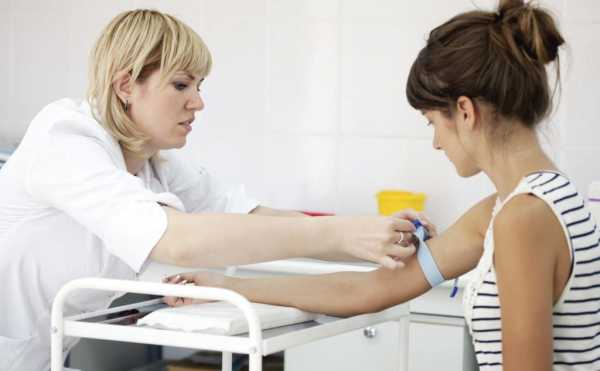
Альбумин в крови - что это такое? Норма альбумина в анализах у женщин и мужчин
Уровень альбумина в крови определяется с помощью биохимического анализа. Завышенные или заниженные показатели вещества, получаемого путем фракционирования, свидетельствуют о патологическом процессе в организме.
Альбумин или белковые фракции — наиболее часто встречающиеся исследуемые показатели, ведь вещество отражает, насколько полноценно работает печень по синтезу белков.
Интересный факт: в течение 2 суток печень продуцирует 15 грамм альбумина, приносящего пользу до 20 дней.
Альбумин — что это такое в биохимическом анализе крови?
Альбумин — основной белок в крови, составляющий более половины (от 50 до 65%) от общего количества плазмы. Синтезируется печенью человека и располагается в периферийной крови, лимфе, спинномозговой и интерстициальной жидкости. Жизненный период альбумина длится 15-20 суток. Белковое соединение низкомолекулярно, хотя фракция белков плазмы крови резервирует более 600 разновидностей аминокислот.
По результатам биохимического анализа крови и содержанию в кровяной сыворотке альбумина врач диагностирует работу почек и печени. Снижение концентрации белкового соединения указывает на наличие ревматизма и опухолей злокачественного характера.
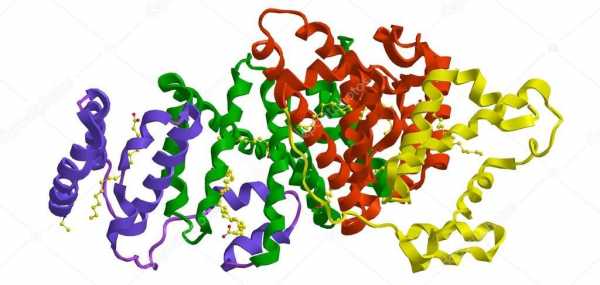 На картинке: молекулярная структура сывороточного альбумина человека
На картинке: молекулярная структура сывороточного альбумина человекаАльбумины — важнейшие элементы в кровяной сыворотке, благодаря которым осуществляется полноценная деятельность организма.
Белки циркулируют с кровотоком и выполняют следующие функции:
- наиважнейшая функция белковой фракции — связь и транспортировка различных веществ — гормонов, кислот, жиров, билирубина, кальция, соединения тканей.
- Отвечает за поддержание давления в плазме крови, благодаря чему жидкость не вызывает отеков, не проникает в соединительную и мышечную ткань.
- Резервное назначение — сохранение элементов белка. Молекулы альбумина отвечают за сохранность аминокислот, необходимых для правильного функционирования организма. Во время длительного голодания запасы аминокислот истощаются.
к содержанию ↑Внимание! Не игнорируйте врачебные рекомендации относительно сдачи биохимического анализа. Благодаря биохимии крови диагностируются патологии, связанные с колебаниями альбумина. Своевременная сдача анализа способствует предотвращению развития патологии и назначению эффективного лечения.
Альбумин: норма в крови
Нормы альбуминовой фракции в крови колеблются в пределах 35 -33 г / л, это намного больше содержания гамма-глобулина (8,0 — 12,0 — 17,0 г / л) и фибриногена (2,0 — 4,0 г / л), а в кровяной сыворотке фибриноген заметить затруднительно.
Нормы белка установлены в зависимости от возрастной категории людей. При сдаче анализа нормальный уровень в плазме у мужчины и женщины одинаковый, поэтому врач опирается на норму альбумина, исходя из возраста пациента.
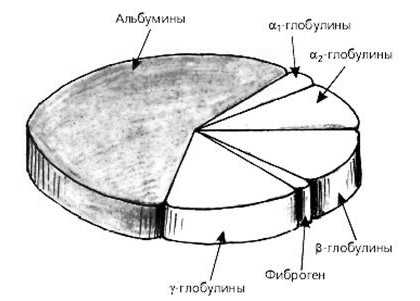 Изображено: доли белков в крови человека
Изображено: доли белков в крови человекаНиже представлены нормы крови в зависимости от возрастной категории пациентов:
- Малыши с рождения до 3 лет — 25 — 50 г / л;
- Дети с 3 до 14 лет — 38 — 54 г / л;
- 14 — 60 лет — 33 — 55 г / л;
- Пожилые люди старше 60 лет — 34 — 48 г / л.
к содержанию ↑Стоит отметить, что: у людей зрелого возраста замечается понижение уровня альбумина в крови.
Таблица норм по возрастам
| Возраст | Альбумин, г/л | α1, г/л | α2, г/л | β, г/л | γ, г/л |
|---|---|---|---|---|---|
| От 0 до 7 дней | 32,5 – 40,7 | 1,2 – 4,2 | 6,8 – 11,2 | 4,5 – 6,7 | 3,5 – 8,5 |
| От 1 недели до года | 33,6 – 42,0 | 1,24 – 4,3 | 7,1 – 11,5 | 4,6 – 6,9 | 3,3 – 8,8 |
| От 1 года до 5 лет | 33,6 – 43,0 | 2,0 – 4,6 | 7,0 – 13,0 | 4,8 – 8,5 | 5,2 – 10,2 |
| От 5 до 8 лет | 37,0 – 47,1 | 2,0 – 4,2 | 8,0 – 11,1 | 5,3 – 8,1 | 5,3 – 11,8 |
| От 8 до 11 лет | 40,6 – 45,6 | 2,2 – 3,9 | 7,5 – 10,3 | 4,9 - 7,1 | 6,0 – 12,2 |
| От 11 лет до 21 года | 38,9 – 46,0 | 2,3 – 5,3 | 7,3 – 10,5 | 6,0 – 9,0 | 7,3 – 14,3 |
| После 21 года | 40,2 – 50,6 | 2,1 – 3,5 | 5,1 – 8,5 | 6,0 – 9,4 | 8,1 – 13,0 |
Норма альбумина в крови у женщин
Исследуя биохимический анализ крови беременной женщины, замечается снижение концентрации белка в плазме. Норма содержания альбумина во время вынашивания ребенка, в период лактации составляет 30 -34 г / л.
После родов и по окончании грудного вскармливания уровень белкового соединения в женском организме нормализуется до привычных значений.
Важная информация! Повышение или понижение альбумина обусловлено внешними и внутренними факторами и указывает на патогенный процесс в организме представительницы женского пола.
Иногда недостаток белка вызван физиологическими особенностями, ведь белки выделяются в организм будущей мамы и поступают к плоду. Сбалансированное питание, полноценный отдых способствуют нормализации альбумина у беременной.
к содержанию ↑Норма альбумина в крови у мужчин
Нормальный уровень альбумина у представителей мужского пола средних лет составляет 33 — 55 г/ л.
к содержанию ↑Норма альбумина у детей
Детские показатели также зависят от возраста и чем младше ребенок, тем ниже содержание альбумина в крови:
- 0 — 7 дней — 32,5 — 40,7 г/ л;
- 7 дней — 12 месяцев — 33,6 — 42,0 г/ л;
- 1 год — 5 лет — 33,6 — 43,0 г/ л;
- 5 — 8 лет — 37,0 — 47,1 г/ л;
- 8 — 11 лет — 40,6 — 45,6 г/ л;
- 11 лет — 21 год — 38,9 — 46 г/ л.
У юношей и девушек старше 21 года концентрация белкового соединения в крови варьируется в пределах 40,2 — 50,6 г/ л.
к содержанию ↑Внимание! Референтные значения в анализе, сдаваемом в разных лабораториях, различны. При сомнениях в результате проведения биохимического теста предлагается пересдать кровь в другом медицинском учреждении.
Норма белковых фракций в сыворотке крови
| Белковые фракции в плазме крови | Норма, г/л | Соотношение групп, % |
|---|---|---|
| Общий белок | 65 – 85 | |
| Альбумин | 35 - 55 | 54 - 65 |
| α1 (альфа-1)-глобулины | 1,4 – 3,0 | 02.05.2018 |
| α2 (альфа-2)- глобулины | 5,6 – 9,1 | 01.07.2013 |
| β (бета)-глобулины | 5,4 – 9,1 | 01.08.2015 |
| γ (гамма)-глобулины | 8,1 – 12,0 | 01.12.2022 |
| Фибриноген * | 2,0 – 4,0 |
Если альбумин повышен в крови — что это значит?
Если по результатам биохимии заметно повышение уровня альбумина, констатируется гиперальбуминемия, которая свидетельствует чаще всего о дегидратации (обезвоживании) организма.
Частые приступы рвоты, длительная диарея способствуют патологическому уменьшению жидкости в организме. Это становится причиной загустения крови и отрицательно сказывается на состоянии здоровья.
Другая причина повышенного уровня белка — сильное переутомление.
Повышенный уровень альбумина диагностируется редко.
Но при установке гиперальбуминемии диагностируются следующие заболевания:
- поражение желудочно-кишечного тракта холерным вибрионом;
- инфекционные заболевания;
- кишечная непроходимость;
- системная красная волчанка;
- плазмоцитома;
- ревматоидный артрит;
- пиелонефрит;
- сахарный диабет;
- гепатит, цирроз печени;
- химические, термические или лучевые повреждения кожи;
- длительный прием сильнодействующих лекарственных препаратов — глюкокортикостероидов или бромсульфалеина.
Для понижения белка рекомендовано придерживаться определенных немедикаментозных способов:
- придерживание диеты с употреблением низкокалорийной пищи, избегать продуктов с высоким содержанием белков и углеводов, сделать акцент на вареной, тушеной, пареной еде с исключением жареных, соленых, острых блюд;
- отказаться от употребления спиртных напитков, так как пораженная алкоголем почка не способна производить полноценный синтез и абсорбцию белков;
- прекратить курить — у заядлых курильщиков повышается риск развития гипертонии, что влияет на чрезмерное содержание альбумина в крови. Специалисты советуют постепенно бросать курить, иначе вероятно осложнение состояния;
- употреблять большое количество жидкости — не менее 2 литров в день во избежание обезвоживания и образования тромбов.
При отсутствии улучшений в анализе врач назначает применение медикаментов с использованием препаратов группы ингибиторов или лекарств, ускоряющих регуляцию синтеза холестерина в организме.
к содержанию ↑Низкий альбумин: причины
При понижении содержания альбумина и достижении 25 — 30 г / л констатируется гипоальбуминемия.
Сниженная концентрация белка свидетельствует о таких состояниях как:
- злокачественный процесс в организме;
- воспалительное заболевание почек — диабетическая нефропатия, нефротический синдром;
- болезни пищеварительной системы;
- лейкемия, сепсис крови;
- дисфункции сердечно-сосудистой системы;
- функциональные нарушения печени — атрофия, цирроз, гепатит;
- поражение соединительной ткани;
- наличие сильных травм, ожогов;
- чрезмерное содержание воды в организме;
- отек легких;
- сильные кровопотери, переливание кровезаменителей;
- генетические патологии, вследствие которых уровень альбумина снижается;
- длительное голодание, вызванное придерживанием низкобелковой и несбалансированной диет.
Другие причины, из-за которых уровень альбумина снижается:
- прием некоторых медикаментов, особенно при передозировке;
- злоупотребление алкоголем и табакокурением.
 При повышенном уровне альбумина не поддавайтесь панике и не ищите у себя заболевания.
При повышенном уровне альбумина не поддавайтесь панике и не ищите у себя заболевания.
Пониженные показатели белка в биохимическом анализе появляются вследствие приема эстрогеносодержащих препаратов, голодания и употребления глюкокортикостероидов.
После получения результатов обратитесь к врачу для назначения дополнительных анализов.
к содержанию ↑Как повысить альбумин в крови?
Наиболее легкий способ повышения концентрации альбумина — ежедневное употребление продуктов с большим содержанием белков, жиров и клетчатки:
- яйца;
- молочные и кисломолочные продукты;
- курятина;
- овсянка;
- рыба, морепродукты;
- орехи и липиды;
- фрукты и овощи.
Питательный режим желательно согласовать с лечащим врачом.
Гипоальбуминемия часто связана с неправильной работой печени, поэтому врачи советуют исключить из рациона:
- соленое, копченое, жареное, острое;
- алкоголь.
Также важно пролечить инфекции, начать борьбу с ожирением, не злоупотреблять медикаментозными препаратами без назначения специалиста.
Другой метод повышения содержания белка — употребление печеночного чая. Травяной сбор способствует нормализации работы печени, очищает орган от шлаков и токсинов, улучшая общее состояние больного.
Напиток имеет минимум противопоказаний за исключением индивидуальной непереносимости и наличия камней в желчном пузыре, но перед применением желательно проконсультироваться с лечащим врачом.
 На фото: печеночный фито-чай
На фото: печеночный фито-чайПри гипоальбуминемии назначают препарат Альбумин. Лекарство вводится внутривенным струйным и капельным вливанием. Дозировка зависит от индивидуальных показаний, возраста и положения больного — иногда Альбумин применяется для лечения беременных женщин.
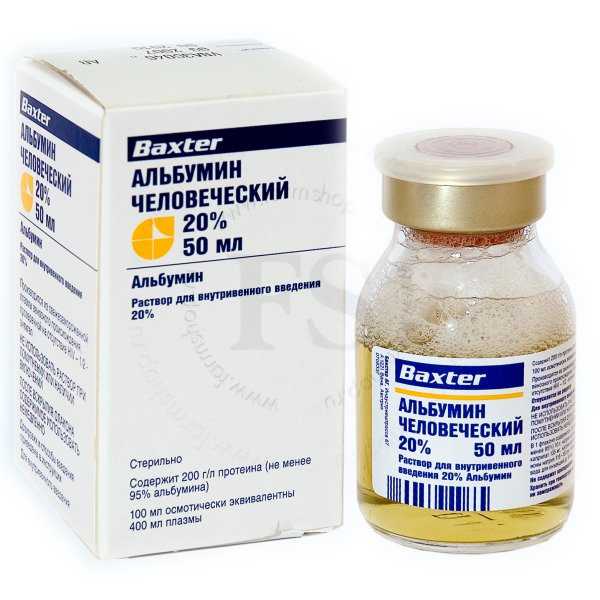 На фото: препарат Альбумин человеческий, 20%, 50 мл.
На фото: препарат Альбумин человеческий, 20%, 50 мл.Справка! Медикамент обладает противопоказаниями и рядом побочных действий, поэтому нельзя заниматься самолечением.
к содержанию ↑
Подготовка к сдаче анализа
Биохимический анализ крови производится натощак в утренние часы. За 12 часов до забора крови из вены рекомендуется исключить из рациона жареную, соленую, копченую пищу.
Желательно избегать стрессовых ситуаций, перенапряжений и занятий спортом.
к содержанию ↑Обратите внимание! Если заниматься перед сдачей анализа активными видами деятельности, спортом — это дает ложный результат или способствует повышению уровня альбумина.
Видео
- альбумины - Биохимия
Преальбумин
Перед фракцией альбуминов при использовании метода радиальной иммунодиффузии обнаруживается белок, образующий дугу преципитации, и получивший название преальбумин. Этот богатый триптофаном белок (ММ 60 кД) с периодом полужизни 1,9 сут синтезируется в печени и выполняет в основном транспортную функцию. В крови он циркулирует в очень прочном комплексе с ретинолсвязывающим белком, препятствует его выходу из кровеносного русла и ответственен за перенос ретинола в ткани. Имеются данные об участии преальбумина в транспорте тироксина и трийодтиронина (10‑20% всего количества гормонов).
Нормальные величины
| Сыворотка | 0,18‑0,38 г/л |
| Спинно-мозговая жидкость | 0,012-0,05 г/л |
Клинико‑диагностическое значение
Количество белка отражает функциональное состояние печени. Снижение уровня происходит при заболеваниях печени, особенно при остром вирусном гепатите, при хроническом гепатите, злокачественных новообразованиях с метастазом в печень.
Преальбумин является более ранним индикатором заболеваний, чем альбумин.
Альбумин
Следующая по подвижности фракция — альбуминовая, эта весьма гомогенная фракция синтезируется почти исключительно в печени. У человека выявлено восемь аутосомно наследуемых вариантов сывороточного альбумина. Молекула альбумина представляет собой эллипс размером 3×15 нм, состоит из одной полипептидной цепочки. Его третичная структура сформирована при помощи 17 дисульфидных связей и имеет три домена. Период полужизни молекулы альбумина составляет 19‑20 сут. Белок гетерогенен в отношении содержания свободных SH‑групп: он либо содержит SH‑группу, либо нет. Кроме того, отмечается микрогетерогенность молекул альбумина, что связано с количеством и качеством агрегированных с альбумином молекул. Значение альбумина в крови заключается:
- поддержание коллоидно-осмотического давления,
- это богатый и быстро реализуемый резерв белка,
- транспортная функция – связывание и перенос длинноцепочечных жирных кислот – основная физиологическая функция сывороточного альбумина.
Кроме того, альбумин переносит пигменты (билирубин), катионы (например, Ca2+ и Mg2+), анионы (Cl–), желчные кислоты, витамины, гормоны (альдостерон, прогестерон, гидрокортизон), органические красители, лекарственные вещества (дигоксин, барбитураты, пенициллин, ацетилсалициловая кислота, сердечные гликозиды).
Кроме электрофореза, cодержание альбумина определяют фотометрическими и иммунологическими методами. Для фотометрических способов определения используются бромкрезоловый зеленый, бромкрезоловый красный, натриевая соль бензойной кислоты и ряд других красителей. Наиболее специфичной является реакция альбумина с бромкрезоловым зеленым, в ацетатном буфере окраска развивается быстро и сохраняется в течение 2 часов. Особенностью метода является необходимость введения в реакцию детергентов для предотвращения преципитации комплекса альбумина с красителем, с этой целью используются катионные и анионные детергенты, но чаще применяют неионные детергенты — твин 20, бридж 35, твин 80, тритон Х‑100.
Указанный метод утвержден в качестве унифицированного.
Нормальные величины
| Сыворотка крови | 30-50 г/л |
Клинико-диагностическое значение
Сыворотка
Истинного повышения (гиперальбуминемии), обусловленного естественной причиной, не наблюдается.
Снижение содержания альбуминовой фракции происходит при состояниях, характеризующихся:
- пониженным синтезом в печени: врожденная анальбуминемия, белковое голодание, нарушение всасывания аминокислот, тяжелые поражения печени (цирроз, дистрофии, некроз, активный гепатит, амилоидоз печени), панкреатит,
- повышенным катаболизмом: лихорадка, кахексии, тяжелые инфекции, коллагенозы, тиреотоксикоз, болезнь Иценко-Кушинга (гиперфункция надпочечников),
- потерей альбумина через кожу, почки, желудочно-кишечный тракт при кровотечениях,
- воспалительные процессы, обусловленные выходом альбумина из кровотока в межклеточное пространство.
Концентрация альбумина <20 г/л сопровождается отеками.